cho 5,4g bột Al tác dụng với 4,48 l khí o2 (dktc)
a,Sau phản ứng chất nào còn dư?Tính m chất dư
b.Tính khối lượng sản phẩm thu đc
0
bài : cho 4,48(l) khí h2 tác dụng với 23,2g f2o3 đun nóng
a) chất nào còn dư phản ứng . Khối Lượng chất dư là bao nhiêu ?
b) tính khối lượng chất rắn thu đc sau phản ứng
\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{4,48}{22,4}=0,2mol\)
\(n_{Fe_2O_3}=\dfrac{m_{Fe_2O_3}}{M_{Fe_2O_3}}=\dfrac{23,2}{160}=0,145mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,145 > 0,2 ( mol )
1/15 0,2 2/15 ( mol 0
Chất còn dư là \(Fe_2O_3\)
\(m_{Fe_2O_3\left(du\right)}=n_{Fe_2O_3\left(du\right)}.M_{Fe_2O_3}=\left(0,145-\dfrac{1}{15}\right).160=12,53g\)
\(m_{Fe}=n_{Fe}.M_{Fe}=\dfrac{2}{15}.56=7,4666g\)
Bài 1: Đốt cháy 6,2(g) P trong bình chứa 6,72(l) khí O2 ở đktc.
a. Sau phản ứng chất nào còn dư và nếu dư thì với khối lượng bao nhiêu? b. Tính khối lượng sản phẩm thu được.
Bài 2: Cho 13g Zn tác dụng với 0,3 mol HCl sau khi kết thúc phản ứng thu được muối kẽm Clorua và khí H2.
a. Viết và cân bằng PTPƯ và cho biết sau khi kết thúc phản ứng thì chất nào còn dư và nếu dư thì dư với khối lượng bao nhiêu?.
b. Tính thể tích của H2 thu được.
Bài 3: Người ta cho 26 g kẽm tác dụng với 49 g H2SO4, sau phản ứng thu được muối ZnSO4, khí hidro và chất còn dư.
a. Viết phương trình phản ứng.
b. Tính thể tích (đktc) khí hidro sinh ra.
c. Tính khối lượng các chất còn lại sau phản ứng.
Bài 4: Nếu cho 4 gam CuO tác dụng với 2,92 g HCl.
a) Cân bằng PTHH.
b) Tính khối lượng các chất còn lại sau phản ứng.
Bài 5: Hòa tan hoàn toàn 15gam CaCO3 vào 200mL dung dịch HCl 2M.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ mol của các chất tan có trong dung dịch thu được.
Bài 6: Hòa tan hết 4,8 gam Magie vào 200 gam dung dịch H2SO4 loãng nồng độ 20%.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ chất tan có trong dung dịch sau phản ứng.
Bài 7: Cho 200 ml dung dịch NaOH nồng độ 2M vào 200 mL dung dịch HCl 4M.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ mol của chất tan trong dung dịch sau phản ứng.
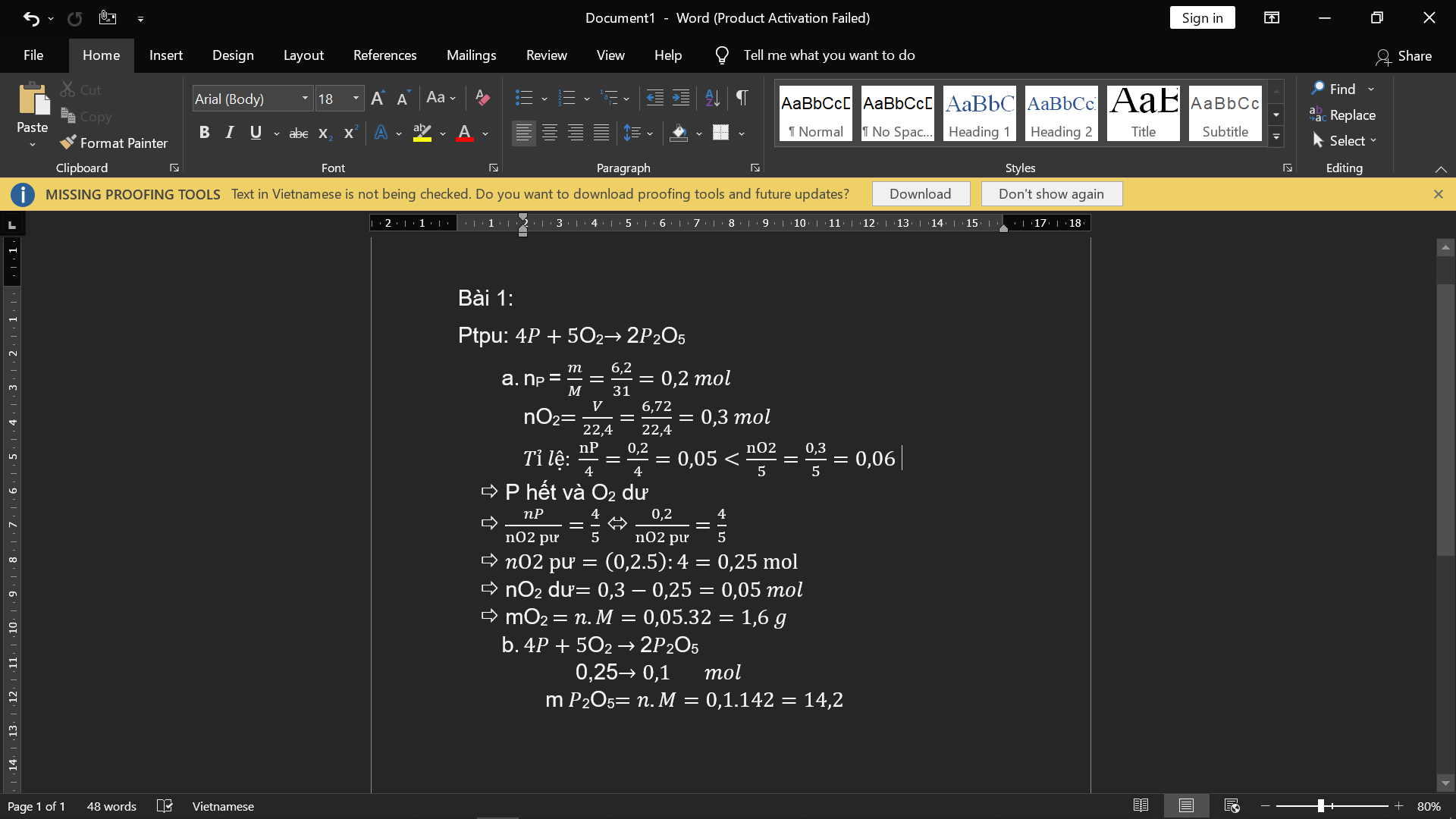
Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)
b ơi đây là bài 1 nka, tí mk làm xog sẽ gửi típ nka ![]()
Cho 3,36 lit khí H2 tác dụng với 1,12 lit khí O2( các thể tích đo ở đktc). Sau phản ứng thu được sản phẩm là H2O.
a) Chất nào còn dư? Dư bao nhiêu lit?
b) Tính khối lượng H2O thu được.
a, Theo gt ta có: $n_{H_2}=0,15(mol);n_{O_2}=0,05(mol)$
$2H_2+O_2\rightarrow 2H_2O$
Sau phản ứng $H_2$ còn dư. Và dư 0,05.22,4=1,12(l)
b, Ta có: $n_{H_2O}=2.n_{O_2}=0,1(mol)\Rightarrow m_{H_2O}=1,8(g)$
nH2 = 3.36/22.4 = 0.15 (mol)
nO2 = 1.12/22.4 = 0.05 (mol)
2H2 + O2 -to-> 2H2O
0.1___0.05_____0.1
VH2 (dư) = ( 0.15 - 0.1) * 22.4 = 1.12 (l)
mH2O = 0.1*18 = 1.8 (g)
Cho 4,8g Mg tác dụng với 6,72 lít khí O2 (đktc) . Sau phản ứng thu được Magie oxit MgO
a/ Chất nào còn dư sau phản ứng và dư bao nhiêu gam
b/ Tìm khối lượng sản phẩm thu được
a. \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH : 2Mg + O2 -> 2MgO
0,2 0,1 0,2
Xét tỉ lệ : \(\dfrac{0,2}{2}< \dfrac{0,3}{1}\) => Mg đủ , O2 dư
\(m_{O_2\left(dư\right)}=\left(0,3-0,1\right).32=6,4\left(g\right)\)
b) \(m_{MgO}=0,2.40=8\left(g\right)\)
\(a.n_{Mg}=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\\ 2Mg+O_2\rightarrow2MgO\\ LTL:\dfrac{0,2}{2}< \dfrac{0,3}{1}\Rightarrow O_2dư\\ n_{O_2\left(dư\right)}=0,3-0,1=0,2\left(mol\right)\\ m_{O_2}=0,2.32=6,4\left(g\right)\\ b.n_{MgO}=n_{Mg}=0,2\left(mol\right)\\ \rightarrow m_{MgO}=0,2.40=8\left(g\right)\)
cho 10,8 g Al tác dụng với 6,048 lít O2 điều kiện tiêu chuẩn
a, Lập phương trình hóa học
b, chất nào còn dư sau phản ứng và dư là bao nhiêu gam
c, Tính khối lượng sản phẩm thu được
\(PTHH:4Al+3O_2->2Al_2O_3\)
BĐ 0,4 0,27 (mol)
PU 0,36---->0,27---->0,18 (mol)
CL 0,04---->0------>0,18 (mol)
b)
\(n_{Al}=\dfrac{m}{M}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{6,048}{22,4}=0,27\left(mol\right)\)
\(\dfrac{n_{Al}}{4}>\dfrac{n_{O_2}}{3}\left(\dfrac{0,4}{4}>\dfrac{0,27}{3}\right)\)
=> Al dư, O2 hết (tính theo O2)
\(m_{Al}=n\cdot M=0,04\cdot27=1,08\left(g\right)\)
c)
\(m_{Al_2O_3}=n\cdot M=0,18\cdot\left(27\cdot2+16\cdot3\right)=18,36\left(g\right)\)
a, PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, Ta có: \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{6,048}{22,4}=0,27\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,4}{4}>\dfrac{0,27}{3}\), ta được Al dư.
Theo PT: \(n_{Al\left(pư\right)}=\dfrac{4}{3}n_{O_2}=0,36\left(mol\right)\)
\(\Rightarrow n_{Al\left(dư\right)}=0,4-0,36=0,04\left(mol\right)\)
\(\Rightarrow m_{Al\left(dư\right)}=0,04.27=1,08\left(g\right)\)
c, Theo PT: \(n_{Al_2O_3}=\dfrac{2}{3}n_{Al}=0,18\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,18.102=18,36\left(g\right)\)
Cho 12.395l khí Oxy cho tác dụng với 10.8g Nhôm sau phản ứng thu được Nhôm oxit AI2O3
a) Chất nào còn dư sau phản ứng và dư bao nhiêu g ?
b) Tính khối lượng sản phẩm thu được sau phản ứng
12,395l ở đk nào vậy em?
pthhL
\(3O_2+4Al\underrightarrow{t^o}2Al_2O_3\)
\(nO_2=12,395:24,9=0,5\left(mol\right)\)
\(nAl=\dfrac{10,8}{27}=0,4\left(mol\right)\)
Xét tỉ lê:
\(\dfrac{nO_2}{3}>\dfrac{nAl}{4}\)
=> Oxy dư và dư: \(mO_{2dư}=0,06.32=2g\)
b, tính theo pthh vì nO2 dư nên lấy số mol của Al
=> \(nAl_2O_3=\dfrac{2}{4}.0,4=0,2\left(mol\right)\)
\(\Rightarrow mAl_2O_3=0,2.102=20,4\left(g\right)\)
Bài 1:
Cho sơ đồ phản ứng sau: Mg + HCl ->MgCl2 + H2
Nếu cho 2,4g Mg tác dụng với 3,65g HCl. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng MgCl2 tạo thành và thể tích khí H2 thu được (đktc)
Bài 2:
Cho sơ đồ phản ứng sau: Al + H2SO4 -> Al2(SO4)3 + H2
Nếu có 5,4g nhôm tác dụng với 14,7g H2SO4. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng Al2(SO4)3 tạo thành và thể tích khí H2 thu được (đktc)
Bài 3:
Hòa tan hoàn toàn 3,78g với kim loại M (hóa trị III) vào dung dịch HCl thu được 4,704l khí H2 (đktc). Xác định kim loại M?
Bài 4:
Cho sơ đồ phản ứng sau: KMnO4 -> ..........+...........+O2
Tính thể tích Oxi (đktc) thu được khi nhiệt phân hủy hoàn toàn 0,4 mol KMnO4
Đốt cháy 6,2g photpho trong bình chứa lượng Oxi ở trên. Tính khối lượng điphotpho pentaoxit?
bạn từng câu lên sẽ dễ nhìn hơn
Đốt cháy 5,4 gam Al trong bình đựng 4,48 lít khí O2(đktc)
a. Chất nào còn dư sau phản ứng? khối lượng bằng bao nhiêu?
b. Tính khối lượng KMnO4 đã bị nhiệt phân để thu được lượng O2 nói trên.
nAl=\(\dfrac{5,4}{27}\)=0,2mol
nO2=\(\dfrac{4,48}{22,4}\)=0,2mol
PTHH:
4Al + 3O2--to->2Al2O3
Tỉ lệ \(\dfrac{0,2}{4}\) <\(\dfrac{0,2}{3}\)->Al hết O2 dưtính theo Al
=>m O2=\(\dfrac{1}{60}\).32=\(\dfrac{8}{15}\)g
2KMnO4-to>K2MnO4+MnO2+O2
0,4--------------------------------------0,2
m KMnO4=0,4.158=63,2g
.
Cho 11g sắt tác dụng với 8,96 lít khí oxi ở điệu kiện tiêu chuẩn
a. Viết phương trình phản ứng xảy ra
b. Sau phản ứng chất nào còn dư? Khối lượng là bao nhiêu?
c. Tính khối lượng sản phẩm thu được
giải giúp em với ạ
a)
$4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3$
b)
$n_{Fe} = \dfrac{11,2}{56} = 0,2(mol) ; n_{O_2} = \dfrac{8,96}{22,4} = 0,4(mol)$
Ta thấy :
$n_{Fe} : 4 > n_{O_2} : 3$ nên $O_2$ dư
$n_{O_2\ pư} = = \dfrac{3}{4}n_{Fe} = 0,15(mol)$
$\Rightarrow m_{O_2\ dư} = (0,4 - 0,15).32 = 8(gam)$
c) $n_{Fe_2O_3} = \dfrac{1}{2}n_{Fe} = 0,1(mol)$
$m_{Fe_2O_3} = 0,1.160 = 16(gam)$
https://hoc24.vn/cau-hoi/cho-112g-fe-tac-dung-vs-896-lit-khi-oxi-dktc-a-viet-phuong-trinh-phan-ung-say-ra-b-sau-phan-ung-chat-nao-con-du-khoi-luong-bao-nhieu-c-tinh.7567611566487
bn tham khảo nhé