Dẫn từ từ 4,48 lít hỗn hợp khí etilen và propilen (đktc) vào dung dịch brom dư thấy khối lượng bình brom tăng 7,7 gam. Tính % thể tích của mỗi khí trong hỗn hợp ban đầu.

Những câu hỏi liên quan
Dẫn từ từ 3,36 lít hỗn hợp khí etilen và propilen(đktc) vào dung dich brom thấy dung dich bị nhạt màu và không có khí thoát ra .Khối lượng dung dịch sau phản ứng tăng 4,9 gam. Tính % theo thể tích của mỗi khí trong hỗn hợp ban đầu.?
\(n_{C_2H_4} = a\ mol;n_{C_3H_6} = b\ mol\\ \Rightarrow a + b = \dfrac{3,36}{22,4} = 0,15(1)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ C_3H_6 + Br_2 \to C_3H_6Br_2\\ m_{tăng} = 28a + 42b = 4,9(2)\\ (1)(2)\Rightarrow a = 0,1; b = 0,05\\ \%V_{C_2H_4} = \dfrac{0,1}{0,15}.100\% = 66,67\%\\ \%V_{C_3H_6} = 100\% -66,67\% = 33,33\%\)
Đúng 2
Bình luận (0)
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,90gam.
Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
Gọi số mol của etilen và propilen lần lượt là x và y mol.
Khối lượng dung dịch sau phản ứng tăng lên chính là khối lượng của hỗn hợp etilen và propilen.
Ta có hệ phương trình:
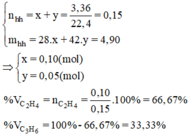
Đúng 1
Bình luận (0)
Câu 1: Dẫn từ từ 4,48 lít hỗn hợp khí etilen và metan (đktc) vào dung dịch brom dư thấy có 24 gam brom phản ứng.
a. Viết PTPU.
b. Tính thể tích của mỗi khí trong hỗn hợp ban đầu lần lượt là (C=12, H=1, Br=80)
C2H4+Br2->C2H4Br2
0,15--0,15 mol
n Br2=\(\dfrac{24}{160}\)=0,15 mol
=>VC2H4=0,15.22,4=3,36l
=>VCH4=4,48-3,36=1,12l
Đúng 1
Bình luận (0)
Dẫn 1,68 lít khí ( ở đktc) gồm hỗn hợp khí metan và khí etilen vào một bình chứa dung dịch Brom thấy dung dịch nhạt màu và khối lượng dung dịch tăng 0,7. Thể tích mỗi khi
trong hỗn hợp ban đầu (ở đktc) là:
Xem chi tiết
Ta có :
\(C_2H_4 + Br_2 \to C_2H_4Br_2 \\m_{C_2H_4} = m_{tăng} = 0,7(gam)\\ \Rightarrow V_{C_2H_4} = \dfrac{0,7}{28}.22,4 = 0,56(lít)\\ \Rightarrow V_{CH_4 } = 1,68 - 0,56 = 1,12(lít)\)
Đúng 1
Bình luận (0)
Bài 4. Hỗn hợp A gồm 4,48 lít hỗn hợp hai khí metan và axetilen ở đktc. Dẫn A vào dung dịch brom dư thấy bình brôm tăng thêm 1,3 gam. Tính % về thể tích của mỗi khí trong hỗn hợp?
\(m_{tăng}=m_{C_2H_2}=1,3\left(g\right)\\ \Rightarrow n_{C_2H_2}=\dfrac{1,3}{26}=0,05\left(mol\right)\\ \Rightarrow\%V_{\dfrac{C_2H_2}{A}}=\dfrac{0,05.22,4}{4,48}.100=25\%\\ \Rightarrow\%V_{\dfrac{CH_4}{A}}=100\%-25\%=75\%\)
Đúng 2
Bình luận (0)
Hỗn hợp khí A gồm etilen và metan, có thể tích bằng 5,6 lít (ở đktc). Dẫn toàn bộ A vào dung dịch brom dư thấy khối lượng của bình dung dịch brom tăng 4,2 gam và còn V lít khí thoát ra. Giá trị của V là
A. 2,24.
B. 1,12.
C. 4,48.
D. 3,36.
p/s: mọi người giải thích giúp mình được không ạ^^
Xem thêm câu trả lời
Dẫn 6.72 lít ( ở đktc ) hỗn hợp khí gồm metan và etilen vào bình đựng dung dịch brom dư sau khi phản ứng xảy ra hoàn toàn thấy có 32 gam brom đã tham gia phản ứng a) tính % thể tích các khí trong hỗn hợp ban đầu b) tính khối lượng rượu etylic thu được khí trong lượng etilen trong hỗn hợp trên tác dụng với nước xúc tác axit , nhiệt độ thích hợp . Biết hiệu suất phản ứng đạt 80%
Dẫn từ từ 4,48 lít hỗn hợp khí etilen và etan (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và 1,12 lít khí thoát ra. Khối lượng dung dịch brom sau phản ứng m gam. Tính m?
\(V_{C_2H_6} = 1,12\ lít \Rightarrow n_{C_2H_4} = \dfrac{4,48-1,12}{22,4} = 0,15(mol)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ m_{tăng}= m_{C_2H_4} = 0,15.28 = 4,2\ gam\)
Đúng 2
Bình luận (0)
Dẫn 7,84 lít hỗn hợp khí etilen và metan(đktc) qua dd Brom dư ,thấy khối lượng tăng lên 4,2 gam . Tính thành phần % thể tích mỗi khí trong hỗn hợp đầu.
\(n_{hhkhí\left(C_2H_4,CH_4\right)}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(m_{tăng}=m_{C_2H_4}=4,2\left(g\right)\\ n_{C_2H_4}=\dfrac{4,2}{28}=0,15\left(mol\right)\\ \%V_{C_2H_4}=\dfrac{0,15}{0,35}=42,85\%\\ \%V_{CH_4}=100\%-42,85\%=57,15\%\)
Đúng 3
Bình luận (0)





















