Cho FeO tác dụng hoàn toàn với hidro ở nhiệt độ cao thu được 8,4 g chất rắn. Tính khối lượng FeO cần dùng.
A.10,8 g
B.21,6 g
C.9,15 g
D. 18,3 g
Giúp mình với(giải chi tiết càng tốt)
Cho 4,48 lít khí CO (đktc) tác dụng với FeO ở nhiệt độ cao. Sau phản ứng thu được chất rắn A có khối lượng nhỏ hơn 1,6g so với lượng FeO ban đầu. Tính khối lượng Fe thu được và % V các chất (cùng trạng thái) sau phản ứng?
$FeO + CO \xrightarrow{t^o} Fe + CO_2$
Theo PTHH : $n_{FeO} = n_{CO\ pư} = n_{Fe} = n_{CO_2} = a(mol)$
$\Rightarrow m_{giảm} = m_{FeO} - m_{Fe} = 72a -56a = 16a = 1,6(gam)$
$\Rightarrow a = 0,1(mol)$
$m_{Fe} = 0,1.56 = 5,6(gam)$
$n_{CO\ dư} = 0,2 - 0,1 = 0,1(mol)$
$\%V_{CO\ dư} = \%V_{CO_2} = \dfrac{0,1}{0,1 + 0,1}.100\% = 50\%$
Để tác dụng hoàn toàn với 4,64 g hỗn hợp FeO, Fe2O3, Fe3O4 cần dùng vừa đủ 160 ml dung dịch HCl 1M. Nếu khử hoàn toàn 4,64 g hỗn hợp trên bằng CO ở nhiệt độ cao thì khối lượng Fe thu được là
A. 3,36 g.
B. 4,36 g.
C. 3,63 g.
D. 4,63 g.
Chọn A
Ta có n O o x i t = 1 2 n a x i t = 1 2 . 0 , 16 . 1 = 0 , 08
m F e = m h h – m o ( o x i t ) = 4,64 – 0,08.16 = 3,36 gam.
Trộn 21,6 gam bột Al với m gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 thu được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến phản ứng xảy ra hoàn toàn thu được chất rắn Z. Cho Z tác dụng với dung dịch NaOH dư thu được 6,72 lít H2 ở đktc. Mặt khác, nếu cho Z tác dụng với dung dịch HNO3 loãng dư thu được 19,04 lít NO là sản phẩm khử duy nhất ở đktc. Giá trị của m là
A. 50,8.
B. 46,0.
C. 58,6.
D. 62,0.
Chọn A.
Rắn Z chứa Al dư (x mol), Al2O3 (y mol) và Fe với x = 2 3 n H 2 = 0 , 2 m o l → B T : A l y = 0 , 3
Khi cho Z tác dụng với HNO3 thì:
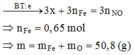
Trộn 21,6 gam bột Al với m gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 thu được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến phản ứng xảy ra hoàn toàn thu được chất rắn Z. Cho Z tác dụng với dung dịch NaOH dư thu được 6,72 lít H2 ở đktc. Mặt khác, nếu cho Z tác dụng với dung dịch HNO3 loãng dư thu được 19,04 lít NO là sản phẩm khử duy nhất ở đktc. Giá trị của m là
A. 50,8
B. 46,0
C. 58,6
D. 62,0
Trộn 21,6 gam bột Al với m gam hỗn hợp X gồm FeO , Fe 2 O 3 và Fe 3 O 4 được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến phản ứng hoàn toàn thu được chất rắn Z. Cho Z tác dụng vớii dung dịch NaOH dư thu được 6,72 lít khí. Nếu cho Z tác dụng với HNO 3 , loãng dư thì thu được 19,04 lít khí NO là sản phẩm khử duy nhất. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 50,8
B. 46,0
C. 58,6
D. 62,0
Cho 4,72 gam hỗn hợp bột gồm các chất Fe, FeO và Fe2O3 tác dụng với CO ở nhiệt độ cao. Phản ứng xong thu được 3,92 gam Fe. Nếu ngâm cùng lượng hỗn hợp các chất trên trong dung dịch CuSO4 dư, phản ứng xong khối lượng chất rắn thu được là 4,96 gam. Khối lượng (gam) Fe, Fe2O3 và FeO trong hỗn hợp ban đầu lần lượt là
A. 1,68; 1,44; 1,6
B. 1,6; 1,54; 1,64
C. 1,6; 1,44; 1,64
D. 1,68; 1,6; 1,44
Đáp án D
Các phản ứng xảy ra:
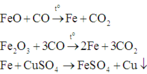
Hỗn hợp rắn thu được khi cho hỗn hợp phản ứng với dung dịch CuSO4 gồm Cu, FeO và Fe2O3.
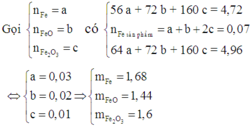
Khử hoàn toàn Sắt(III)Oxit bằng khí Hidro ở nhiệt độ cao thu được kim loại và 10,8 g nước.
a. Tính thể tích khí Hidro cần dùng ở Đktc?
b. Tính khối lượng kim loại sau phản ứng?
Tính khối lượng Sắt(III)Oxit cần dùng?
Fe2O3+3H2-to>2Fe+3H2O
0,2----------0,6------0,4-----0,6 mol
n H2O=\(\dfrac{10,8}{18}\)=0,6 mol
=>VH2=0,6.22,4=13,44l
b)m Fe=0,4.56=22,4g
c) m Fe2O3=0,2.160=32g
Trộn 21,6 gam bột Al với m gam hỗn hợp X (gồm FeO, Fe2O3 và Fe3O4) được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp chất rắn Z. Cho Z tác dụng với dung dịch NaOH dư thu được 6,72 lít khí. Nếu cho Z tác dụng với dung dịch HNO3 loãng, dư thì thu được 19,04 lít NO (sản phẩm khử duy nhất). Biết các thể tích đo ở đktc. Giá trị của m là:
A. 58,6
B. 50,8
C. 46,0
D. 62,0
cho 2,3 gam natri tác dụng hoàn toàn với nước thu được V lít khí hiđro ở đktc.
a)Viết phơng trình hóa học của phản ứng.
b) Tính giá trị của V.
c) Lấy toàn bộ lượng khí H2 thu được ở trên tác dụng với 2,4 gam CuO ở nhiệt độ cao. Tính khối lượng chất rắn thu được sau phản ứng.
a) $2Na + 2H_2O \to 2NaOH + H_2$
b) $n_{Na} = \dfrac{2,3}{23} = 0,1(mol)$
Theo PTHH :
$n_{H_2} = \dfrac{1}{2}n_{Na} = 0,05(mol)$
$V_{H_2} = 0,05.22,4 = 1,12(lít)$
c) $n_{CuO} = \dfrac{2,4}{80} = 0,03(mol)$
$CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
Ta thấy :
$n_{CuO} : 1 < n_{H_2} : 1$ nên $H_2$ dư
$n_{Cu} = n_{CuO} = 0,03(mol)$
$m_{Cu} = 0,03.64 = 1,92(gam)$