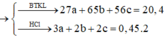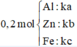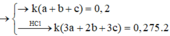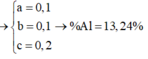Bài 22: Cho a gam hỗn hợp X gồm Fe và Al tác dụng hoàn toàn với dung dịch HCl dư thì thu được 11,2 lit khí ở đktc. Mặt khác, cho a gam hỗn hợp X gồm Fe và Al tác dụng vừa đủ với 13,44 lít khí Cl2 ở đktc. Tính a=?

Những câu hỏi liên quan
Bài 23: Cho 23,8 gam hỗn hợp X gồm Mg, Fe và Al tác dụng hoàn toàn với dung dịch HCl dư thì thu được 17,92 lit khí ở đktc. Mặt khác, cho 23,8 gam hỗn hợp X tác dụng vừa đủ với 20,16 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?
Gọi số mol Mg, Fe, Al là a, b, c
=> 24a + 56b + 27c = 23,8
PTHH: Mg + 2HCl --> MgCl2 + H2
a------------------------->a
Fe + 2HCl --> FeCl2 + H2
b------------------------->b
2Al + 6HCl --> 2AlCl3 + 3H2
c------------------------->1,5c
=> a + b + 1,5c = \(\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
a-->a
2Fe + 3Cl2 --to--> 2FeCl3
b--->1,5b
2Al + 3Cl2 --to--> 2AlCl3
c--->1,5c
=> \(a+1,5b+1,5c=\dfrac{20,16}{22,4}=0,9\left(mol\right)\)
=> a = 0,3; b = 0,2; c = 0,2
=> \(\left\{{}\begin{matrix}m_{Mg}=0,3.24=7,2\left(g\right)\\m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Bài 7: Cho 10,65 gam hỗn hợp X gồm Zn, Fe và Al tác dụng hoàn toàn với 200 gam dung dịch HCl a% vừa đủ thì thu được 10,08 lit khí ở đktc. Mặt khác, cho 10,65 gam hỗn hợp X tác dụng vừa đủ với 5,6 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.b. Tính a?c. Tính C% các chất trong dung dịch thu được sau phản ứng.
Đọc tiếp
Bài 7: Cho 10,65 gam hỗn hợp X gồm Zn, Fe và Al tác dụng hoàn toàn với 200 gam dung dịch HCl a% vừa đủ thì thu được 10,08 lit khí ở đktc. Mặt khác, cho 10,65 gam hỗn hợp X tác dụng vừa đủ với 5,6 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?
a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.
b. Tính a=?
c. Tính C% các chất trong dung dịch thu được sau phản ứng.
Cho 10,65 gam hỗn hợp X gồm Zn, Fe và Al tác dụng hoàn toàn với 200 gam dung dịch HCl a% vừa đủ thì thu được 5,04 lit khí ở đktc. Mặt khác, cho 10,65 gam hỗn hợp X tác dụng vừa đủ với 5,6 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.b. Tính a?c. Tính C% các chất trong dung dịch thu được sau phản ứng.
Đọc tiếp
Cho 10,65 gam hỗn hợp X gồm Zn, Fe và Al tác dụng hoàn toàn với 200 gam dung dịch HCl a% vừa đủ thì thu được 5,04 lit khí ở đktc. Mặt khác, cho 10,65 gam hỗn hợp X tác dụng vừa đủ với 5,6 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?
a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.
b. Tính a=?
c. Tính C% các chất trong dung dịch thu được sau phản ứng.
Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Al}=c\left(mol\right)\end{matrix}\right.\) => 65a + 56b + 27c = 10,65 (1)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Fe + 2HCl --> FeCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
=> \(n_{H_2}=a+b+1,5c=\dfrac{5,04}{22,4}=0,225\left(mol\right)\) (2)
PTHH: Zn + Cl2 --to--> ZnCl2
2Fe + 3Cl2 --to--> 2FeCl3
2Al + 3Cl2 --to--> 2AlCl3
=> \(n_{Cl_2}=a+1,5b+1,5c=\dfrac{5,6}{22,4}=0,25\left(mol\right)\) (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,05\left(mol\right)\\c=0,05\left(mol\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}m_{Zn}=0,1.65=6,5\left(g\right)\\m_{Fe}=0,05.56=2,8\left(g\right)\\m_{Al}=0,05.27=1,35\left(g\right)\end{matrix}\right.\)
a) \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{6,5}{10,65}.100\%=61,033\%\\\%m_{Fe}=\dfrac{2,8}{10,65}.100\%=26,291\%\\\%m_{Al}=\dfrac{1,35}{10,65}.100\%=12,676\%\end{matrix}\right.\)
b) nHCl = 2a + 2b + 3c = 0,45 (mol)
=> mHCl = 0,45.36,5 = 16,425 (g)
=> \(a\%=C\%=\dfrac{16,425}{200}.100\%=8,2125\%\)
c) mdd sau pư = 10,65 + 200 - 0,225.2 = 210,2 (g)
=> \(\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{0,1.136}{210,2}.100\%=6,47\%\\C\%_{FeCl_2}=\dfrac{0,05.127}{210,2}.100\%=3,02\%\\C\%_{AlCl_3}=\dfrac{0,05.133,5}{210,2}.100\%=3,176\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 9,52 gam hỗn hợp X gồm Mg, Fe và Al tác dụng hoàn toàn với 200 ml dung dịch HCl aM vừa đủ thì thu được 14,336 lit khí ở đktc. Mặt khác, cho 9,52 gam hỗn hợp X tác dụng vừa đủ với 8,064 lít khí Cl2 ở đktc.
a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.
b. Tính a=?
c. Tính CM các chất trong dung dịch thu được sau phản ứng.
Sửa: $V_{H_2}=7,168(l)$
$a\bigg)$
Đặt $n_{Mg}=x;n_{Fe}=y;n_{Al}=z$
$\to 24x+56y+27z=9,52(1)$
$n_{H_2}=\dfrac{7,168}{22,4}=0,32(mol)$
$n_{Cl_2}=\dfrac{8,064}{22,4}=0,36(mol)$
BTe: $x+y+1,5z=n_{H_2}=0,32(2)$
BTe: $x+1,5y+1,5z=n_{Cl_2}=0,36(3)$
Từ $(1)(2)(3)\to x=0,12(mol);y=0,08(mol);z=0,08(mol)$
$\to \begin{cases} \%m_{Mg}=\dfrac{0,12.24}{9,52}.100\%=30,25\%\\ \%m_{Fe}=\dfrac{0,08.56}{9,52}.100\%=47,06\%\\ \%m_{Al}=100-47,06-30,25=22,69\% \end{cases}$
$b\bigg)$
Bảo toàn H: $n_{HCl}=2n_{H_2}=0,64(mol)$
$\to C_{M_{HCl}}=\dfrac{0,64}{0,2}=3,2M$
$\to a=3,2$
$c\bigg)$
Dung dịch sau gồm $MgCl_2,FeCl_2,AlCl_3$
Bảo toàn $Mg,Al,Fe:n_{MgCl_2}=0,12(mol);n_{AlCl_3}=n_{FeCl_2}=0,08(mol)$
$\to C_{M_{MgCl_2}}=\dfrac{0,12}{0,2}=0,6M$
$\to C_{M_{AlCl_3}}=C_{M_{FeCl_2}}=\dfrac{0,08}{0,2}=0,4M$
Đúng 2
Bình luận (0)
$a\bigg)$
Đặt $n_{Mg}=x;n_{Fe}=y;n_{Al}=z$
$\to 24x+56y+27z=9,52(1)$
$n_{H_2}=\dfrac{14,336}{22,4}=0,64(mol)$
$n_{Cl_2}=\dfrac{8,064}{22,4}=0,36(mol)$
BTe: $x+y+1,5z=n_{H_2}=0,64(2)$
BTe: $x+1,5y+1,5z=n_{Cl_2}=0,36(3)$
Từ $(1)(2)(3)\to$ nghiệm âm, xem lại đề
Đúng 0
Bình luận (3)
Cho 9,52 gam hỗn hợp X gồm Mg, Fe và Al tác dụng hoàn toàn với 200 ml dung dịch HCl aM vừa đủ thì thu được 14,336 lit khí ở đktc. Mặt khác, cho 9,52 gam hỗn hợp X tác dụng vừa đủ với 8,064 lít khí Cl2 ở đktc.
a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.
b. Tính a=?
c. Tính CM các chất trong dung dịch thu được sau phản ứng.
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Phần trăm của Al trong hỗn hợp A là (biết các khí đo ở đktc) A. 26,47%. B. 19,85%. C. 33,09%. D. 13,24%.
Đọc tiếp
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Phần trăm của Al trong hỗn hợp A là (biết các khí đo ở đktc)
A. 26,47%.
B. 19,85%.
C. 33,09%.
D. 13,24%.
Đáp án D
Xét trường hợp 20,4 gam A tác dụng với dung dịch HCl dư:
Gọi số mol các chất là Al: a mol; Zn: b mol; Fe: c mol
Ta có:

Các quá trình nhường, nhận electron:
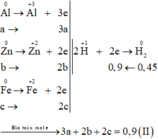
Xét trường hợp 0,2 mol A tác dụng với Cl2:
Gọi số mol các chất là Al: ka mol; Zn: kb mol; Fe: kc mol
Ta có:
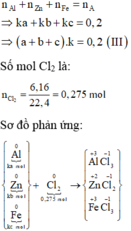
Các quá trình nhường, nhận electron:
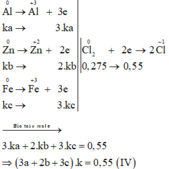
Lấy (IV) chia (III) vế với vế ta được:

Đúng 0
Bình luận (0)
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Tính thành phần phần % về khối lượng của Al trong hỗn hợp A (biết khí đo được ở đktc) A.26,47% B. 19,85% C.33,09% D.13,24%
Đọc tiếp
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Tính thành phần phần % về khối lượng của Al trong hỗn hợp A (biết khí đo được ở đktc)
A.26,47%
B. 19,85%
C.33,09%
D.13,24%
Hỗn hợp X gồm Mg, Al và Fe. Cho 14,7 gam hỗn hợp X tác dụng hoàn toàn với dung dịch NaOH, sinh ra 3,36 lít khí (ở dktc). Mặt khác, nếu cho 14,7 gam X tác dụng hoàn toàn với dung dịch HCl, thu được 10,08 lít khí (ở đktc)a) Tinh số mol mỗi kim loại trong 14,7 gam hỗn hợp X.b) Nếu cho m gam hỗn hợp X tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (duy nhất, ở dktc). Viết các phương trình phản ứng...
Đọc tiếp
Hỗn hợp X gồm Mg, Al và Fe. Cho 14,7 gam hỗn hợp X tác dụng hoàn toàn với dung dịch NaOH, sinh ra 3,36 lít khí (ở dktc). Mặt khác, nếu cho 14,7 gam X tác dụng hoàn toàn với dung dịch HCl, thu được 10,08 lít khí (ở đktc)
a) Tinh số mol mỗi kim loại trong 14,7 gam hỗn hợp X.
b) Nếu cho m gam hỗn hợp X tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (duy nhất, ở dktc). Viết các phương trình phản ứng và tính giá trị của m
Để tác dụng hết với 35,7 gam hỗn hợp X gồm Cu, Fe, Al ở dạng bột, nung nóng cần vừa đủ 21,84 lít khí Cl2. Mặt khác, khi cho 0,25 mol hỗn hợp X tác dụng với dung dịch HCl dư thì thu được 4,48 lít khí H2. Tính % khối lượng mỗi kim loại trong hỗn hợp X. Biết thể tích các khí đó ở đktc.
\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right),n_{Al}=c\left(mol\right)\)
\(m_X=64a+56b+27b=35.7\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{21.84}{22.4}=0.975\left(mol\right)\)
\(Cu+Cl_2\underrightarrow{^{^{t^0}}}CuCl_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(Al+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}AlCl_3\)
\(n_{Cl_2}=a+1.5b+1.5c=0.975\left(mol\right)\left(2\right)\)
\(n_{hh}=ka+kb+kc=0.25\left(mol\right)\)
\(n_{H_2}=kb+k\cdot1.5c=0.2\left(mol\right)\)
\(\Leftrightarrow a-0.25b-0.875c=0\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=0.3,b=0.15,c=0.3\)
\(\%Cu=\dfrac{0.3\cdot64}{35.7}\cdot100\%=53.78\%\)
\(\%Fe=\dfrac{0.15\cdot56}{35.7}\cdot100\%=23.52\%\)
\(\text{%Al=22.7%}\)
Đúng 1
Bình luận (0)