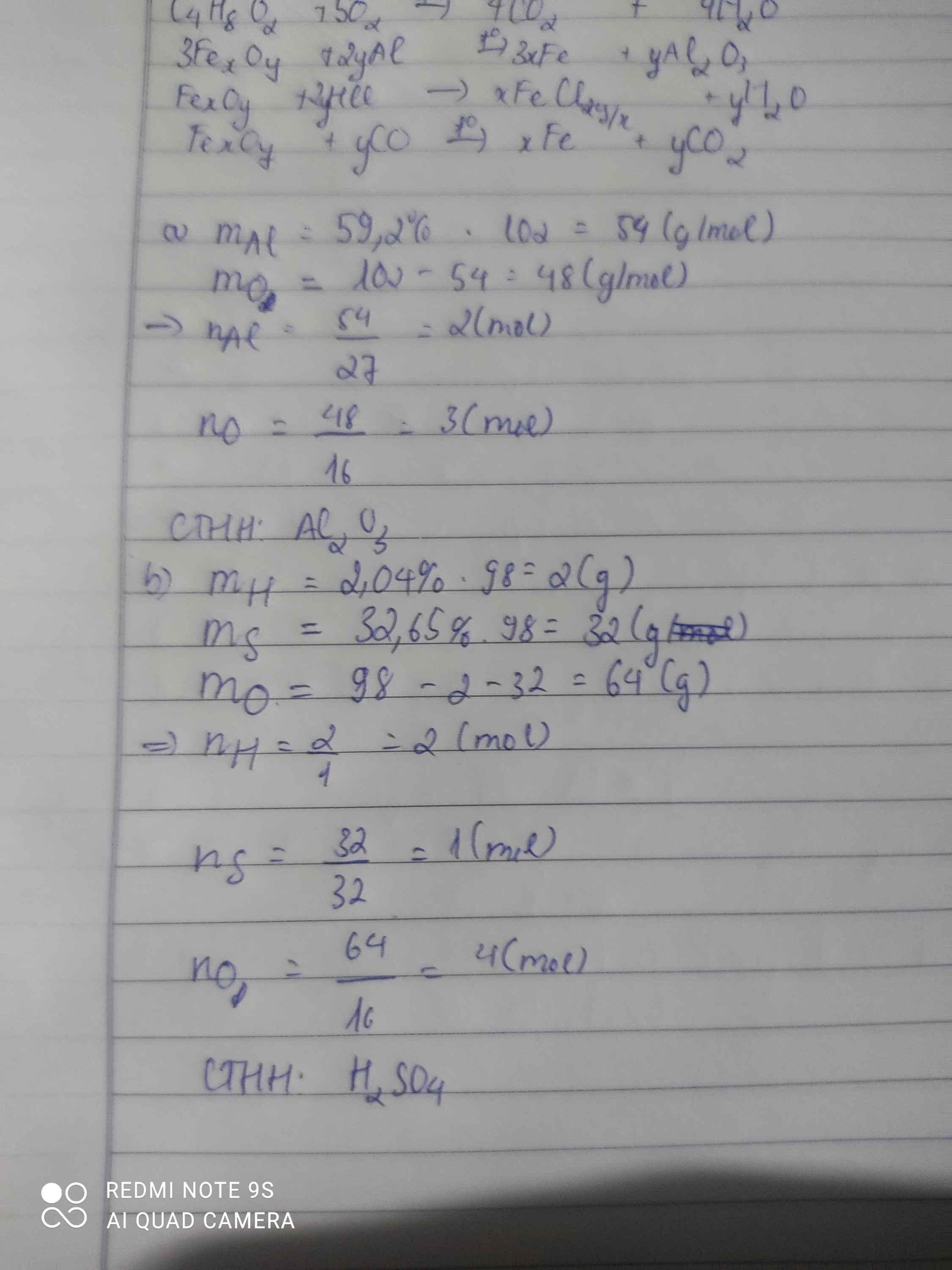B là oxit của một kim loại R chưa rõ hoá trị với Oxi. Biết thành phần % về khối lượng của oxi trong hợp chất bằng 3/7 thành phần % về khối lượng của R trong hợp chất đó. Xác định công thức hóa học của B?

Những câu hỏi liên quan
B là oxit của kim loại r chưa rõ hóa trị biết thành phần trăm về khối lượng của R trong hợp chất đó
Bài 3: Hợp chất tạo bởi kim loại R hoá trị III với oxi. Tìm tên kim loại R và công thức hóa học của hợp chất Biết trong hợp chất đó nguyên tố R kết hợp với oxi theo tỉ lệ khối lượng là 7:3.
\(CTHH:R_2O_3\\ \Rightarrow\dfrac{m_R}{m_O}=\dfrac{M_R.2}{16.3}=\dfrac{7}{3}\\ \Rightarrow\dfrac{M_R}{24}=\dfrac{7}{3}\Rightarrow M_R=56\left(g/mol\right)\)
Vậy R là \(Fe\) và \(CTHH:Fe_2O_3\)
Đúng 2
Bình luận (0)
Bài 3: Hợp chất tạo bởi kim loại R hoá trị III với oxi. Tìm tên kim loại R và công thức hóa học của hợp chất Biết trong hợp chất đó nguyên tố R kết hợp với oxi theo tỉ lệ khối lượng là 7:3.
1. Một hợp chất của nguyên tố R (hóa trị IV) với oxi có phần trăm khối lượng của nguyên tố R là 50%. Xác định nguyên tố R và công thức hóa học của hợp chất?2. Xác định công thức hóa học của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4? Biết rằng M chiếm 20% khối lượng của phân tử?3. Hợp chất A ở thể khí có %mC 75% và còn lại là H. Xác định CTHH của A? Biết tỉ khối của khí A với khí oxi là 0,54. Hợp chất B tạo bởi hidro và nhóm nguyên tử ( XOy) hóa trị III. Biết rằng phân tử B nặng bằng p...
Đọc tiếp
1. Một hợp chất của nguyên tố R (hóa trị IV) với oxi có phần trăm khối lượng của nguyên tố R là 50%. Xác định nguyên tố R và công thức hóa học của hợp chất?
2. Xác định công thức hóa học của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4? Biết rằng M chiếm 20% khối lượng của phân tử?
3. Hợp chất A ở thể khí có %mC = 75% và còn lại là H. Xác định CTHH của A? Biết tỉ khối của khí A với khí oxi là 0,5
4. Hợp chất B tạo bởi hidro và nhóm nguyên tử ( XOy) hóa trị III. Biết rằng phân tử B nặng bằng phân tử H2SO4 và nguyên tố oxi chiếm 65,31% về khối lượng của B.
a. Xác định chỉ số y và nguyên tử khối của nguyên tố X?
b. Cho biết tên, kí hiệu hóa học của X và công thức hóa học của B?
1. CT của hợp chất : RO2 (do R hóa trị IV)
Ta có : \(\%R=\dfrac{R}{R+16.2}.100=50\)
=> R=32
Vậy R là lưu huỳnh (S), CTHH của hợp chất : SO2
Đúng 2
Bình luận (1)
2. CTHH của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4 là MSO4 (do M hóa trị II)
Ta có : \(\%M=\dfrac{M}{M+96}.100=20\)
=>M=24
Vây M là Magie (Mg), CTHH của hợp chất MgSO4
Đúng 2
Bình luận (0)
3. Đặt CTHH của A là CxHy
\(M_A=0,5M_{O_2}=16\left(đvC\right)\)
Ta có : \(\%C=\dfrac{12x}{16}.100=75\Rightarrow x=1\)
Mặc khác : 12x + y = 16
=> y=4
Vậy CTHH của A là CH4
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
B là oxit của 1 kim loại R chưa rõ hóa trị.biết thành phần % về khối lượng của oxi trong hợp chất bằng \(\frac{3}{7}\)thành phần % về khối lượng của R trong hợp chất đó.xác định công thức hóa học của B
https://i.imgur.com/qiO6jVN.jpg
1) Một hợp chất chứa 59,2 % Al về khối lượng, còn lại là oxi. Xác định công thức hóa học của hợp chất biết khối lượng mol của hợp chất là 102 g/mol.
2) Xác định công thức hóa học của hợp chất A. Biết thành phần phần trăm về khối lượng các nguyên tố: 2,04% H, 32,65% S, còn lại là oxi, MA = 98 g/mol.
Bài 2:
\(Đặt.CTTQ.của.A:H_xS_yO_z\left(x,y,z:nguyên,dương\right)\\ Ta.có:\left\{{}\begin{matrix}x=\dfrac{98.2,04\%}{1}=2\\y=\dfrac{98.32,65\%}{32}=1\\z=\dfrac{98.\left(100\%-2,04\%-32,65\%\right)}{16}=4\end{matrix}\right.\\ \Rightarrow x=2;y=1;z=4\\ \Rightarrow CTHH:H_2SO_4\)
Đúng 4
Bình luận (1)
Bài 1: Sửa đề 59,2% Al thành 52,9% Al
\(Đặt.CTTQ:Al_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{52,9\%.102}{27}\approx2\\ \Rightarrow y\approx\dfrac{\left(100\%-52,9\%\right).102}{16}\approx3\\ \Rightarrow CTHH:Al_2O_3\)
Đúng 4
Bình luận (0)
1) \(m_{Al}=102.\dfrac{59,2}{100}=60,384\) (g)
\(m_O=102.\dfrac{100-59,2}{100}=41,616\) (g).
\(n_{Al}=\dfrac{m}{M}=\dfrac{60,384}{27}\approx2\) (mol).
\(n_O=\dfrac{m}{M}=\dfrac{41,616}{16}\approx3\) (mol).
-Công thức hóa học của hợp chất: \(Al_2O_3\).
2) \(m_H=98.\dfrac{2,04}{100}=1,9992\) (g).
\(m_S=98.\dfrac{32,65}{100}=31,997\) (g).
\(m_O=98.\dfrac{100-2,04-32,65}{100}=64,0038\) (g).
\(n_H=\dfrac{m}{M}=\dfrac{1,9992}{1}\approx2\) (mol).
\(n_S=\dfrac{m}{M}=\dfrac{31,997}{32}\approx1\) (mol).
\(n_O=\dfrac{m}{M}=\dfrac{64,0038}{16}\approx4\) (mol).
-Cộng thức hóa học của hợp chất A: \(H_2SO_4\)
Đúng 1
Bình luận (3)
a) Một hợp chất chứa 59,2 % Al về khối lượng, còn lại là oxi. Xác định công thức hóa học của hợp chất biết khối lượng mol của hợp chất là 102 g/mol.
b) Xác định công thức hóa học của hợp chất A. Biết thành phần phần trăm về khối lượng các nguyên tố: 2,04% H, 32,65% S, còn lại là oxi, MA = 98 g/mol.
B là 1 oxít của kim loại R chưa rõ hóa trị biết thành phần % về khối lượng của oxi có trong hợp chất bằng 7/3 thành phần % về khối lượng của R trong hợp chất đó xác định công thức hóa học của B
Gọi CTHH oxit kim loại R là R2Ox ( Hóa trị của R: x , )
Viết tắt: R = MR nhé!
Ta có: %mO = \(\frac{16x}{2R+16x}.100\%\)
%mR = \(\frac{2R}{2R+16x}.100\%\)
Theo đề ra, ta có: %mO = \(\frac{7}{3}\%m_R\)
\(\Rightarrow\frac{16x}{2R+16x}=\frac{7}{3}\times\frac{2R}{2R+16x}\)
\(\Rightarrow R=\frac{56}{3}x\)
Xét thấy chỉ có x = 3 là phù hợp
=> R = 56
=> R là Fe
=> CTHH của B: Fe2O3
Đúng 0
Bình luận (5)
- Giả sử : %mR = a% %mO = 3/7a%
- Gọi hoá trị của R là n -> CTTQ của B là: R2On
- Ta có: 2 : n = (a%/Mr): ( 3/7a%?16) => Mr =112n/6
- Vì n là hóa trị của nguyên tố nên n phải nguyên dương, ta có:
|
n |
I |
II |
III |
IV |
|
Mr |
18,6 |
37,3 |
56 |
76,4 |
|
|
loại |
loại |
chọn |
loại |
=> R là kim loại có hóa trị III, NTK=56 => R là Fe
- Vậy công thức hóa học của B là Fe2O3.
Đúng 0
Bình luận (0)
Một hợp chất oxit của sắt có thành phần về khối lượng nguyên tố sắt so với oxi là 7:3. Vậy hợp chất đó có công thức hoá học là: A.
F
e
2
O
3
B. FeO C.
F
e
3
O
4
D.
F
e
O
H
2
Đọc tiếp
Một hợp chất oxit của sắt có thành phần về khối lượng nguyên tố sắt so với oxi là 7:3. Vậy hợp chất đó có công thức hoá học là:
A. F e 2 O 3
B. FeO
C. F e 3 O 4
D. F e O H 2
Gọi công thức oxit sắt cần tìm là F e X O Y
Theo bài ta có: : = 7 : 3
Ta coi m F e = 7 gam; m O = 3 gam.
Khi đó:
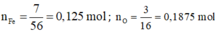
⇒ m C a O H 2 = 2.(40+17.2) = 148kg
⇒ n F e : n O = x : y = 0,125 : 0,1875 = 2 : 3
Vậy oxit sắt cần tìm là F e 2 O 3
⇒ Chọn A.
Đúng 0
Bình luận (0)