
Những câu hỏi liên quan
Cho 13 g hỗn hợp bột các kim loại magie, nhôm và đồng tác dụng với dung dịch HCl 2M dư. Phản ứng xong thu được 10,08 lít khí bay ra ở (đktc) và 4 g chất rắn không tan. a/ Tính thành phần % khối lượng mỗi kim loại có trong hỗn hợp. b/ Để trung hòa lượng axit HCl 2M dư người ta dùng dung dịch NaOH vừa đủ. Hãy tính thể tích dung dịch HCl 2M đã dùng.
Chất rắn ko tan là Cu
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=13-4=9(1)\)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,45(2)\\ (1)(2)\Rightarrow x=0,15(mol);y=0,2(mol)\\ a,\%_{Cu}=\dfrac{4}{13}.100\%=30,77\%\\ \%_{Mg}=\dfrac{0,15.24}{13}.100\%=27,69\%\\ \%_{Al}=100\%-30,77\%-27,69\%=41,54\%\\ b,\Sigma n_{HCl}=2x+3y=0,9(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,9}{2}=0,45(l)\)
Đúng 2
Bình luận (1)
Hòa tan 5,2g hỗn hợp gồm Mg và Fe bằng dung dịch axit HCl thì thu được 6,72l \(H_2\) (đ.k.t.c). Sau phản ứng thấy còn 6,25g một chất rắn không tan. Tính thành phần phần trăm về khối lượng mỗi kim loại trong hỗn hợp
Hòa tan 25g hỗn hợp gồm Ag, Zn, Mg vào 800ml HCl 2M dư. Sau phản ứng thu được 6,5g chất rắn không tan. Lượng axit dư có thể hòa tan được 16g CuO. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu .
Hòa tan hỗn hợp vào HCl dư
=> chết rắn ko tan là Ag => mAg = 6,25 g
Lượng axit dư có thể hòa tan được = 16 g CuO
\(n_{CuO}=\dfrac{m}{M}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH ( hòa tan axit dư )
2HCl + CuO ---> CuCl2 + H2O
..0,4......0,2............0,2.......0,2...(mol)
\(\sum n_{HCl}=2\cdot0,8=1,6\left(mol\right)\)
=> nHCl phản ứng với hỗn hợp = 1,6 - 0,4 = 1,2 (mol)
gọi x , y lần lượt là số mol của Mg và Zn
PTHH
Mg + 2HCl ----> MgCl2 + H2
x.........2x.............x.........x..(mol)
Zn + 2HCl ---> ZnCl2 + H2
y........2y.............y............y..(mo
Ta có hệ PT
\(\left\{{}\begin{matrix}24x+65y=25-6,5\\2x+2y=1,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,5\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=n\cdot M=0,5\cdot24=12\left(g\right)\)
\(\Rightarrow m_{Zn}=n\cdot M=0,1\cdot65=6,5\left(g\right)\)
Đúng 0
Bình luận (1)
hòa tan 25 g hỗn hợp bạc kiễm và magie vào 800 cm3 dung dịch HCl 2M có dư. Sau phản ứng thu được 6,5 gam chất rắn không tan. Lượng axit dư có thể hòa tan được 16 gam đồng oxit. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Giúp hộ nha đang cần gấp lắm!!!
https://i.imgur.com/ZgHdtx7.jpg
Cho một lượng hỗn hợp gồm Zn và Cu tác dụng với lượng dư dung dịch axit HCL , thu được 4,48 lít khí H2 (đktc) . Sau phản ứng thấy còn 19,5 gam một chất rắn không tan. Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp.
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl -->ZnCl2 + H2
____0,2<----------------------0,2
=> mZn = 0,2.65 = 13 (g)
mCu = mrắn không tan = 19,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{13}{13+19,5}.100\%=40\%\\\%Cu=\dfrac{19,5}{13+19,5}.100\%=60\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
`n_(H_2)=4,48/22,4=0,2 (mol)`
Ta có PTHH: `Zn+2HCl --> ZnCl_2 +H_2`
Theo PT: `1`--------------------------------`1`
Theo đề: `0,2`------------------------------`0,2`
`m_(Zn)=0,2.65=13(g)`
Vì `Cu` không phản ứng với `HCl` nên `m_(chất rắn không tan)=m_(Cu)=19,5(gam)`
`%Zn=13/(13+19,5) .100%=40%`
`%Cu=100%-40%=60%`
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm Mg và Fe có khối lượng 8,64 gam được chia thành hai phần bằng nhau. Phần 1: Hòa tan hoàn toàn vào dung dịch HNO3 loãng, dư thoát ra 555ml hỗn hợp khí NO và NO2 đo ở 27,3° C và 2 atm và có tỉ khối hơi so với H2 bằng 18,8889. Phần 2: Đem hòa tan vào 400ml dung dịch chứa AgNO3 và Cu(NO3)2. Sau phản ứng thu được chất rắn gồm 3 kim loại có khối lượng 7,68g. Hòa tan chất rắn này trong dung dịch HCl dư thấy khối lượng chất rắn đã giảm đi 21,88%. Nồng độ của dung dịch AgNO3 và Cu(NO3)2 t...
Đọc tiếp
Cho hỗn hợp gồm Mg và Fe có khối lượng 8,64 gam được chia thành hai phần bằng nhau.
Phần 1: Hòa tan hoàn toàn vào dung dịch HNO3 loãng, dư thoát ra 555ml hỗn hợp khí NO và NO2 đo ở 27,3° C và 2 atm và có tỉ khối hơi so với H2 bằng 18,8889.
Phần 2: Đem hòa tan vào 400ml dung dịch chứa AgNO3 và Cu(NO3)2. Sau phản ứng thu được chất rắn gồm 3 kim loại có khối lượng 7,68g. Hòa tan chất rắn này trong dung dịch HCl dư thấy khối lượng chất rắn đã giảm đi 21,88%. Nồng độ của dung dịch AgNO3 và Cu(NO3)2 trong dung dịch lần lượt là
A.0,15M và 0,1M
B. 0,1M và 0,1M
C.0,05M và 0,15M
D. 0,125M và 0,215M
Đáp án C:
Gọi x, y là số mol Mg và Fe trong mỗi phần
=> 24x+56y = 4,32
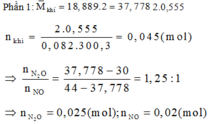

Phần 2: Gọi a, b lần lượt là số mol của AgNO3 và Cu(NO3)2
Sau phản ứng có 3 kim loại là Ag, Cu và Fe dư.
Gọi số mol Fe tham gia phản ứng là t (mol)
Bảo toàn electron ta có: nenhường= ne nhận
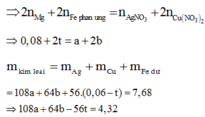
Chỉ có duy nhất Fe dư tan trong HCl
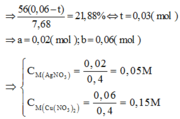
Đúng 0
Bình luận (0)
Bài 2: Hòa tan 16 g hỗn hợp CuO và MgO vào dung dịch HCl dư. Sau phản ứng thu được 32,5 g muối.
a. Tính thành phần % theo khối lượng mỗi chất trong hỗn hợp ban đầu.
b. Tính khối lượng mỗi muối thu được sau phản ứng.
Gọi \(\left\{{}\begin{matrix}n_{CuO}=x\\n_{MgO}=y\end{matrix}\right.\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x x ( mol )
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}80x+40y=16\\135x+95y=32,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{CuO}=0,1.80=8g\)
\(\Rightarrow m_{MgO}=0,2.40=8g\)
\(\%m_{CuO}=\dfrac{8}{16}.100=50\%\)
\(\%m_{MgO}=\dfrac{8}{16}.100=50\%\)
\(m_{CuCl_2}=0,1.135=13,5g\)
\(m_{MgCl_2}=0,2.95=19g\)
Đúng 3
Bình luận (0)
Một hỗn hợp gồm Al và Fe2O3, thực hiện phản ứng nhiệt nhôm ở nơi không có không khí. Hỗn hợp sản phẩm rắn thu được sau phản ứng trộn đều rồi chia thành hai phần. Cho phần 1 vào dung dịch NaOH lấy dư thì thu được 6,72 lít hiđro và chất rắn không tan trong NaOH có khối lượng bằng 34,783% khối lượng của phần 1. Hòa tan hết phần 2 vào dung dịch HCl thì thu được 26,88 lít hiđro (các thể tích ở đktc), các phản ứng đều hoàn toàn. Khối lượng từng chất rắn trong hỗn hợp ban đầu là: A. 10,8 gam Al; 64,0 g...
Đọc tiếp
Một hỗn hợp gồm Al và Fe2O3, thực hiện phản ứng nhiệt nhôm ở nơi không có không khí. Hỗn hợp sản phẩm rắn thu được sau phản ứng trộn đều rồi chia thành hai phần. Cho phần 1 vào dung dịch NaOH lấy dư thì thu được 6,72 lít hiđro và chất rắn không tan trong NaOH có khối lượng bằng 34,783% khối lượng của phần 1. Hòa tan hết phần 2 vào dung dịch HCl thì thu được 26,88 lít hiđro (các thể tích ở đktc), các phản ứng đều hoàn toàn. Khối lượng từng chất rắn trong hỗn hợp ban đầu là:
A. 10,8 gam Al; 64,0 gam Fe2O3.
B. 27,0 gam Al; 32,0 gam Fe2O3.
C. 32,4 gam Al; 32,0 gam Fe2O3.
D. 45,0 gam Al; 80,0 gam Fe2O3.
Cho một lượng hỗn hợp gồm Ag và Zn tác dụng với lượng dư dung dịch axit \(H_2SO_4\), thu được 5,6lít khí \(H_2\) (đ.k.t.c). Sau phản ứng thấy còn 6,25g một chất rắn không tan. Tính thành phần phần trăm về khối lượng mỗi kim loại trong hỗn hợp
Chất không tan là Ag.
=> mAg= 6,25(g)
nH2=0,25(mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
-> nZn=nH2= 0,25(mol)
=>mZn= 0,25 . 65=16,25(g)
=> \(\%mAg=\dfrac{6,25}{6,25+16,25}.100\approx27,778\%\\ \Rightarrow\%mZn\approx72,222\%\)
Đúng 1
Bình luận (0)























