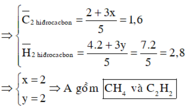Trộn H2 và O2 theo tỉ lệ về khối lượng 1:4 ta đc hỗn hợp khí A. Cho nổ hỗn hợp khí A thì thấy thể tích khí còn lại là 3,36 lít(đktc). Tính thể tích của hỗn hợp khí A(đktc)

Những câu hỏi liên quan
trộn h2 và o2 theo tỉ lệ về khối lượng tương ứng là 3:8 ta được hỗn hợp khí Q.Cho nổ hỗn hợp khí Q trong bình kín đến phản ứng hoàn toàn rồi đưa về nhiệt độ ban đầu thì thấy thể tích còn lại là 1.792 lít .tính thể tích khí Q đã phản ứng ở đktc.Giải đầy đủ giúp em với ạ!Em cảm ơn !
\(\dfrac{mH2}{mO2}\)=\(\dfrac{3}{8}\)=x
=>;mH2=x=>nH2=\(\dfrac{3x}{2}\)mol
m02=\(\dfrac{8x}{32}\)=\(\dfrac{x}{4}\)mol
PTHH: 2H2 + O2 to→ 2H2O
xét: \(\dfrac{3x}{2}\);\(\dfrac{3x}{12}\)
h2 dư, o2 hết
nh2dư=\(\dfrac{3x}{2}-\dfrac{3x}{12}\)\(=\dfrac{15x}{12}\)=\(\dfrac{1,792}{22,4}\)=0,08(mol)
=>x=\(\dfrac{0,08.12}{15}\)=0,064
nO2=\(\dfrac{0,064}{4}\)=0,016(mol)
nH2=\(\dfrac{0,064.3}{2}\)=0,096(mol)
VQ(đktc)=22,4(0,016+0,096)=2,5088(lít)
Đúng 2
Bình luận (0)
trộn h2 và o2 theo tỉ lệ về khối lượng tương ứng là 3:8 ta được hỗn hợp khí Q.Cho nổ hỗn hợp khí Q trong bình kín đến phản ứng hoàn toàn rồi đưa về nhiệt độ ban đầu thì thấy thể tích còn lại là 1.792 lít .tính thể tích khí Q đã phản ứng ở đktc.Giải đầy đủ giúp em với ạ!Em cảm ơn !
Gọi số mol H2, O2 là a, b (mol)
Ta có: \(\dfrac{m_{H_2}}{m_{O_2}}=\dfrac{3}{8}\)
=> \(\dfrac{2a}{32b}=\dfrac{3}{8}\Rightarrow\dfrac{a}{b}=\dfrac{6}{1}\) hay a = 6b
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{6b}{2}>\dfrac{b}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
2b<---b
=> \(n_{H_2\left(dư\right)}=6b-2b=4b=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
=> b = 0,02 (mol)
=> a = 0,12 (mol)
=> VQ = (0,02 + 0,12).22,4 = 3,136 (l)
Đúng 4
Bình luận (0)
Hỗn hợp khí A chứa hai hiđrocacbon, hỗn hợp khí B chứa O2 và O3 (tỉ khối của B so với H2 là 18,4). Trộn A và B theo tỉ lệ 1 : 2 về thể tích rồi đốt cháy thì chỉ còn CO2 và hơi H2O theo tỉ lệ 8 : 7 về thể tích. Nếu dẫn 5 lít A qua nước brom dư thì thể tích khí còn lại 2 lít. Công thức phân tử của hai hiđrocacbon là (các thể tích khí đo cùng điều kiện nhiệt độ, áp suất) A. CH4 và C3H6. B. CH4 và C4H2. C. CH4 và C2H2. D. CH4 và C3H4.
Đọc tiếp
Hỗn hợp khí A chứa hai hiđrocacbon, hỗn hợp khí B chứa O2 và O3 (tỉ khối của B so với H2 là 18,4). Trộn A và B theo tỉ lệ 1 : 2 về thể tích rồi đốt cháy thì chỉ còn CO2 và hơi H2O theo tỉ lệ 8 : 7 về thể tích. Nếu dẫn 5 lít A qua nước brom dư thì thể tích khí còn lại 2 lít. Công thức phân tử của hai hiđrocacbon là (các thể tích khí đo cùng điều kiện nhiệt độ, áp suất)
A. CH4 và C3H6.
B. CH4 và C4H2.
C. CH4 và C2H2.
D. CH4 và C3H4.
Cho hỗn hợp khí A gồm N2 và O2 có tỉ lệ thể tích tương ứng là 5:3
a/ tính tỉ khối của hỗn hợp khí A đối với không khí
b/ Tính thể tích (đktc) của 3,54 g khí A
c/ Phải trộn thêm vào 20 lít hỗn hợp A ở trên bao nhiêu lít khí hidro để được hỗn hợp mới có tỉ khối so với H2 bằng 6,5.Biết các thể tích đo ở cùng điều kiện nhiệt đọ và áp suất.
Hỗn hợp khí A chứa Cl2 và O2 có tỉ lệ mol tương ứng là 1 : 2.
(a) Tính phần trăm thể tích, phần trăm khối lượng của mỗi khí trong A.
(b) Tính tỉ khối hỗn hợp A so với khí H2.
(c) Tính khối lượng của 6,72 lít hỗn hợp khí A (ở đktc).
Giả sử có 1 mol khí Cl2, 2 mol khí O2
a) \(\left\{{}\begin{matrix}\%V_{Cl_2}=\dfrac{1}{1+2}.100\%=33,33\%\\\%V_{O_2}=\dfrac{2}{1+2}.100\%=66,67\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cl_2}=\dfrac{1.71}{1.71+2.32}.100\%=52,59\%\\\%m_{O_2}=\dfrac{2.32}{1.71+2.32}.100\%=47,41\%\end{matrix}\right.\)
b) \(\overline{M}=\dfrac{1.71+2.32}{1+2}=45\left(g/mol\right)\)
=> \(d_{A/H_2}=\dfrac{45}{2}=22,5\)
c) \(n_A=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> mA = 0,3.45 = 13,5 (g)
Đúng 4
Bình luận (0)
Hỗn hợp khí X gồm N2 và O2. Ở đktc 0,672 lít khí X có khối lượng 0,88 (g).
a) Tính % về thể tích các khí trong hỗn hợp X.
b) Tính thể tích H2 ở đktc có thể tích bằng thể tích của 2,2 (g) hỗn hợp khí X.
nX = 0,672/22,4 = 0,03 (mol)
Gọi nN2 = a (mol); nO2 = b (mol)
a + b = 0,03
28a + 32b = 0,88
=> a = 0,02 (mol); b = 0,01 (mol)
%VN2 = 0,02/0,03 = 66,66%
%VO2 = 100% - 66,66% = 33,34%
M(X) = 0,88/0,03 = 88/3 (g/mol)
nX = 2,2 : 88/3 = 0,075 (mol)
VH2 = VX = 0,075 . 22,4 = 1,68 (l)
Đúng 3
Bình luận (0)
hỗn hợp khí A chứa Cl và o2, có tỉ lệ có tỉ lệ mol tương ứng 1:2. tính %thể tích, % khối lượng của mỗi khí trong A, tỉ khối hh A so vs h2 và khối lượng của 6,72l hỗn hợp khí A (đktc)
\(Coi: n_{Cl_2} = 1(mol) \to n_{O_2} = 2(mol)\\ \%V_{Cl_2} = \dfrac{1}{1+2}.100\% = 33,33\%\\ \%V_{O_2} = 100\% -33,33\% = 66,67\%\\ M_A = \dfrac{1.71+2.32}{1+2}=45(g/mol)\\ d_{A/H_2} = \dfrac{45}{2} = 22,5\)
\(\text{Trong 6,72 lít khí A : }m_A = 45.\dfrac{6,72}{22,4}=13,5(gam)\)
Đúng 1
Bình luận (0)
hỗn hợp A gồm cl2 và o2, cho biết 6,72 lít hỗn hợp A ở đktc có tỉ khối so với khí H2 là 29 a, tính thành phần % thể tích mỗi khí trong hỗn hợp A b, tính khối lượng mỗi khí có trong hỗn hợp trên
a) \(\left\{{}\begin{matrix}n_{Cl_2}+n_{O_2}=\dfrac{6,72}{22,4}=0,3\\\overline{M}=\dfrac{71.n_{Cl_2}+32.n_{O_2}}{n_{Cl_2}+n_{O_2}}=2.29=58\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{Cl_2}=0,2\left(mol\right)\\n_{O_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{Cl_2}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%V_{O_2}=\dfrac{0,1}{0,3}.100\%=33,33\%\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}m_{Cl_2}=0,2.71=14,2\left(g\right)\\m_{O_2}=0,1.32=3,2\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho hỗn hợp khí A gồm N2 và O2 có tỉ lệ thể tích tương ứng là 5:3
a/ tính tỉ khối của hỗn hợp khí A đối với không khí
b/ Tính thể tích (đktc) của 3,54 g khí A
c/ Phải trộn thêm vào 20lit hỗn hợp A ở trên bao nhiêu lít khí hidro để được hỗn hợp mới có tỉ khối so với hidro bằng 6,5.Biết các thể tích đo ở cùng điều kiện nhiệt đọ và áp suất.
a/ Tỉ khối của hỗn hợp khí A đối với không khí là:
\(d_{A:kk}=\dfrac{M_A}{29}=\dfrac{60}{29}=2\)
b/ Thể tích khí A là:
\(V=22,4.3,54=79,296\left(l\right)\)
Câu c mình không biết làm :V mà 2 câu trên có đúng hay không mình cũng không biết nốt :V
Đúng 0
Bình luận (0)