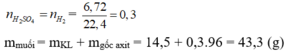Cho 24,4 g hỗn hợp toluen và etylbenzen tác dụng với dung dịch KMnO4/H2SO4 loãng. Sau phản ứng thấy khối lượng KMnO4 cần dùng là 60,04 gam. Khối lượng của axit tạo thành sau phản ứng là?

Những câu hỏi liên quan
cho m gam hỗn hợp Fe và Cu tác dụng với lượng dư dung dịch axit H2S04 loãng thì thu được 8,96 lít khí (đktc) .Sau phản ứng thấy còn 5 g chất rắn không tan .Tính thành phần % về khối lượng của mỗi kim loại trong hỗn hợp ban đầu
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,4 0,4
\(m_{Fe}=0,4.56=22,4\left(g\right)\)
\(m_{hh}=22,4+5=27,4\left(g\right)\)
\(\%m_{Fe}=\dfrac{22,4.100\%}{27,4}=81,75\%;\%m_{Cu}=100-81,75=18,25\%\)
Đúng 1
Bình luận (0)
Cho 11,2 gam Fe vào 300ml dung dịch (HNO3 0,5M và HCl 2M) thu được khí NO duy nhất và dung dịch X. Cho dung dịch X tác dụng với lượng dư dung dịch KMnO4/H2SO4 loãng. Biết các phản ứng xảy ra hoàn toàn. Khối lượng KMnO4 đã bị khử là: A. 4,71 gam B. 23,70 gam C. 18,96 gam D. 20,14 gam.
Đọc tiếp
Cho 11,2 gam Fe vào 300ml dung dịch (HNO3 0,5M và HCl 2M) thu được khí NO duy nhất và dung dịch X. Cho dung dịch X tác dụng với lượng dư dung dịch KMnO4/H2SO4 loãng. Biết các phản ứng xảy ra hoàn toàn. Khối lượng KMnO4 đã bị khử là:
A. 4,71 gam
B. 23,70 gam
C. 18,96 gam
D. 20,14 gam.
Giúp mik vớiB1: Cho 26g kẽm tác dụng vừa đủ với dung dịch H2SO4 loãng có nồng độ 20% a,Tính thể tích chất khí tạo thành (ở dktc và khối lượng muối tạo thành )b,Tính khối lượng dd H2SO4 20% cần dùng cho phản ứngc,Tính nồng độ %dd thu được sau phản ứngB2:Cho 12,8g hỗn hợp A gồm Mg và MgO vào tác dụng vừa đủ với dung dịch HCl 14,6% , thu được 4,48 lít chất khí(ở dktc)a,Tính % khối lượng mỗi chất trong A b, Tính khối lượng dung dịch HCl 14,6% dùng cho phản ứngc,Tính nồng độ % chất tan cho ...
Đọc tiếp
Giúp mik với
B1: Cho 26g kẽm tác dụng vừa đủ với dung dịch H2SO4 loãng có nồng độ 20%
a,Tính thể tích chất khí tạo thành (ở dktc và khối lượng muối tạo thành )
b,Tính khối lượng dd H2SO4 20% cần dùng cho phản ứng
c,Tính nồng độ %dd thu được sau phản ứng
B2:Cho 12,8g hỗn hợp A gồm Mg và MgO vào tác dụng vừa đủ với dung dịch HCl 14,6% , thu được 4,48 lít chất khí(ở dktc)
a,Tính % khối lượng mỗi chất trong A
b, Tính khối lượng dung dịch HCl 14,6% dùng cho phản ứng
c,Tính nồng độ % chất tan cho dung dịch sau phản ứng
Bài 1 :
PTHH : Zn + H2SO4 ------> ZnSO4 + H2
\(n_{Zn}=\frac{m}{M}=\frac{26}{65}=0,4\left(mol\right)\)
Theo PTHH : nH2 = nZn = 0,4 mol
=> Khối lượng H2 được tạo ra ở đktc là :
\(V=n\times22,4\)
\(\Rightarrow V_{H_2}=0,4\times22,4\)
\(\Rightarrow V_{H_2}=8,96\left(l\right)\)
Theo PTHH : nZnSO4 = nZn = 0,4 mol
=> Khối lượng muối được tạo thành là :
\(m=n\times M\)
\(\Rightarrow m_{ZnSO_4}=0,4\times161\)
\(\Rightarrow m_{ZnSO_4}=64,4\left(g\right)\)
b) Theo PT : \(n_{H_2SO_4}=n_{Zn}=0,4\left(mol\right)\)
=> Khối lượng \(H_2SO_4\)cần dùng cho phản ứng là :
\(m=n\times M\)
\(\Rightarrow m_{H_2SO_4}=0,4\times98\)
\(\Rightarrow m_{H_2SO_4}=39,2\left(g\right)\)
c) Nồng độ phần trăm thu được sau phản ứng là :
\(C\%=\frac{m_{ct}}{m_{dd}}\times100\%\)
\(\Rightarrow C\%=\frac{39,2}{64,4}\times100\%\approx60,9\%\)
Vậy :.........................
Cho 2 hỗn hợp Cu và Al tác dụng với 250ml H2SO4 loãng dư . Sau phản ứng thu được dung dịch B và 6,72l khí C và 3,2g kim loại
a) Dung dịch B và khí C là chất gì ?
b)Tính % khối lượng của mỗi kim loại trong hỗn hợp?
c)Tính nồng độ axit cần dùng?
a) B là \(Al_2\left(SO_4\right)_3\), C là \(Cu\)
\(b)n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 0,1 0,3
\(m_{hh}=0,2.27+3,2=8,6g\\ \%m_{Cu}=\dfrac{3,2}{8,6}\cdot100=37,21\%\\ \%m_{Al}=100-37,21=62,79\%\\ c)C_{M_{H_2SO_4}}=\dfrac{0,3}{0,25}=1,2M\)
Đúng 2
Bình luận (1)
Hòa tan hết 11,61 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe bằng 500ml dung dịch hỗn hợp axit HCl 1,5M và H2SO4 0,45M (loãng) thu được dung dịch X và 13,44 lít khí H2 (đktc). Cho rằng các axit phản ứng đồng thời với các kim loại. Tổng khối lượng muối tạo thành sau phản ứng là A. 38,935 gam B. 59,835 gam C. 38,395 gam D. 40,935 gam
Đọc tiếp
Hòa tan hết 11,61 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe bằng 500ml dung dịch hỗn hợp axit HCl 1,5M và H2SO4 0,45M (loãng) thu được dung dịch X và 13,44 lít khí H2 (đktc). Cho rằng các axit phản ứng đồng thời với các kim loại. Tổng khối lượng muối tạo thành sau phản ứng là
A. 38,935 gam
B. 59,835 gam
C. 38,395 gam
D. 40,935 gam
Đáp án : B
Vì phản ứng các axit đồng thời => số mol HCl và H2SO4 phản ứng theo tỷ lệ mol giống như nồng độ mol ban đầu của chúng
=> nHCl : nH2SO4 = 1,5 : 0,45 = 10 : 3 = 10x : 3x
=> 2nH2 = nHCl + 2nH2SO4 => 1,2 mol = 10x + 2.3x
=> x = 0,075 mol
=> Trong muối có : 0,225 mol SO42- và 0,75 mol Cl- ; ion kim loại
( phản ứng hết axit)
=> mmuối = 11,61 + 0,225.96 + 0,75.35,5 = 59,835g
Đúng 0
Bình luận (0)
Cho KI tác dụng với dung dịch KMnO4 trong môi trường H2SO4, người ta thu được 1,51 gam MnSO4 theo phưong trình phản ứng sau: KI + KMnO4 + H2SO4 g I2 +... Số mol I2 tạo thành và số mol KI phản ứng là: A. 0,00025 và 0,0005 B. 0,025 và 0,05 C. 0,25 và 0,5 D. 0,0025 và 0,005
Đọc tiếp
Cho KI tác dụng với dung dịch KMnO4 trong môi trường H2SO4, người ta thu được 1,51 gam MnSO4 theo phưong trình phản ứng sau: KI + KMnO4 + H2SO4 g I2 +... Số mol I2 tạo thành và số mol KI phản ứng là:
A. 0,00025 và 0,0005
B. 0,025 và 0,05
C. 0,25 và 0,5
D. 0,0025 và 0,005
Đáp án B
Bước đầu tiên, cần hoàn thành phương trình phản ứng với đầy đủ các chất và hệ số:
![]()
![]()
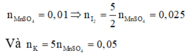
Nhận xét: Ngoài việc viết đầy đủ phản ứng như trên, các bạn vẫn có thể giải quyết bài toán bằng việc áp dụng định luật bảo toàn moi electron và bảo toàn nguyên tố:

Áp dụng định luật bào toàn mol electron, ta có:
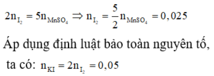
Đúng 0
Bình luận (0)
Cho KI tác dụng với dung dịch KMnO4 trong môi trường H2SO4, người ta thu được 1,51 gam MnSO4 theo phưong trình phản ứng sau: KI + KMnO4 + H2SO4 g I2 +... Số mol I2 tạo thành và số mol KI phản ứng là: A. 0,00025 và 0,0005 B. 0,025 và 0,05 C. 0,25 và 0,5 D. 0,0025 và 0,005
Đọc tiếp
Cho KI tác dụng với dung dịch KMnO4 trong môi trường H2SO4, người ta thu được 1,51 gam MnSO4 theo phưong trình phản ứng sau: KI + KMnO4 + H2SO4 g I2 +... Số mol I2 tạo thành và số mol KI phản ứng là:
A. 0,00025 và 0,0005
B. 0,025 và 0,05
C. 0,25 và 0,5
D. 0,0025 và 0,005
Đáp án B
Bước đầu tiên, cần hoàn thành phương trình phản ứng với đầy đủ các chất và hệ số:
![]()
![]()
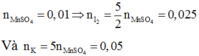
Nhận xét: Ngoài việc viết đầy đủ phản ứng như trên, các bạn vẫn có thể giải quyết bài toán bằng việc áp dụng định luật bảo toàn moi electron và bảo toàn nguyên tố:
Quá trình nhường electron:

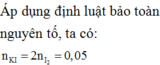
Đúng 0
Bình luận (0)
Cho 14,5g hỗn hợp Mg, Fe, Zn tác dụng hết với dung dịch H2SO4 loãng thấy thoát ra 6,72 lít H2 (đktc). Cô cạn dung dịch sau phản ứng được khối lượng muối khan tạo ra là: A. 34,3 g B. 43,3 g C. 33,4 g D. 33,8 g
Đọc tiếp
Cho 14,5g hỗn hợp Mg, Fe, Zn tác dụng hết với dung dịch H2SO4 loãng thấy thoát ra 6,72 lít H2 (đktc). Cô cạn dung dịch sau phản ứng được khối lượng muối khan tạo ra là:
A. 34,3 g
B. 43,3 g
C. 33,4 g
D. 33,8 g
Hoà tan 10 gam hỗn hợp bột Fe và
F
e
2
O
3
bằng dung dịch
H
2
S
O
4
loãng dư thu được 0,672 lít khí (đktc) và dung dịch X. Cho dung dịch X tác dụng vài NaOH dư, thu được kết tủa. Nung kết tủa trong không khí đến khối lượng không đổi được 11,2 gam chất rắn. Thể tích dung dịch
K
M
n
O...
Đọc tiếp
Hoà tan 10 gam hỗn hợp bột Fe và F e 2 O 3 bằng dung dịch H 2 S O 4 loãng dư thu được 0,672 lít khí (đktc) và dung dịch X. Cho dung dịch X tác dụng vài NaOH dư, thu được kết tủa. Nung kết tủa trong không khí đến khối lượng không đổi được 11,2 gam chất rắn. Thể tích dung dịch K M n O 4 0,1M cần phản ứng vừa đủ với dung dịch X là
A. 180 ml
B. 60 ml
C. 100 ml
D. 120 ml