Một dung dịch 42,6 gam một hỗn hợp 2 muối natri của 2 halogen kế tiếp nhau trong bảng tuần hoàn tác dụng với dung dịch agNO3 dư sau phản ứng thu được 85,1 gam xác định công thức 2 muối ban đầu

Những câu hỏi liên quan
Câu 1: Cho 42,6 g muối natri của 2 halogen liên tiếp nhau tác dụng với dung dịch AgNO3 dư, thu được 85,1 g hỗn hợp muối kết tủa. Xác định tên 2 muối halogen. Tính % khối lượng 2 muối trong hỗn hợp ban đầu.Câu 2: Cho 75,9 g muối kali của 2 halogen liên tiếp nhau tác dụng với dung dịch AgNO3 dư, thu được 127,65 g kết tủa. Xác định tên 2 muối halogen. Tính % m 2 muối halogen.Câu 3: Cho 31,1 g hỗn hợp 2 halogen liên tiếp tác dụng vừa đủ với m gam Ba, thu được 65,35 g muối. Xác định tên 2 halogen. Tí...
Đọc tiếp
Câu 1: Cho 42,6 g muối natri của 2 halogen liên tiếp nhau tác dụng với dung dịch AgNO3 dư, thu được 85,1 g hỗn hợp muối kết tủa. Xác định tên 2 muối halogen. Tính % khối lượng 2 muối trong hỗn hợp ban đầu.
Câu 2: Cho 75,9 g muối kali của 2 halogen liên tiếp nhau tác dụng với dung dịch AgNO3 dư, thu được 127,65 g kết tủa. Xác định tên 2 muối halogen. Tính % m 2 muối halogen.
Câu 3: Cho 31,1 g hỗn hợp 2 halogen liên tiếp tác dụng vừa đủ với m gam Ba, thu được 65,35 g muối. Xác định tên 2 halogen. Tính %m 2 halogen
Câu 4: Cho 5,4 g Al phản ứng vừa đủ với 34,65 g hỗn hợp 2 halogen liên tiếp. Xác định tên 2 halogen? Tính %m 2 muối halogen
X và Y là 2 nguyên tố Halogen liên tiếp nhau trong bảng tuần hoàn cho 25,3 gam hỗn hợp muối Natri của chúng td với lượng dư dung dịch AgNO3 thu đc 43,2 gam kết tủa công thức của hai muối là?
- Nếu chỉ một trong hai muối tác dụng với Bạc nitrat :
Suy ra hai muối là NaCl và NaF
\(AgNO_3 + NaCl \to AgCl + NaNO_3\\ n_{NaCl} = n_{AgCl} = \dfrac{43,2}{143,5} = 0,3(mol)\\ \Rightarrow m_{NaCl} = 0,3.58,5 = 17,55 < 25,3(\text{thỏa mãn})\)
- Nếu cả hai muối đều tác dụng với Bạc nitrat :
Gọi CTTQ của hai muối : NaX
\(NaX + AgNO_3 \to AgX + NaNO_3\\ n_{NaX} = n_{AgX} \\ \Leftrightarrow \dfrac{25,3}{23 + X} = \dfrac{43,2}{108+X}\\ \Rightarrow X = 97,13\\ M_{Br} = 80 < M_X = 97,13 < M_I = 127\)
Vậy hai muối là NaBr và NaI
Đúng 1
Bình luận (0)
Hỗn hợp X chứa đồng thời hai muối natri của hai halogen liên tiếp trong bảng tuần hoàn. Lấy một lượng X cho tác dụng vừa đủ với 100 ml dung dịch AgNO3 1M thì thu được 15 gam kết tủa. Công thức phân tử của hai muối trong X là: A. NaF và NaCl B. NaBr và NaI C. NaCl và NaI D. NaCl và NaBr
Đọc tiếp
Hỗn hợp X chứa đồng thời hai muối natri của hai halogen liên tiếp trong bảng tuần hoàn. Lấy một lượng X cho tác dụng vừa đủ với 100 ml dung dịch AgNO3 1M thì thu được 15 gam kết tủa. Công thức phân tử của hai muối trong X là:
A. NaF và NaCl
B. NaBr và NaI
C. NaCl và NaI
D. NaCl và NaBr
Đáp án D
Trường hợp 1: Hai halogen đều tạo được kết tủa với AgNO3
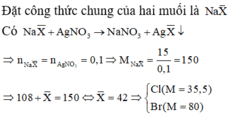
Do đó hai muối trong X là NaCl và NaBr
Trường hợp 2: Hai muối là NaF và NaCl
Phản ứng tạo thành kết tủa chỉ có AgCl và AgF là muối tan:
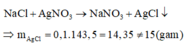
Do đó trường hợp này không thỏa mãn.
Đúng 0
Bình luận (0)
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn. a) Xác định công thức muối sunfat của kim loại kiềm ban đầu. b) Tính nồng độ % của các chất tan trong dung dịch A. c) Dung dịch muối sunfat của kim l...
Đọc tiếp
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m < 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn.
a) Xác định công thức muối sunfat của kim loại kiềm ban đầu.
b) Tính nồng độ % của các chất tan trong dung dịch A.
c) Dung dịch muối sunfat của kim loại kiềm ban đầu có thể tác dụng được với các chất nào sau đây: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Ag, Fe, CuS, Fe(NO3)2? Viết phương trình hóa học của các phản ứng xảy ra.
a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
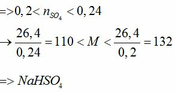
b)
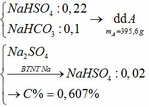
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O
Đúng 0
Bình luận (0)
Cho 1.595 gam hỗn hợp hai muối natri halogen của hai nguyên tố halogen thuộc 2 chu kì liên tiếp nhau vào H2O được 500 gam dung dịch a cho dung dịch a tác dụng với dung dịch AgNO3 dư như thu được 2,87 gam kết tủa
a) tìm tên các halogen
b) tính phần trăm khối lượng mỗi
halogen
c) tuyến C% mỗi muối trong dung dịch a
Xem chi tiết
+) Trường hợp 1: Hỗn hợp gồm NaF và NaCl
PTHH: \(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Ta có: \(n_{AgCl}=\dfrac{2,87}{143,5}=0,02\left(mol\right)=n_{NaCl}\)
\(\Rightarrow m_{NaCl}=0,02\cdot58,5=1,17\left(g\right)\) \(\Rightarrow m_{NaF}=0,415\left(g\right)\)
+) Trường hợp 2: Hỗn hợp không chứa NaF
Gọi công thức chung 2 muối là NaR
PTHH: \(NaR+AgNO_3\rightarrow NaNO_3+AgR\downarrow\)
Theo PTHH: \(n_{NaR}=n_{AgR}\) \(\Rightarrow\dfrac{1,595}{23+\overline{M}_R}=\dfrac{2,87}{108+\overline{M}_R}\)
\(\Rightarrow\overline{M}_R\approx83,3\) \(\Rightarrow\) 2 halogen cần tìm là Brom và Iot
Vậy 2 muối có thể là (NaF và NaCl) hoặc (NaBr và NaI)
*P/s: Các phần còn lại bạn tự làm
Đúng 1
Bình luận (0)
Cho dung dịch chứa 38,85 gam một muối vô cơ của carbonic acid tác dụng vừa đủ với dung dịch chứa 18 gam muối sulfate trung hòa của kim loại hóa trị II, sau phản ứng hoàn toàn thu được 34,95 gam kết tủa. Xác định công thức 2 muối ban đầu.
Cho hỗn hợp X gồm 2 amin đơn chức là đồng đẳng kế tiếp nhau tác dụng với dung dịch HCl thu được 14,2 gam hỗn hợp muối. Cho hỗn hợp muối đó vào dung dịch
AgNO
3
dư thu được 28,7 gam kết tủa. Công thức phân tử của các chất trong hỗn hợp X là A.
C
2
H
7
N
và
C
3...
Đọc tiếp
Cho hỗn hợp X gồm 2 amin đơn chức là đồng đẳng kế tiếp nhau tác dụng với dung dịch HCl thu được 14,2 gam hỗn hợp muối. Cho hỗn hợp muối đó vào dung dịch AgNO 3 dư thu được 28,7 gam kết tủa. Công thức phân tử của các chất trong hỗn hợp X là
A. C 2 H 7 N và C 3 H 9 N
B. CH 5 N và C 2 H 7 N
C. CH 5 N và C 3 H 9 N
D. C 3 H 9 N và C 4 H 11 N
Cho 7,2 gam hỗn hợp A gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA tác dụng với dung dịch HCl dư. Hấp thụ khí CO2 vào 450ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Xác định công thức 2 muối A. BeCO3 và MgCO3 B. MgCO3 và CaCO3 C. CaCO3 và SrCO3 D.Đáp án khác
Đọc tiếp
Cho 7,2 gam hỗn hợp A gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA tác dụng với dung dịch HCl dư. Hấp thụ khí CO2 vào 450ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Xác định công thức 2 muối
A. BeCO3 và MgCO3
B. MgCO3 và CaCO3
C. CaCO3 và SrCO3
D.Đáp án khác
Cho 1,5 gam muối natri halogenua tác dụng với 10 ml dung dịch bạc nitrat, sau khi phản ứng xảy ra người ta thu được 2,35 gam kết tủa. Xác định công thức của muối natri halogenua và nồng độ mol của dung dịch AgNO3
Tăng giảm khối lượng ta có; $n_{NaX}=\frac{2,35-1,5}{108-23}=0,01(mol)$
$\Rightarrow M_{NaX}=150\Rightarrow X=127$
Vậy CTHH của muối là NaI
Bảo toàn nguyên tố X và Ag ta có: $n_{AgNO_3}=n_{AgI}=0,01(mol)\Rightarrow C_{M}=1M$
Đúng 1
Bình luận (0)
PTHH: \(NaX+AgNO_3\rightarrow NaNO_3+AgX\downarrow\)
Theo PTHH: \(n_{NaX}=n_{AgX}\)
\(\Rightarrow\dfrac{1,5}{23+X}=\dfrac{2,35}{108+X}\) \(\Leftrightarrow X=127\) (Iot)
\(\Rightarrow\) Công thức: NaI
Ta có: \(n_{AgNO_3}=n_{NaI}=\dfrac{1,5}{150}=0,01\left(mol\right)\)
\(\Rightarrow C_{M_{AgNO_3}}=\dfrac{0,01}{0,01}=1\left(M\right)\)
Đúng 0
Bình luận (0)