cho biết Al tác dụng với 58,8g axit sunfuric (H2SO4) thu được nhôm sunfat ( Al2(SO4)3) và khí H2. Viết PTHH và tính khối lượng Al đã phản ứng. Tính khối lượng nhôm sunfat và thể tích khí H2 sinh ra ở điều kiện tiêu chuẩn.

Những câu hỏi liên quan
Cho 1 lượng bột Al phản ứng vừa đủ với dung dịch có chứa 44,1g H2so4 ,thu được muối Al2(so4)3 Và Khí H2.
A)tính Khối Lượng Al Phản Ứng
B)tính Thể Tích Khí H2( ở Đktc)
C)tính Khối Lượng AL2(So4)3 Theo 2 Cách
a) $n_{H_2SO_4} = \dfrac{44,1}{98} = 0,45(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
Theo PTHH :
$n_{Al} = \dfrac{2}{3}n_{H_2SO_4} = 0,3(mol)$
$m_{Al} = 0,3.27 = 8,1(gam)$
b) $n_{H_2} = n_{H_2SO_4} = 0,45(mol)$
$\Rightarrow V_{H_2} = 0,45.22,4 =1 0,08(lít)$
c)
Cách 1 : $n_{Al_2(SO_4)_3} = \dfrac{1}{3}n_{H_2SO_4} = 0,15(mol)$
$\Rightarrow m_{Al_2(SO_4)_3} = 0,15.342 = 51,3(gam)$
Cách 2 : Bảo toàn khối lượng, $m_{Al_2(SO_4)_3} = 8,1 + 44,1 - 0,45.2 = 51,3(gam)$
Đúng 2
Bình luận (0)
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vủa đủ dung dịch H2SO4 10% thu được 2,24 lít khí H2 (đktc). Khối lượng dung dịch thu được sau phản ứng là:
A. 101,48 gam
B. 101,68 gam
C. 97,80 gam
D. 88,20 gam
Đáp án B
Ta có:
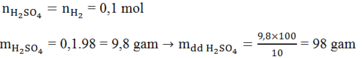
Áp dụng định luật bảo toàn khôi lượng:
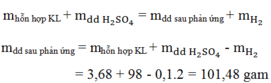
Đúng 0
Bình luận (0)
Cho magie tác dụng với axit sunfuric H2SO4 , sau phản ứng thu được muối magie sunfat MgSO4 và 4,48l khí hidro (đktc)
a, Tính khối lượng magie và axit sunfuric tham gia phản ứng
b, Tính số phân tử muối magie sunfat thu được
a) \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(n_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{Mg}=n_{H2SO4}=n_{MgSO4}=0,2\left(mol\right)\)
\(m_{Mg}=0,2.24=4,8\left(g\right)\)
\(m_{H2SO4}=0,2.98=19,6\left(g\right)\)
b)Số phân tử MgSO4=\(0,2.6.10^{23}=1,2.10^{23}\) phân tử
Mg+H2SO4-->MgSO4+H2
0,2--0,2-----------0,2 ------0,2 mol
nH2=4,48\22,4=0,2 mol
=>mMg=0,2.24=4,8 g
=>mH2SO4 =0,2.98=19,6 g
: Cho Al tác dụng vừa đủ với 58,8g H2SO4, thu được Al2(SO4)3 và khí H2
a/ Thể tích khí hiđro sinh ra ở đktc.
b/ Khối lượng nhôm đã dùng
a) \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
\(PTHH\): \(2Al+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2\)
______0,4<------0,6------------------------->0,6
=> VH2 = 0,6.22,4 = 13,44 (l)
b) mAl = 0,4.27 = 10,8(g)
Đúng 2
Bình luận (0)
\(n_{H_2SO_4}=\dfrac{58.8}{98}=0.6\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(0.4........0.6..................................0.6\)
\(V_{H_2}=0.6\cdot22.4=13.44\left(l\right)\)
\(m_{Al}=0.4\cdot27=10.8\left(g\right)\)
Đúng 0
Bình luận (0)
Cho m gam Zinc (Zn) tác dụng vừa đủ với V lít dung dịch hydrochloric acid (HCl) thu được 6,72 lít khí hydrogen (H2) ở đktca) Viết phương trình phản ứng xảy rab) Tính giá trị m và khối lượng muối thu được sau phản ứngc) Tính giá Vd) Dẫn toàn bộ lượng khí hydrogen thu được ở trên đi qua 32 gam bột Fe2O3 đun nóng. Tính khối lượng chất rắn thu được sau phản ứng
Đọc tiếp
Cho m gam Zinc (Zn) tác dụng vừa đủ với V lít dung dịch hydrochloric acid (HCl) thu được 6,72 lít khí hydrogen (H2) ở đktc
a) Viết phương trình phản ứng xảy ra
b) Tính giá trị m và khối lượng muối thu được sau phản ứng
c) Tính giá V
d) Dẫn toàn bộ lượng khí hydrogen thu được ở trên đi qua 32 gam bột Fe2O3 đun nóng. Tính khối lượng chất rắn thu được sau phản ứng
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl ---> FeCl2 + H2
0,3<---------------0,3<----0,3
=> \(\left\{{}\begin{matrix}m=0,3.65=19,5\left(g\right)\\m_{muối}=0,3.136=40,8\left(g\right)\\V_{ddHCl}:thiếu.C_M\end{matrix}\right.\)
\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
LTL: \(0,2>\dfrac{0,3}{3}\) => Fe2O3 dư
Theo pthh: nFe2O3 (pư) = \(\dfrac{1}{3}n_{H_2}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\)
nFe = \(\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\)
=> mchất rắn = 0,1.160 + 0,2.56 = 27,2 (g)
Đúng 2
Bình luận (1)
Zn+2HCl->ZnCl2+H2
0,3---0,6----0,3----0,3
n H2=0,3 mol
=>m Zn=0,3.65=19,5g
=>m muối=0,3.136=40,8g
c) thiếu đề
d)
Fe2O3+3H2-to>2Fe+3H2O
0,3------0,2
n Fe2O3=0,2 mol
=>Fe2O3 dư
=>m cr=0,2.56+0,1.160=27,2g
Đúng 2
Bình luận (0)
Cho m gam bột sắt tác dụng hoàn toàn với dung dịch HCl 10% thu được 1,12lit khí hidro ( ở đktc )
a , Viết PTHH của phản ứng trên
b , Tính khối lượng bột sắt ( m )
c , Tính khối lượng dung dịch HCl cần dùng ( Biết : Fe = 56 ; H=1 )
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,05__0,1____________0,05 (mol)
b, mFe = 0,05.56 = 2,8 (g)
c, mHCl = 0,1.36,5 = 3,65 (g)
\(\Rightarrow m_{ddHCl}=\dfrac{3,65}{10\%}=36,5\left(g\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.05......0.1...................0.05\)
\(m_{Fe}=0.05\cdot56=2.8\left(g\right)\)
\(m_{dd_{HCl}}=\dfrac{0.1\cdot36.5\cdot100}{10}=36.5\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 4. Cho 12g sắt (III) oxit phản ứng với khí Hiđro ta thu đc sắt và nước
a, Tính thể tích khí oxi (ở đktc) cần dùng
b, Tính khối lượng sắt thu đc sau phản ứng
Bài 5. Cho 19,5g Zn tác dụng với dung dịch axit sunfuric loãng thu đc kẽm sunfat và khí hiđro
a, Tính khối lượng kẽm sunfat thu đc sau phản ứng
b, Tính thể tích khí Hiđro thu đc ở (đktc)
Đọc tiếp
Bài 4. Cho 12g sắt (III) oxit phản ứng với khí Hiđro ta thu đc sắt và nước
a, Tính thể tích khí oxi (ở đktc) cần dùng
b, Tính khối lượng sắt thu đc sau phản ứng
Bài 5. Cho 19,5g Zn tác dụng với dung dịch axit sunfuric loãng thu đc kẽm sunfat và khí hiđro
a, Tính khối lượng kẽm sunfat thu đc sau phản ứng
b, Tính thể tích khí Hiđro thu đc ở (đktc)
Bài 4 câu a đề là thể tích H2 nha bạn
a)\(Fe2O3+3H2-->2Fe+3H2O\)
\(n_{Fe2O3}=\frac{12}{160}=0,075\left(mol\right)\)
\(n_{H2}=3n_{Fe2O3}=0,225\left(mol\right)\)
\(V_{H2}=0,225.22,4=5,04\left(l\right)\)
b)\(n_{Fe}=2n_{Fe2O3}=0,15\left(mol\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
Bài 6
a)\(Zn+H2SO4-->ZnSO4+H2\)
\(n_{Zn}=\frac{19,5}{65}=0,3\left(mol\right)\)
\(n_{ZnSO4}=n_{Zn}=0,3\left(mol\right)\)
\(m_{ZnSO4}=0,3.162=48,3\left(g\right)\)
b)\(n_{H2}=n_{Zn}=0,3\left(mol\right)\)
\(V_{H2}=0,3.22,4=6,72\left(l\right)\)
a)Fe2O3+3H2−−>2Fe+3H2O
0,075-------0,225---0,15 mol
nFe2O3=12/160=0,075(mol)
VH2=0,225.22,4=5,04(l)
b)
mFe=0,15.56=8,4(g)
Bài 6
a)Zn+H2SO4−−>ZnSO4+H2
0,3----------------------0,3---0,3
nZn=19,5/65=0,3(mol)
mZnSO4=0,3.162=48,3(g)
b)
=>VH2=0,3.22,4=6,72(l)
B5, Pthh: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Số mol của 19,5g Zn là:
\(n=\frac{m}{M}=\frac{19,5}{65}=0,3\left(mol\right)\)
KL \(ZnSO_4\) sau phản ứng là:
\(m=n\times M=0,3\times\left(65+32+16\times4\right)=48,3\left(g\right)\)
Thể tích khi \(H_2\)(đktc) là
\(V=n\times22,4=0,3\times22,4=6,72\)
Xem thêm câu trả lời
Cho 5,4g nhôm tác dụng vừa đủ với 29,4 g H2SO4 tạo ra a(g) nhôm sunfat (Al2(SO4)3 và 0,6g hiđro A Viết phương thức hóa học của phản ứng B Viết công thức về khối lượng các chất trong phản ứng C tính khối lượng của nhóm sunfat al2so4 sinh ra
a) 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b) Theo ĐLBTKL: mAl + mH2SO4 = mAl2(SO4)3 + mH2 (1)
c) (1) => mAl2(SO4)3 = 5,4 + 29,4 - 0,6 = 34,2 (g)
Đúng 2
Bình luận (0)
cho 0,896 lít (đktc) hỗn hợp khí gồm CH4 và C2H4 tác dụng với oxi dư. lượng oxi tham gia phản ứng là 3,52 g
a, viết pt hoá học
b, tính phần trăm thể tích mỗi khí trong hỗn hợp
c, tính khối lương khí co2 tạo ra
CH4+2O2-to>CO2+2H2O
x---------2x-------x
C2H4+3O2-to>2CO2+2H2O
y-------------3y------2y
=>Ta có :
\(\left\{{}\begin{matrix}x+y=0,04\\2x+3y=0,11\end{matrix}\right.\)
=>x=0,01, y=0,03 mol
=>%VCH4=\(\dfrac{0,01.22,4}{0,896}100\)=25%
=>%VC2H4=75%
=>m CO2=(0,01+0,03.2).44=3,08g
Đúng 4
Bình luận (0)
a, ta có PTHH :
CH4 + 2O2 \(\Rightarrow\) CO2 + 2H2O (*)
C2H4 + 3O2 \(\Rightarrow\) 2CO2 + 2H2O(+)
b, Gọi x, y lần lượ là số mol của CH4 , C2H4 ( x, y > 0 )
Ta có : nh = \(\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(\Rightarrow x+y=0,04\left(mol\right)\) (1)
lại có no2 pứ = \(\dfrac{3,52}{32}=0,11\left(mol\right)\)
\(\Rightarrow2x+3y=0,11\left(mol\right)\) (2)
Từ (1) và (2) ta có hệ pt:\(\left\{{}\begin{matrix}x+y=0,04\\2x+3y=0,11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,01\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
%VCH4 = \(\dfrac{0,01}{0,04}\times100\%=25\%\)
%VC2H4 = \(\dfrac{0,03}{0,04}\times100\%=75\%\)
c, Theo pt nCO2(*) = nCH4 = 0,01 (mol)
nCO2(+) = 2nC2H4 = 0,6 (mol)
\(\Rightarrow m_{co_2}=\left(0,01+0,6\right)\times44=26,84\left(g\right)\)
Đúng 1
Bình luận (0)



























