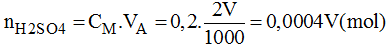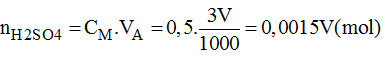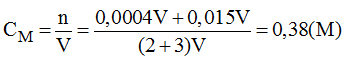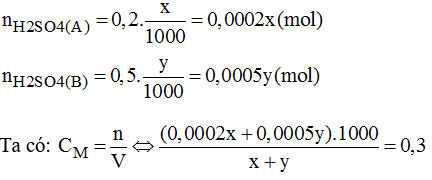Câu 5 (2,0 điểm): A là dung dịch H2SO4 0,2M, B là dung dịch H2SO4 0,5M. Phải trộn A và B theo tỉ lệ thể tích như thế nào để được dung dịch H2SO4 0,3M

Những câu hỏi liên quan
A là dung dịch
H
2
S
O
4
có nồng độ 0,2M. B là dung dịch
H
2
S
O
4
có nồng độ 0,5M.Phải trộn A và B theo tỉ lệ nào về thể tích để được dung dịch
H
2
S
O
4
có nồng độ 0,3M.
Đọc tiếp
A là dung dịch H 2 S O 4 có nồng độ 0,2M. B là dung dịch H 2 S O 4 có nồng độ 0,5M.
Phải trộn A và B theo tỉ lệ nào về thể tích để được dung dịch H 2 S O 4 có nồng độ 0,3M.
Pha chế dung dịch H 2 S O 4 0,3M.
Gọi x(l) là thể tích của dung dịch axit A.
y(l) là thể tích của dung dịch B.
n H 2 S O 4 ( A ) = C M . V A = 0,2 . x (mol)
n H 2 S O 4 ( B ) = C M . V B = 0,5 . y (mol)
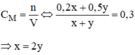
Vậy: ta phải trộn 2 thể tích dung dịch axit A với 1 thể tích dung dịch axit B, ta sẽ được dung dịch H 2 S O 4 có C M = 0,3M.
Đúng 1
Bình luận (0)
A là dung dịch H2SO4 0,2M, B là dung dịch H2SO4 0,5M. Trộn A và B theo tỉ lệ thể tích VA : VB = 2:3 được dung dich C.
a) Xác đinh Nồng độ mol của C
b) Phải trộn A và B theo tỉ lệ thể tích như thế nào để được dung dịch H2SO4 0,3M
a/ Theo quy tắc đường chéo ta có:
\(\dfrac{2}{3}=\dfrac{0,5-C_{MC}}{C_{MC}-0,2}\)
\(\Leftrightarrow C_{MC}=0,38\left(M\right)\)
b/ Theo quy tắc đường chéo ta có:
\(\dfrac{V_A}{V_B}=\dfrac{0,5-0,3}{0,3-0,2}=2\)
Đúng 0
Bình luận (3)
Dung dịch A gồm HCl 0,2M ; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M, Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH13? A. 11:9 B. 9:11 C. 101:99 D. 99:101
Đọc tiếp
Dung dịch A gồm HCl 0,2M ; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M, Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH=13?
A. 11:9
B. 9:11
C. 101:99
D. 99:101
Đáp án A
Gọi thể tích dung dịch A là V1 lít. Có nH+ = ( 0,2+0,3+0,1.2+0,3).V1 = V1 mol
Gọi thể tích dung dịch B là V2 lít. Có nOH- = ( 0,3+ 0,4+ 0,15.2).V2 = V2 mol
H+ + OH- → H2O
V1 V2
Dung dịch thu được có pH = 13 nên OH- dư
nOHdư = V2- V1 mol
[OH-]dư = (V2-V1)/(V2+ V1) = 10-1 suy ra V1: V2 = 11:9
Đúng 0
Bình luận (0)
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH 13? A. 11 : 9. B. 9 : 11. C. 101 : 99. D. 99 : 101.
Đọc tiếp
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH = 13?
A. 11 : 9.
B. 9 : 11.
C. 101 : 99.
D. 99 : 101.
Chọn B.
Nồng độ H+ ban đầu là: (0,2 + 0,3 + 0,1.2 + 0,3) = 1M.
Nồng độ OH- ban đầu là: (0,3 + 0,4 + 0,15.2) = 1M.
Dung dịch sau phản ứng có pH = 13, suy ra OH- dư, pOH = 1.
Nồng độ OH- dư là: 10-1 = 0,1M.
Áp dụng sơ đồ đường chéo cho trường hợp OH- dư, ta được:
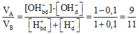
Đúng 0
Bình luận (0)
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH 13? A. 11 : 9 B. 9 : 11 C. 101 : 99 D. 99 : 101
Đọc tiếp
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH = 13?
A. 11 : 9
B. 9 : 11
C. 101 : 99
D. 99 : 101
Đáp án B.
Nồng độ H+ ban đầu là: (0,2 + 0,3 + 0,1.2 + 0,3) = 1M.
Nồng độ OH- ban đầu là: (0,3 + 0,4 + 0,15.2) = 1M.
Dung dịch sau phản ứng có pH = 13, suy ra OH- dư, pOH = 1.
Nồng độ OH- dư là: 10-1 = 0,1M.
Áp dụng sơ đồ đường chéo cho trường hợp OH- dư, ta được:
VA/VB = (1-0,1)/(1+0,1) = 9/11
Đúng 0
Bình luận (0)
A là dung dịch
H
2
S
O
4
có nồng độ 0,2M. B là dung dịch
H
2
S
O
4
có nồng độ 0,5M.Nếu trộn A và B theo tỉ lệ thể tích
V
A
:
V
B
2:3 được dung dịch C. Hãy xác định nồng độ mol của dung dịch C.
Đọc tiếp
A là dung dịch H 2 S O 4 có nồng độ 0,2M. B là dung dịch H 2 S O 4 có nồng độ 0,5M.
Nếu trộn A và B theo tỉ lệ thể tích V A : V B = 2:3 được dung dịch C. Hãy xác định nồng độ mol của dung dịch C.
Ta có: V A : V B = 2:3
Số mol H 2 S O 4 có trong 2V (l) dung dịch A:
n H 2 S O 4 = C M . V A = 0,2 . 2V = 0,4V (mol)
Số mol H 2 S O 4 có trong 3V (l) dung dịch B:
n H 2 S O 4 = C M . V B = 0,5 . 3V = 1,5V (mol)
Nồng độ mol của dung dịch H 2 S O 4 sau khi pha trộn:
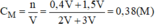
Vậy nồng độ mol của dung dịch C là 0,38M.
Đúng 1
Bình luận (0)
A là dung dịch H2SO4 0.2M. B là dung dịch H2SO4 0.5M
a) nếu trộn A và B theo tỉ lệ thể tích Va: Vb= 2:3 thì được dung dịch C có nồng độ bao nhiêu?
b) nếu phải trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch C có nồng độ là bao nhiêu?
\(a) V_A = 2(lít) \to V_B = 3(lít)\\ \Rightarrow V_{dd} = 2 + 3 = 5(lít)\\ n_{H_2SO_4\ trong\ C} = 0,2.2 + 0,5.3 = 1,9(mol)\\ C_{M_{H_2SO_4}} = \dfrac{1,9}{5} = 0,38M\)
Đúng 1
Bình luận (3)
Bài 3: Một dung dịch CuSO4 có KL riêng D 1,206 g/ml . Từ 165,84 ml dung dịch này, người ta thu đk 56,25 kết tinh CuSO4. 5H2O. Xác định nồng độ & của dung dịch CUSO4 đã dùng.
Bài 4
A là dung dịch H2SO4 0,2M , B là dung dịch H2SO4 0,5M
a) Trộn A và B theo tỉ lệ thể tích VA : Vb 2: 3 được dung dịch C. Xác định nồng độ mol của C
b) Phải trộn A và B theo tỉ lệ thể tích ntn để được dung dịch H2SO4 0,3M ?
Đọc tiếp
Bài 3: Một dung dịch CuSO4 có KL riêng D = 1,206 g/ml . Từ 165,84 ml dung dịch này, người ta thu đk 56,25 kết tinh CuSO4. 5H2O. Xác định nồng độ & của dung dịch CUSO4 đã dùng.
Bài 4
A là dung dịch H2SO4 0,2M , B là dung dịch H2SO4 0,5M
a) Trộn A và B theo tỉ lệ thể tích VA : Vb = 2: 3 được dung dịch C. Xác định nồng độ mol của C
b) Phải trộn A và B theo tỉ lệ thể tích ntn để được dung dịch H2SO4 0,3M ?
A là dung dịch H2SO4 có nồng độ 0,2M.
B là dung dịch H2SO4 có nồng độ 0,5M.
a) Nếu trôn A và B theo tỉ lệ thể tích V A : V B = 2 : 3 được dd C. Tính nồng độ mol của dd C.
b) Phải trộn A và B theo tỉ lệ nào về thể tích để được dd H2SO4 có nồng độ 0,3M?
a) Ta có: VA:VB = 2:3
Số mol H2SO4 có trong 2V dung dịch A:
Số mol H2SO4 có trong 3V dung dịch B:
Nồng độ mol của dung dịch H2SO4 sau khi pha trộn:
Vậy nồng độ mol của dung dịch C là 0,38M.
b) Pha chế dung dịch H2SO4 0,3M.
Gọi x(ml) là thể tích của dung dịch axit A.
y(ml) là thể tích của dung dịch B.
→ x = 2y . Vậy nêu y = 1 và x = 2.
Vậy ta phải trộn 2 thể tích dung dịch axit A với 1 thể tích dung dịch axit B, ta sẽ được dung dịch H2SO4 có CM = 0,3M.
Đúng 0
Bình luận (0)