cho 10gam CaCO3, MgCO3, BaCO3 vào dd HCl được CO2, H20, và 11,1 g Hỗn hợp Y CaCl2, MgCl2,BaCl2.Tìm thể tích CO2 thu được?
Câu 2: Cho các phản ứng sau:
(1) CaCO3 + 2HCl → CaCl2 + H2O + CO2 (2) MgCO3 + 2HCl → MgCl2+ H2O + CO2
(3) Na2CO3 + 2HCl → 2NaCl + H2O + CO2 (4) BaCO3 + 2HCl → BaCl2 + H2O+ CO2
(5) K2CO3 + 2HCl → 2NaCl + H2O + CO2 (6) Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
Số phản ứng có phương trình ion rút gọn CO32- + 2H+ → H2O + CO2 là
A. 2 B. 3 C. 4 D. 5
\(\text{Chọn B}\\ \text{Gồm: (3); (5);(6)}\)
Cho a g hỗn hợp BaCO3, CaCO3 tác dụng hết với V lít dd HCl 0,4 M thấy giải phóng 4,48 lít CO2 (đktc). Dẫn khí thu được vào dd Ca(OH)2 dư.
a. Khối lượng kết tủa thu được là B. 15 gam C. 20g A. 10g D. 25 gam
b. Thể tích dd HCI cần dùng là C. 1,6 lít B. 1,5 lít A. 1 lít D. 1,7 lít
c. Giá trị của a nằm trong khoảng nào? A. 10 gam <a <20 gam B. 20 gam <a <35,4 gam C. 20g <a <39,4g D. 20g < a <40g
a) \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,2----->0,2
=> mCaCO3 = 0,2.100 = 20 (g)
=> C
b)
PTHH: BaCO3 + 2HCl --> BaCl2 + CO2 + H2O
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
=> nHCl = 2.nCO2 = 2.0,2 = 0,4 (mol)
=> \(V_{dd.HCl}=\dfrac{0,4}{0,4}=1\left(l\right)\)
=> A
c)
nmuối = 0,2 (mol)
Có: 100.0,2 < a < 197.0,2
=> 20 < a < 39,4
=> C
. PTHH: C O 2 + C a ( O H ) 2 → C a C O 3 + H 2 O n C O 2 = 4 , 48 22 , 4 = 0 , 2 m o l → n C a C O 3 = n C O 2 = 0 , 2 m o l → m C a C O 3 = 0 , 2.100 = 20 g a m → Chọn C. b. PTHH: B a C O 3 + 2 H C l → B a C l 2 + C O 2 + H 2 O C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O Nhận xét: Từ PTHH ta thấy n H C l = 2 n C O 2 = 0 , 4 m o l → V H C l = 0 , 4 0 , 4 = 1 , 0 l í t → Chọn A. c. Giả sử hỗn hợp ban đầu chỉ có BaCO3 n B a C O 3 = n C O 2 = 0 , 2 m o l → m B a C O 3 = 0 , 2.197 = 39 , 4 g a m Giả sử hỗn hợp ban đầu chỉ có CaCO3 n C a C O 3 = n C O 2 = 0 , 2 m o l → m C a C O 3 = 0 , 2.100 = 20 g a m Thực tế, hỗn hợp ban đầu chứa cả BaCO3 và CaCO3 nên giá trị của a nằm trong khoảng 20 gam < a < 39,4 gam
Cho 42 gam hỗn hợp hai muối MgCO3 và CaCO3 vào 1,2 lít dung dịch HCl 1M thu được dung dịch Z. Thể tích (lít) khí CO2 (đktc) sinh ra có giá trị là
A. 10,304.
B. 9,408 < V < 11,2.
C. 9,408 < V < 13,44.
D. 11,2 < V < 13,44.
Đáp án B
Giả sử hỗn hợp chỉ gồm ![]()
hỗn hợp chỉ gồm : ![]()
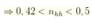 do đó HCl luôn dư
do đó HCl luôn dư
![]()
Nhiệt phân hoàn toàn 166 gam hỗn hợp MgCO3 và BaCO3 thu được V lít (đktc) khí CO2. Cho toàn bộ lượng khí CO2 hấp thụ vào dung dịch chứa 1,5 mol NaOH thu được dung dịch X. Thêm dung dịch BaCl2 vào dung dịch X thấy tạo thành 118,2 gam kết tủa. Phần trăm theo khối lượng của MgCO3 trong hỗn hợp đầu là
A. 5,06%
B. 15,18%
C. 20,24%
D. 25,30%
Đáp án A
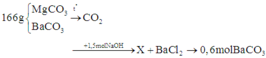
X + BaCl2 thu được kết tủa
Trong X chứa Na2CO3 và n N a 2 C O 3 = n B a C O 3 = 0,6
Vậy khi cho CO2 phản ứng với NaOH ta có phản ứng:
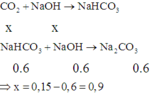
Gọi a và b lần lượt là số mol của MgCO3 và BaCO3 ta có:
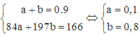
cho 13,4(g) hỗn hợp gồm CaCO3 và MgCO3 vào dd HCl dư . Sau pứ thu được 3,36(l) CO2 ( ở ĐKTC )
a) Tính số gam mỗi chất trong hỗn hợp.
b) Tính thể tích dd HCl 1M cần vừa đủ
CaCO3 + 2HCl -> CaCl2 + CO2 + H2O (1)
MgCO3 + 2HCl -> MgCl2 + CO2 + H2O (2)
nCO2=0,15(mol)
Đặt nCaCO3=a
nMgCO3=b
Ta có hệ:
\(\left\{{}\begin{matrix}100a+84b=13,4\\a+b=0,15\end{matrix}\right.\)
=>a=0,05;b=0,1
mCaCO3=100.0,05=5(g)
mMgCO3=13,4-5=8,4(g)
b;
nHCl=2nCO2=0,3(mol)
Vdd HCl=\(\dfrac{0,3}{1}=0,3\left(lít\right)\)
Nhiệt phân hoàn toàn 166 gam hỗn hợp MgCO3 và BaCO3 thu được V lít (đktc) khí CO2. Cho toàn bộ lượng khí CO2 hấp thụ vào dung dịch chứa 1,5 mol NaOH thu được dung dịch X. Thêm dung dịch BaCl2 vào dung dịch X thấy tạo thành 118,2 gam kết tủa.Xác định thành phần phần trăm theo khối lượng của mỗi muối ban đầu
\(n_{BaCO_3}=\dfrac{118,2}{197}=0,6\left(mol\right)\)
BaCl2 + Na2CO3 → BaCO3 + 2NaCl
0,6<------------0,6
TH1 : Chỉ tạo 1 muối Na2CO3
Bảo toàn nguyên tố C => \(n_{CO_2}=n_{Na_2CO_3}=0,6\left(mol\right)\) ( NaOH dư)
Đặt x, y lần lượt là số mol MgCO3, BaCO3
\(84x+197y=166\)
Bảo toàn nguyên tố C => \(x+y=n_{CO_2}=0,6\)
=> x=-0,42 ; y=1,02 ( nghiệm âm, loại )
TH2: Tạo 2 muối NaHCO3 và Na2CO3
\(n_{NaOH}=1,5\left(mol\right)\)
Bảo toàn nguyên tố Na :
\(n_{NaHCO_3}=n_{NaOH}-n_{Na_2CO_3}.2=1,5-0,6.2=0,3\left(mol\right)\)
Bảo toàn nguyên tố C :
\(n_{CO_2}=n_{NaHCO_3}+n_{Na_2CO_3}=0,3+0,6=0,9\left(mol\right)\)
Đặt x, y lần lượt là số mol MgCO3, BaCO3
\(84x+197y=166\)
Bảo toàn nguyên tố C => \(x+y=n_{CO_2}=0,9\)
=> x=0,1 ; y=0,8
=> \(\%m_{MgCO_3}=\dfrac{0,1.84}{166}.100=5,06\%\)
=> \(\%m_{BaCO_3}=100-5,06=94,94\%\)
Cho 22,95 gam BaO tan hoàn toàn trong nước được dung dịch A.
a) Dẫn từ từ khí CO2 vào dung dịch A, thu được 23,64 gam kết tủa. Tính thể tích khí CO2 (đktc) đã phản ứng.
b) Hòa tan hoàn toàn 18,4 gam hỗn hợp MgCO3 và CaCO3 trong dung dịch HCl, toàn bộ lượng khí CO2 sinh ra được hấp thụ vào dung dịch A. Hỏi có thu được kết tủa không? Tại sao?
a) \(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
\(n_{Ba\left(OH\right)_2}=n_{BaO}=0,15\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{23,64}{197}=0,12\left(mol\right)\)
Bảo toàn nguyên tố Ba => \(n_{Ba\left(HCO_3\right)_2}=0,15-0,12=0,03\left(mol\right)\)
Bảo toàn nguyên tố C: \(n_{CO_2}=0,12+0,03.2=0,18\left(mol\right)\)
=> \(V_{CO_2}=0,18.22,4=4,032\left(l\right)\)
b)Bảo toàn nguyên tố C : \(n_{CO_2}=n_{MgCO_3}+n_{CaCO_3}=a\left(mol\right)\)
Ta có : \(\dfrac{18,4}{100}< a< \dfrac{18,4}{84}\)
=> \(0,184< a< 0,22\)
\(n_{OH^-}=0,15.2=0,3\left(mol\right)\)
Lập T: \(\dfrac{0,3}{0,22}< T< \dfrac{0,3}{0,184}\)
=>\(1,36< T< 1,63\)
Do 1< \(1,36< T< 1,63\) <2
=> Phản ứng luôn tạo kết tủa
Cho 15,9g hỗn hợp X gồm 2 muối MgCO3 và CaCO3 vào 0.4l dd HCl 1M thu được dd Y
a) Hỏi dd Y có dư axit không?
b) tính lượng CO2 có thể thu được
c) Cho vào dd Y một lượng dd NaHCO3 dư thì thể tích khí CO2 thu được là 1,12l (đktc) tính khối lượng NaHCO3 thêm vào