hòa tan hoàn toàn hỗn hợp gồm Zn , ZnO bằng dung dịch HNO3 loãng , dư . kết thúc thí nghiệm không có khí thoát ra , dung dịch thu được chứa 8 gam NH4NO3 và 113,4 gam Zn(NO3)2 . phần trăm số mol Zn có trong hỗn hợp ban đầu là bao nhiêu ?
hòa tan hoàn toàn hỗn hợp gồm Zn , ZnO bằng dung dịch HNO3 loãng , dư . kết thúc thí nghiệm không có khí thoát ra , dung dịch thu được chứa 8 gam NH4NO3 và 113,4 gam Zn(NO3)2 . phần trăm số mol Zn có trong hỗn hợp ban đầu là bao nhiêu ?
theo thủy ngĩ thì là 61,50% đóBình Trần Thị
Đúng 0
Bình luận (1)
hòa tan hoàn toàn hỗn hợp gồm Zn , ZnO bằng dung dịch HNO3 loãng , dư . kết thúc thí nghiệm không có khí thoát ra , dung dịch thu được chứa 8 gam NH4NO3 và 113,4 gam Zn(NO3)2 . phần trăm số mol Zn có trong hỗn hợp ban đầu là bao nhiêu ?
hòa tan hoàn toàn hỗn hợp gồm Zn , ZnO bằng dung dịch HNO3 loãng , dư . kết thúc thí nghiệm không có khí thoát ra , dung dịch thu được chứa 8 gam NH4NO3 và 113,4 gam Zn(NO3)2 . phần trăm số mol Zn có trong hỗn hợp ban đầu là bao nhiêu ?
Hòa tan hoàn toàn 33,1 gam hỗn hợp X gồm Mg, Fe, Zn vào dung dịch H2SO4 loãng dư thấy có 13,44 lít khí thoát ra (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là A. 78,7. B. 75,5. C. 74,6. D. 90,7
Đọc tiếp
Hòa tan hoàn toàn 33,1 gam hỗn hợp X gồm Mg, Fe, Zn vào dung dịch H2SO4 loãng dư thấy có 13,44 lít khí thoát ra (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là
A. 78,7.
B. 75,5.
C. 74,6.
D. 90,7
Đáp án D
Khí thu được là H2 : n H 2 = 13 , 44 22 , 4 = 0 , 6 mol
Gọi M là kim loại chung cho Mg, Fe và Zn với hóa trị n
Sơ đồ phản ứng :
![]()
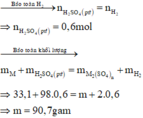
Đúng 0
Bình luận (0)
Dung dịch HNO3 loãng tác dụng với hỗn hợp gồm Zn và ZnO tạo ra dung dịch chứa 8 gam NH4NO3 và 113,4 gam Zn(NO3)2. Vậy % khối lượng của Zn trong hỗn hợp ban đầu bằng A. 71,37% B. 28,63% C. 61,61% D. 38,39%
Đọc tiếp
Dung dịch HNO3 loãng tác dụng với hỗn hợp gồm Zn và ZnO tạo ra dung dịch chứa 8 gam NH4NO3 và 113,4 gam Zn(NO3)2. Vậy % khối lượng của Zn trong hỗn hợp ban đầu bằng
A. 71,37%
B. 28,63%
C. 61,61%
D. 38,39%
Cho m gam hỗn hợp gồm Mg và Zn hòa tan hoàn toàn trong dung dịch HCl loãng, vừa đủ thì thu được dung dịch X chứa 14,4 gam hỗn hợp muối clorua và 2,912 lít khí H2 (đktc) thoát ra. Xác định giá trị m.
$Mg + 2HCl \to MgCl_2 + H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{H_2} = \dfrac{2,912}{22,4} = 0,13(mol)$
$n_{HCl} = 2n_{H_2} = 0,13.2 = 0,26(mol)$
Bảo toàn khối lượng :
$m = m_{muối} + m_{H_2} - m_{HCl} = 14,4 + 0,13.2 - 0,26.36,5 = 5,17(gam)$
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn 34,24 gam hỗn hợp X gồm FeCO3, Fe3O4 và Fe(NO3)2 trong dung dịch chứa NaNO3 và NaHSO4, kết thúc phản ứng thu được dung dịch Y (không chứa muối amoni) và hỗn hợp khí Z gồm CO2 và NO (tỉ lệ mol tương ứng 1 : 3). Dung dịch Y hòa tan tối đa 8,4 gam bột Fe (không có khí thoát ra). Nếu cho dung dịch Ba(OH)2 dư vào Y, thu được 209,18 gam kết tủa. Phần trăm khối lượng của Fe3O4 trong X là A. 33,88%. B. 40,65%. C. 27,10%. D. 54,21%.
Đọc tiếp
Hòa tan hoàn toàn 34,24 gam hỗn hợp X gồm FeCO3, Fe3O4 và Fe(NO3)2 trong dung dịch chứa NaNO3 và NaHSO4, kết thúc phản ứng thu được dung dịch Y (không chứa muối amoni) và hỗn hợp khí Z gồm CO2 và NO (tỉ lệ mol tương ứng 1 : 3). Dung dịch Y hòa tan tối đa 8,4 gam bột Fe (không có khí thoát ra). Nếu cho dung dịch Ba(OH)2 dư vào Y, thu được 209,18 gam kết tủa. Phần trăm khối lượng của Fe3O4 trong X là
A. 33,88%.
B. 40,65%.
C. 27,10%.
D. 54,21%.
Hòa tan hoàn toàn 34,24 gam hỗn hợp X gồm FeCO3, Fe3O4 và Fe(NO3)2 trong dung dịch chứa NaNO3 và NaHSO4, kết thúc phản ứng thu được dung dịch Y (không chứa muối amoni) và hỗn hợp khí Z gồm CO2 và NO (tỉ lệ mol tương ứng 1 : 3). Dung dịch Y hòa tan tối đa 8,4 gam bột Fe (không có khí thoát ra). Nếu cho dung dịch Ba(OH)2 dư vào Y, thu được 209,18 gam kết tủa. Phần trăm khối lượng của Fe3O4 trong X là A. 33,88%. B. 40,65%. C. 27,10%. D. 54,21%.
Đọc tiếp
Hòa tan hoàn toàn 34,24 gam hỗn hợp X gồm FeCO3, Fe3O4 và Fe(NO3)2 trong dung dịch chứa NaNO3 và NaHSO4, kết thúc phản ứng thu được dung dịch Y (không chứa muối amoni) và hỗn hợp khí Z gồm CO2 và NO (tỉ lệ mol tương ứng 1 : 3). Dung dịch Y hòa tan tối đa 8,4 gam bột Fe (không có khí thoát ra). Nếu cho dung dịch Ba(OH)2 dư vào Y, thu được 209,18 gam kết tủa. Phần trăm khối lượng của Fe3O4 trong X là
A. 33,88%.
B. 40,65%.
C. 27,10%.
D. 54,21%.
Hòa tan hoàn toàn hỗn hợp X gồm Zn và ZnO với tỉ lệ tương ứng 4:3 vào dung dịch chứa 1,62 mol HCl và 0,19 mol NaNO3. Kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và hỗn hợp khí Z gồm hai khí, trong đó có một khí hóa nâu được trong không khí, tỉ khối của Z đối với He bằng 6,1. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là A. 103,01. B. 99,70. C. 103,55. D. 107,92.
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Zn và ZnO với tỉ lệ tương ứng 4:3 vào dung dịch chứa 1,62 mol HCl và 0,19 mol NaNO3. Kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và hỗn hợp khí Z gồm hai khí, trong đó có một khí hóa nâu được trong không khí, tỉ khối của Z đối với He bằng 6,1. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là
A. 103,01.
B. 99,70.
C. 103,55.
D. 107,92.
Hỗn hợp Z chắc chắn có NO. MZ = 24,4 ⇒ Có H2.
⇒ Sơ đồ đường chéo ⇒ nNO : nH2 = 4 : 1
+ Đặt nNH4 = c ta có sơ đồ:
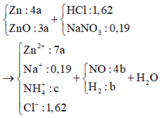
+ Phương trình bảo toàn điện tích: 4nZn = 8nNH4+ + 3nNO + 2nH2
8a = 8c + 4b×3 + b×2 8a – 14b – 8c = 0 (1).
+ Phương trình bảo toàn điện tích: 2nZn2+ + nNa+ + nNH4+ = nCl–
14a + 0,19 + c = 1,62 14a + c = 1,43 (2).
+ Phương trình bảo toàn nitơ: nNH4+ + nNOub> = nNaNO3
c×1 + 4b×1 = 0,19 4b + c = 0,19 (3)
+ Giải hệ (1) (2) và (3) ⇒ a = 0,1 và c = 0,03
⇒ mMuối = 7×0,1×65 + 0,19×23 + 0,03×18 + 1,62×35,5 = 107,92 gam
Đáp án D
Đúng 0
Bình luận (0)













