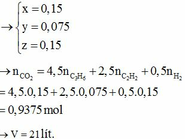Hỗn hợp X gồm axit oleic, axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam hỗn hợp X cần vừa đủ 71,792 lit khí O2 (đo ở đktc) thu được 2,25 mol CO2. Mặt khác m gam hỗn hợp X làm mất màu vừa đủ 6,4 gam brom trong CCl4. Nếu cho m gam hỗn hợp X phản ứng với dung dịch NaOH đun nóng (vừa đủ) thu glixerol và dung dịch chứa hai muối. Phần trăm khối lượng của Y trong m gam hỗn hợp X là
Hỗn hợp X gồm axit oleic, axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam hỗn hợp X cần vừa đủ 71,792 lit khí O2 (đo ở đktc) thu được 2,25 mol CO2. Mặt khác m gam hỗn hợp X làm mất màu vừa đủ 6,4 gam brom trong CCl4. Nếu cho m gam hỗn hợp X phản ứng với dung dịch NaOH đun nóng (vừa đủ) thu glixerol và dung dịch chứa hai muối. Phần trăm khối lượng của Y trong m gam hỗn hợp X là
Đọc tiếp
\(n_{O_2}=\dfrac{71,792}{22,4}=3,205\left(mol\right)\)
\(n_{Br_2}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
Đặt: \(\left\{{}\begin{matrix}\left(C_{17}H_xCOO\right)_3C_3H_5:a\left(mol\right)\\C_{17}H_yCOOH:b\left(mol\right)\\H_2O:c\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}6a+2b+3,205.2=2,25.2+c\left(BT.O\right)\\57a+18b=2,25\left(BT.C\right)\\110a+36b=2c+0,04.2\left(BT.H\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,03\\c=2,15\end{matrix}\right.\)
Có:
\(n_{Br_2}=0,04\) => X gồm \(\left\{{}\begin{matrix}C_{17}H_{33}COOH:0,02\left(mol\right)\\C_{17}H_{35}COOH:0,005\left(mol\right)\\\left(C_{17}H_{33}COO\right)_2C_3H_5\left(C_{17}H_{35}COO\right):0,01\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%_{m_Y\left(X\right)}=\dfrac{886.0,01.100\%}{15,92}=55,65\%\)
Đúng 1
Bình luận (0)
Hỗn hợp X gồm axit panmitic , axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam X thu được 1,56 mol \(CO_2\) và 1,52 mol \(H_2O\) . Mặt khác, m gam X tác dụng vừa đủ với 0,09 mol NaOH trong dung dịch, thu được glixerol và dung dịch chỉ chứa a gam hỗn hợp muối natri panmitat, natri stearat. Tính giá trị của A
\(n_Y=\dfrac{n_{CO_2}-n_{H_2O}}{k-1}=\dfrac{1.56-1.52}{3-1}=0.02\left(mol\right)\)
\(\Rightarrow n_{axit}=0.09-0.02\cdot3=0.03\left(mol\right)\)
\(n_{glixerol}=0.02\left(mol\right)\)
\(m_X=1,56\cdot12+1.52\cdot2+0.02\cdot6\cdot16+0.03\cdot2\cdot16=24.64\left(g\right)\)
\(BTKL:\)
\(m_{Muối}=24.64+0.09\cdot40-0.02\cdot92-0.03\cdot18=25.86\left(g\right)\)
Đúng 2
Bình luận (0)
Cho hỗn hợp X gồm một axit cacboxylic đơn chức, một ancol đơn chức và este tạo bởi axit và ancol đó. Đốt cháy hoàn toàn 1,55 gam hỗn hợp X thu được 1,736 lít CO2 (ở đktc) và 1,26 gam H2O. Mặt khác khi cho 1,55 gam hỗn hợp X tác dụng vừa hết với 125 ml dung dịch NaOH 0,1 M tạo ra m gam muối. Sau phản ứng tổng số gam ancol thu được là 0,74 gam và ứng với 0,01 mol. Vậy giá trị của m là: A. 1,175 gam B. 1,205 gam C. 1,275 gam D. 1,305 gam
Đọc tiếp
Cho hỗn hợp X gồm một axit cacboxylic đơn chức, một ancol đơn chức và este tạo bởi axit và ancol đó. Đốt cháy hoàn toàn 1,55 gam hỗn hợp X thu được 1,736 lít CO2 (ở đktc) và 1,26 gam H2O. Mặt khác khi cho 1,55 gam hỗn hợp X tác dụng vừa hết với 125 ml dung dịch NaOH 0,1 M tạo ra m gam muối. Sau phản ứng tổng số gam ancol thu được là 0,74 gam và ứng với 0,01 mol. Vậy giá trị của m là:
A. 1,175 gam
B. 1,205 gam
C. 1,275 gam
D. 1,305 gam
Chọn đáp án A
trước hết ta tính được ngay
Mancol = 0,74 ÷ 0,01 = 74
→ ancol là C3H7OH.
Xét phản ứng đốt cháy:
a x i t , e s t e , a n c o l + O 2 → C O 2 + H 2 O
BTKL
m O 2 = m C O 2 + m H 2 O - m h h = 0 , 0775 × 44 + 0 , 07 × 18 - 1 , 55 = 3 , 12 g a m
→ n O 2 = 0 , 0975 m o l
Tiếp phản ứng sau:
axit + NaOH → muối + nước
Vậy mmuối = 0,9 + 0,0125 × 22
= 1,175 gam
Đúng 0
Bình luận (0)
Khi nung butan với xúc tác thích hợp thu được hỗn hợp X gồm CH4, C3H6, C2H4, C2H6, C4H8, H2 và C4H10 dư. Đốt cháy hoàn toàn hỗn hợp X thu được 8,96 lít CO2 (đo ở đktc) và 9,0 gam H2O. Mặt khác, hỗn hợp X làm mất màu vừa hết 12 gam Br2 trong dung dịch nước brom. Hiệu suất phản ứng nung butan là A.75%. B.65%. C.50%. D.45%.
Đọc tiếp
Khi nung butan với xúc tác thích hợp thu được hỗn hợp X gồm CH4, C3H6, C2H4, C2H6, C4H8, H2 và C4H10 dư. Đốt cháy hoàn toàn hỗn hợp X thu được 8,96 lít CO2 (đo ở đktc) và 9,0 gam H2O. Mặt khác, hỗn hợp X làm mất màu vừa hết 12 gam Br2 trong dung dịch nước brom. Hiệu suất phản ứng nung butan là
A.75%.
B.65%.
C.50%.
D.45%.
Hỗn hợp X gồm
C
3
H
6
,
C
4
H
10
,
C
2
H
2
v
à
H
2
. Cho m gam X vào bình kín có chứa một ít bột Ni làm xúc tác. Nung nóng bình thu được hỗn hợp Y. Đốt cháy hoàn toàn Y cần dùng vừ...
Đọc tiếp
Hỗn hợp X gồm C 3 H 6 , C 4 H 10 , C 2 H 2 v à H 2 . Cho m gam X vào bình kín có chứa một ít bột Ni làm xúc tác. Nung nóng bình thu được hỗn hợp Y. Đốt cháy hoàn toàn Y cần dùng vừa đủ V lít O 2 (đktc). Sản ph m cháy cho hấp thụ hết vào bình đựng nước vôi trong dư, thu được một dung dịch có khối lượng giảm 2,145 gam. Nếu cho Y đi qua bình đựng lượng dư dung dịch brom trong C C l 4 thì có 2,4 gam brom phản ứng. Mặt khác, cho 1,12 lít (đktc) hỗn hợp X đi qua bình đựng dung dịch brom dư trong C C l 4 , thấy có 6,4 gam brom phản ứng. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V gần với giá trị nào sau đây nhất?
A. 24
B. 22
C. 26
D. 28
Đáp án B
Nhận thấy
![]()
->nên coi hỗn hợp X gồm
![]()
Khi đốt cháy Y tương đương đốt cháy X sinh ra
![]()
![]()
= 21,45
=> 114x + 94y - 18z = 21,45
Khi cho 0,5 mol hỗn hợp X đi qua bình đựng dung dịch brom dư trong C C l 4 thấy có 0,4 mol brom phản ứng
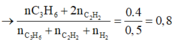
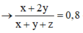
![]()
Vì phản ứng xảy ra hoàn toàn mà hỗn hợp Y sau phản ứng có khả năng làm mất B r 2 chứng tỏ => đã phản ứng hoàn toàn
Bảo toàn liên kết π => z + 0,15 = x + 2y
Ta có hệ

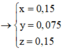
![]()
= 4,5.0,15 + 2,5.0,075 + 0,5.0,15 = 0,9375 mol
=> V= 21 lít
Đúng 0
Bình luận (0)
Hỗn hợp X gồm
C
3
H
6
,
C
4
H
10
,
C
2
H
2
v
à
H
2
. Cho m gam X vào bình kín có chứa một ít bột Ni làm xúc tác. Nung nóng bình thu được hỗn hợp Y. Đốt cháy hoàn toàn Y cần dùng vừa đủ V lít khí...
Đọc tiếp
Hỗn hợp X gồm C 3 H 6 , C 4 H 10 , C 2 H 2 v à H 2 . Cho m gam X vào bình kín có chứa một ít bột Ni làm xúc tác. Nung nóng bình thu được hỗn hợp Y. Đốt cháy hoàn toàn Y cần dùng vừa đủ V lít khí O 2 (đktc). Sản ph m cháy cho hấp thụ hết vào bình đựng nước vôi trong dư, thu được một dung dịch có khối lượng giảm 2,145 gam. Nếu cho Y đi qua bình đựng lượng dư dung dịch brom trong C C l 4 thì có 2,4 gam brom phản ứng. Mặt khác, cho 1,12 lít (đktc) hỗn hợp X đi qua bình đựng dung dịch brom dư trong C C l 4 , thấy có 6,4 gam brom phản ứng. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V gần với giá trị nào sau đây nhất?
A. 24
B. 22
C. 26
D. 28
Hỗn hợp X gồm 3 anken. Cho a gam hỗn hợp X làm mất màu vừa hết 32 gam brom. Hiđro hoá hoàn toàn hỗn hợp X thu được hỗn hợp Y. Đốt cháy hoàn toàn hỗn hợp Y thu được 22 gam CO2 và m gam H2O. Xác định m. A. 12,6 gam B. 10,8 gam C. 14,4 gam D. 9,0 gam
Đọc tiếp
Hỗn hợp X gồm 3 anken. Cho a gam hỗn hợp X làm mất màu vừa hết 32 gam brom. Hiđro hoá hoàn toàn hỗn hợp X thu được hỗn hợp Y. Đốt cháy hoàn toàn hỗn hợp Y thu được 22 gam CO2 và m gam H2O. Xác định m.
A. 12,6 gam
B. 10,8 gam
C. 14,4 gam
D. 9,0 gam
nAnken = nBr2 = 32 : 160 = 0,2
X + H2 → Y
Ta có: nH2 = nAnken = 0,2 mol
Đốt cháy Y chính là đốt cháy X và H2
Đốt cháy X có: nH2O = nCO2
Đốt cháy H2 có: nH2O = nH2
⇒ Đốt cháy Y có: nH2O = nCO2 + nH2 = nCO2 + nAnken = 22 : 44 + 0,2 = 0,7
⇒ m = 0,7.18= 12,6g
Đáp án A.
Đúng 0
Bình luận (0)
Khi nung butan với xúc tác thích hợp đến phản ứng hoàn toàn thu được hỗn hợp T gồm CH4, C2H6, C2H4, C3H6, C4H8, C4H6 và H2. Đốt cháy hoàn toàn hỗn hợp T thu được 8,96 lít CO2 (đo ở đktc) và 9,0 gam H2O. Mặt khác hỗnKhi nung butan với xúc tác thích hợp đến phản ứng hoàn toàn thu được hỗn hợp T gồm CH4, C2H6, C2H4, C3H6, C4H8, C4H6 và H2. Đốt cháy hoàn toàn hỗn hợp T thu được 8,96 lít CO2 (đo ở đktc) và 9,0 gam H2O. Mặt khác hỗn hợp T làm mất màu vừa hết 19,2 gam Br2 trong dung dịch nước brom. Phầ...
Đọc tiếp
Khi nung butan với xúc tác thích hợp đến phản ứng hoàn toàn thu được hỗn hợp T gồm CH4, C2H6, C2H4, C3H6, C4H8, C4H6 và H2. Đốt cháy hoàn toàn hỗn hợp T thu được 8,96 lít CO2 (đo ở đktc) và 9,0 gam H2O. Mặt khác hỗnKhi nung butan với xúc tác thích hợp đến phản ứng hoàn toàn thu được hỗn hợp T gồm CH4, C2H6, C2H4, C3H6, C4H8, C4H6 và H2. Đốt cháy hoàn toàn hỗn hợp T thu được 8,96 lít CO2 (đo ở đktc) và 9,0 gam H2O. Mặt khác hỗn hợp T làm mất màu vừa hết 19,2 gam Br2 trong dung dịch nước brom. Phần trăm về số mol của C4H6 trong T là hợp T làm mất màu vừa hết 19,2 gam Br2 trong dung dịch nước brom. Phần trăm về số mol của C4H6 trong T là
A. 9,091%
B. 16,67%
C. 22,22%
D. 8,333%
Đáp án A
Áp dụng định luật bảo toàn nguyên tố:
![]()
Khi cho T qua dung dịch nước brom thì C2H4, C2H4, C4H8, C4H6 phản ứng với brom.
![]() (1)
(1)
![]() (2)
(2)
Từ (1) và (2) có
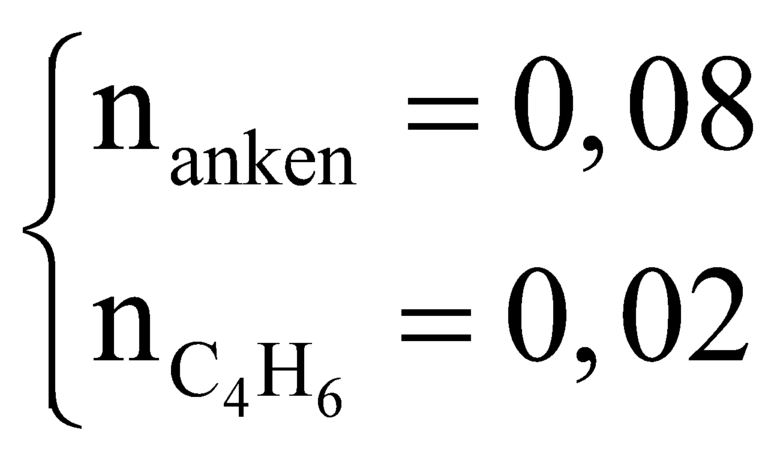
![]()
Đúng 0
Bình luận (0)
Hỗn hợp X gồm C3H6, C4H10, C2H2 và H2. Cho m gam X vào bình kín chứa một ít bột Ni làm xúc tác. Nung nóng bình thu được hỗn hợp Y. Đốt cháy hoàn toàn Y cần vừa đủ V lít O2 (đktc). Sản phẩm cháy cho hấp thụ hết vào bình đựng nước vôi trong, thu được một dung dịch có khối lượng giảm 2,45 gam. Nếu cho Y đi qua bình đựng lượng dư dung dịch brom trong CCl4 thì có 24 gam phản ứng. Mặt khác, cho 11,2 lít (đktc) hỗn hợp X đi qua bình đựng dung dịch brom dư trong CCl4 thì có 64 gam phản ứng. Biết các phả...
Đọc tiếp
Hỗn hợp X gồm C3H6, C4H10, C2H2 và H2. Cho m gam X vào bình kín chứa một ít bột Ni làm xúc tác. Nung nóng bình thu được hỗn hợp Y. Đốt cháy hoàn toàn Y cần vừa đủ V lít O2 (đktc). Sản phẩm cháy cho hấp thụ hết vào bình đựng nước vôi trong, thu được một dung dịch có khối lượng giảm 2,45 gam. Nếu cho Y đi qua bình đựng lượng dư dung dịch brom trong CCl4 thì có 24 gam phản ứng. Mặt khác, cho 11,2 lít (đktc) hỗn hợp X đi qua bình đựng dung dịch brom dư trong CCl4 thì có 64 gam phản ứng. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là:
A. 21,00
B. 14,28
C. 10,05
D. 28,56
Đáp án A
Gọi x, y, z, t lần lượt là số mol của C3H6, C4H10, C2H2 và H2 trong m gam X.
Do Y có phản ứng với dung dịch brom nên H2 hết, ta có:
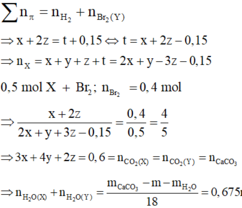
mX = mY = mC +mH = 8,55 gam
Theo định luật bảo toàn nguyên tố, ta có:
![]()
Đúng 0
Bình luận (0)
Hỗn hợp X gồm ankan M, anken N và ankin P có cùng số nguyên tử hiđro trong phân tử. Đốt cháy hoàn toàn 8,96 lít X (đktc), rồi dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư thu được 70 gam kết tủa. Mặt khác, 15 gam hỗn hợp X làm mất màu tối đa V ml dung dịch Br2 1M. Biết các phản ứng xảy ra hoàn toàn. a) Xác định công thức phân tử, viết công thức cấu tạo của M, N và P. b) Tính V.
Đọc tiếp
Hỗn hợp X gồm ankan M, anken N và ankin P có cùng số nguyên tử hiđro trong phân tử. Đốt cháy hoàn toàn 8,96 lít X (đktc), rồi dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư thu được 70 gam kết tủa. Mặt khác, 15 gam hỗn hợp X làm mất màu tối đa V ml dung dịch Br2 1M. Biết các phản ứng xảy ra hoàn toàn.
a) Xác định công thức phân tử, viết công thức cấu tạo của M, N và P.
b) Tính V.
a) Mấu chốt ở chỗ chỉ số H bằng nhau
Đặt ankan M: CnH2n+2
→anken N: Cn+1H2n+2 (giải thích: anken có C = ½ H)
ankin P: Cn+2H2n+2 [giải thích: ankin có C = ½ (H + 2)]
·Xét TN đốt cháy hỗn hợp X:
nX = 0,4 mol; nCO2 = nCaCO3 = 0,7 mol
=> C trung bình =0,7: 0,4 = 1,75
=> Trong hỗn hợp có ít nhất một chất có số C < 1,75
=> n = 1
→M: CH4
N: C2H4 → CTCT: CH2=CH2
P: C3H4 → CTCT: CH≡C–CH3
b) Đặt CTTB: C1,75H4 (M=25)
=> số liên kết pi TB = 0,75
nX = 15 : 25 = 0,6mol
C1,75H4 + 0,75Br2 → C1,75H4Br1,5
0,6 → 0,45 (mol)
=> V = 450ml
Đúng 0
Bình luận (0)