3,51 gam muối ăn (NaCl) có số mol là
A. 0,052 mol.
B. 0,15 mol.
C. 0,03 mol.
D. 0,06 mol.
Trong một dung dịch có chứa 0,01 mol Ca2+, 0,01 mol Mg2+, 0,03 mol Clvà x mol NO3
-
.
Vậy giá trị của x là
A. 0,05 mol.
B. 0,04 mol.
C. 0,03 mol.
D. 0,01 mol.
Số mol NaCl có trong 200 ml dung dịch NaCl 3M là *
1 điểm
A. 0,2 mol.
B. 1,2 mol.
C. 0,6 mol.
D. 0,3 mol.
Số mol electron cần để oxi hóa 1,5 mol Al thành Al³⁺ là
A. 3 mol.
B. 4,5 mol.
C. 1,5 mol.
D. 0,5 mol.
Sục khí CO2 vào dung dịch Ca(OH)2 thu được 3 gam kết tủa. Lọc tách kết tủa rồi đun nóng nước còn lại thu thêm 2gam kết tủa nữa. Giá trị của a là
A. 0,05 mol.
B. 0,06 mol.
C. 0,07 mol.
D. 0,08 mol.
Số mol CaCO3 là nCaCO3 = 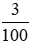
Số mol kết tủa thêm nCaCO3 = 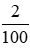
Theo pt ⇒ nCa(HCO3)2 = nCaCO3 = 0,02 mol
Tổng số mol CO2 = nCO2 (1) + nCO2 (2) = 0,03 + 2. 0,02 = 0,07 (mol)
Chọn C
Có bao nhiêu mol nguyên tử O trong 1 mol phân tử N2O5?
A 4 mol.
B 2 mol.
C 3 mol.
D 5 mol.
Số mol của kali hiđroxit có trong 200 gam dung dịch kalihiđroxit 5,6% là?( K=39, H=1, O=16 )
A.
3,5 mol.
B.
0,1mol .
C.
3,57 mol.
D.
0,2 mol.
\(m_{KOH}=\dfrac{200.5,6}{100}=11,2\left(g\right)=>n_{KOH}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
=> D
Số mol của kali hiđroxit có trong 200 gam dung dịch kalihiđroxit 5,6% là?( K=39, H=1, O=16 )
A.
3,5 mol.
B.
0,1mol .
C.
3,57 mol.
D.
0,2 mol.
\(n_{KOH}=\dfrac{5,6.200}{100.56}=0,2\left(mol\right)\)
=> D
Số mol của kali hiđroxit có trong 200 gam dung dịch kalihiđroxit 5,6% là?( K=39, H=1, O=16 )
A.
3,5 mol.
B.
0,1mol .
C.
3,57 mol.
D.
0,2 mol.
Đáp án D
\(m_{KOH}=200.5,6\%=11,2\left(gam\right)\\ n_{KOH}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Cho 15,2 gam muối sắt (II) sunfat tác dụng với dung dịch H2SO4 đặc nóng, dư, sau phản ứng thu được dung dịch X và khí SO2. Tính số mol H2SO4 đã tham gia phản ứng
A. 0,1 mol.
B. 0,2 mol
C. 0,3 mol.
D. 0,4 mol.
nFeSO4=15,2/152=0,1(mol)
PTHH: 2 FeSO4 + 2H2SO4(đ) -to-> Fe2(SO4)3 + SO2 + 2 H2O
0,1_______________0,1_________0,05______0,1(mol)
=> Chọn A
Cho 15,2 gam muối sắt (II) sunfat tác dụng với dung dịch H2SO4 đặc nóng, dư, sau phản ứng thu được dung dịch X và khí SO2. Tính số mol H2SO4 đã tham gia phản ứng
A. 0,1 mol.
B. 0,2 mol
C. 0,3 mol.
D. 0,4 mol.
\(2FeSO_4+2H_2SO_4 \buildrel{{t^o}}\over\longrightarrow Fe_2(SO_4)_3+SO_2+2H_2O\\ n_{FeSO_4}=\frac{15,2}{152}=0,1(mol)\\ n_{H_2SO_4}=n_{FeSO_4}=0,1(mol)\\ \to A \)