“Trong quá trình phản ứng, lượng chất phản ứng ….., lượng chất sản phẩm ….…”. Cụm từ cần điền vào dấu (…) trong nội dung trên lần lượt là *
A, B, C là ba chất hữu cơ có %C, %H (theo khối lượng) lần lượt là 92,3% và 7,7%, tỉ lệ khối lượng mol tương ứng là 1: 2 : 3. Từ A có thể điều chế B hoặc C bằng một phản ứng. C không làm mất màu nước brom. Đốt 0,1 mol B rồi dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch nước vôi trong dư. Khối lượng dung dịch tăng hoặc giảm bao nhiêu gam ?
A. giảm 21,2 gam.
B. giảm 18,8 gam.
C. Tăng 21,2 gam.
D. tăng 40 gam.
Đun nóng m gam hỗn hợp Cu và Fe có tỉ lệ khối lượng tương ứng 7:3 với một lượng dung dịch HNO3. Khi các phản ứng kết thúc, thu được 0,75m gam chất rắn, dung dịch X và 5,6 lít hỗn hợp khí (đktc) gồm NO và NO2 (không có sản phẩm khử khác của N+5). Biết lượng HNO3 đã phản ứng là 44,1 gam. Giá trị của m là:
A. 448
B. 40,5
C. 33,6
D. 50,4
Đáp án D
Khối lượng Fe = 0,3m gam và khối lượng Cu = 0,7m gam
Sau phản ứng còn 0,75m gam → Fe chỉ phản ứng 0,25m gam; Fe dư vậy sau phản ứng chỉ thu được muối Fe2+.
Ta có:
![]()
Số mol của Fe(NO3)2 = 0,25m/56
Sơ đồ phản ứng:
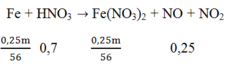
Áp dụng ĐLBT nguyên tố N ta có:
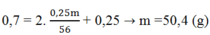
Câu 4: Các chất hữu cơ đơn giản đầu tiên được tổng hợp từ chất vô cơ là nhờ:
A. enzim có sẵn trong môi trường xúc tác phản ứng.
B. các phản ứng xảy ra tự nhiên.
C. nguồn năng lượng tự nhiên: năng lượng mặt trời, núi lửa ...
D. năng lượng vũ trụ.
Câu 5: Vật chất hữu cơ giống với vật chất vô cơ ở điểm cơ bản nào?
A. Thành phần gồm các nguyên tố tự nhiên.
B. Đều có cấu trúc đa phân.
C. Đều có thể tương tác lẫn nhau và tương tác với môi trường.
D. Đều tồn tại trong tế bào hoặc trong cơ thể sống.
cho 8,4g sắt chảy trong bình chứa 1,12 L khí oxi
a. tính khối lượng oxit săt́ từ thu đc
b. chất nào còn dư sau phản ứng?, khối lượng chất dư là bn?
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_{O2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Pt : \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4|\)
3 2 1
0,15 0,05 0,025
a) Lập tỉ số so sánh : \(\dfrac{0,15}{3}>\dfrac{0,05}{2}\)
⇒ Fe dư , O2 phản ứng hết
⇒ Tính toán dựa vào số mol của O2
\(n_{Fe3O4}=\dfrac{0,05.1}{2}=0,025\left(mol\right)\)
⇒ \(m_{Fe3O4}=0,025.232=5,8\left(g\right)\)
b) \(n_{Fe\left(dư\right)}=0,15-\left(\dfrac{0,05.3}{2}\right)0,075\left(mol\right)\)
⇒ \(m_{Fe\left(dư\right)}=0,075.56=4,2\left(g\right)\)
Chúc bạn học tốt
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right);n_{O_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\ a,PTHH:3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ Vì:\dfrac{0,05}{2}< \dfrac{0,15}{3}\Rightarrow Fedư\\ n_{Fe_3O_4}=\dfrac{1}{2}.n_{O_2}=\dfrac{0,05}{2}=0,025\left(mol\right)\\ m_{Fe_3O_4}=232.0,025=5,8\left(g\right)\\ b,n_{Fe\left(dư\right)}=0,15-\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow m_{Fe}\left(dư\right)=0,075.56=4,2\left(g\right)\)
nhiệt phân 87,7 gam hỗn hợp gồm KMnO4 và KClO3. phản ứng thu được chất rắn A có khối lượng 74,9 gam. biết H hai phản ứng là 80%. a) tính khối lượng mỗi chất có trong hỗn hợp đầu b) tính khối lượng từng chất trong A
Câu 15: Điều nào sau đây không phải là đặc điểm của mức phản ứng?
A. Trong một kiểu gen, mỗi gen có mức phản ứng riêng.
B. Tính trạng chất lượng có mức phản ứng hẹp, tính trạng số lượng có mức phản ứng rộng.
C. Mức phản ứng về mỗi tính trạng là giống nhau giữa các giống.
D. Mức phản ứng do gen quy định nên di truyền.
Sục khí Clo tới dư vào dung dịch chứa 0,4 mol H2S. Sau phản ứng thu được dung dịch A
a) Viết và cân bằng phản ứng bằng phương pháp cân bằng e. Xác định vai trò các chất tham gia phản ứng
b) Tính thể tích dung dịch NaOH 1 M cần trung hòa hết A
c) Cho 0,3 mol BaCl2 vào A. Tính khối lượng các chất thu được
Cho 6.048 g Mg phản ứng hết với 189 g dd HNO3 40% thu được dd X ( không chứa muối) amoni và hỗn hợp hkí là oxjt của njtơ.thêm 392 g dd KOH 20% vào dd X, rồi cô cạn và nung sản phẩm đến khối lượng ko đổi thu được 118,06 g hỗn hợp chất rắn. Hãy xác định nồn độ % của các chất trong X
nMg = 0,252, nHNO3 = 1,2 & nKOH = 1,4
Vậy KOH dư, Mg2+ đã kết tủa hết, phần dung dịch chứa KNO3 & KOH dư, phần kết tủa chứa Mg(OH)2, cô cạn và nung thu được KNO2 & KOH dư & MgO
nKOH ban đầu = nKNO2 + nKOH dư = 1,4
m rắn = 85nKNO2 + 56nKOH dư + 40.0,252 = 118,06
—> nKNO2 = 1,02 & nKOH dư = 0,38
Bảo toàn N —> nN trong khí = nHNO3 – nKNO3 = 0,18
Vậy mỗi N+5 đã nhận 0,252.2/0,18 = 2,8 mol electron
—> Số oxi hóa trung bình của N = 5 – 2,8 = +2,2
—> Oxit trung bình NO1,1 (0,18 mol)
nHNO3 pư = 0,252.2 + 0,18 = 0,684
—> nHNO3 dư = 0,516
mdd = mMg + mddHNO3 – mNO1,1 = 189,36
—> C% HNO3 dư & C% Mg(NO3)2
Để xác định hàm lượng nitơ tổng trong chất hữu cơ, theo phương pháp Ken-đan người ta cân 2g mẫu rồi tiến hành vô cơ hóa mẫu để bộ lượng nitơ chuyển thành muối amoni. Sau đó sục dung dịch NaOH 40% vào dung dịch sau phản ứng. Lượng NH3 thoát ra được hấp thụ hoàn toàn bởi 20ml dung dịch H2SO4 0,1M. Chuẩn độ lượng dư H2SO4 cần 10ml NaOH 0,1M nữa. Vậy %N trong chất hữu cơ là bao nhiêu?
A. 2,0%
B. 2,2%
C. 1,8%
D. 2,1%