mọi người giúp em với
Một electron hóa trị nào đó của nguyên tử O (Z = 8) ở trạng thái cơ bản có thể có bộ 4 số
lượng tử như sau:
a. (1, 0, 0, +1/2) b. (2, 2, 0, -1/2) c. (2, 1, -1, +1/2) d. (3, 0, 0, +1/2)
Một phôtôn có năng lượng 1,79 eV bay qua hai nguyên tử có mức kích thích 1,79 eV, nằm trên cùng phương của phôtôn tới. Các nguyên tử này có thể ở trạng thái cơ bản hoặc trạng thái kích thích. Gọi X là số phôtôn có thể thu được sau đó, theo phương của phôtôn tới.Hãy chỉ ra đáp số sai.
A. x = 0. B. x = 1. C. x = 2. D. x = 3.
Câu 1 : Lưu huỳnh có thể tồn tại ở những trạng thái số oxi hoá nào? A. -2; +4; +5; +6 B. -3; +2; +4; +6. C. -2; 0; +4; +6 D. +1 ; 0; +4; +6
Hãy chọn phương án trả lời đúng.
Quần thể nào trong số các quần thể nêu dưới đây ở trạng thái cân bằng di truyền?
| Quần thể | Tần số kiểu gen AA | Tần số kiểu gen Aa | Tần số kiểu gen aa |
|---|---|---|---|
| 1 | 1 | 0 | 0 |
| 2 | 0 | 1 | 0 |
| 3 | 0 | 0 | 1 |
| 4 | 0,2 | 0,5 | 0,3 |
a) Quần thể 1 và 2 b) Quần thể 3 và 4
c) Quần thể 2 và 4 d) Quần thể 1 và 3
Cho các phát biểu sau
1. Tinh thể ion kém bền do lực hút tĩnh điện kém
2. Ở thể rắn, NaCl tồn tại dưới dạng tinh thể ion
3. Các chất chỉ có liên kết cộng hóa trị không cực không dẫn điện ở mọi trạng thái
4. Phân tử CO2 có liên kết cộng hóa trị phân cực
5. I2 có mạng tinh thể nguyên tử
6. Trong phân tử CH4, nguyên tử C có cộng hóa trị 4
7. Trong các đơn chất, số oxi hóa của nguyên tố khác không
8. Số oxi hóa của hiđro trong mọi hợp chất luôn +1
Số phát biểu đúng là
A. 3
B. 4
C. 6
D. 2
Các trường hợp thỏa mãn: 2-3-6
ĐÁP ÁN A
Cho các phát biểu sau
1. Tinh thể ion kém bền do lực hút tĩnh điện kém
2. Ở thể rắn, NaCl tồn tại dưới dạng tinh thể ion
3. Các chất chỉ có liên kết cộng hóa trị không cực không dẫn điện ở mọi trạng thái
4. Phân tử CO2 có liên kết cộng hóa trị phân cực
5. I2 có mạng tinh thể nguyên tử
6. Trong phân tử CH4, nguyên tử C có cộng hóa trị 4
7. Trong các đơn chất, số oxi hóa của nguyên tố khác không
8. Số oxi hóa của hiđro trong mọi hợp chất luôn +1
Số phát biểu đúng là
A. 3
B. 4
C. 6
D. 2
Đáp án A
Các trường hợp thỏa mãn: 2-3-6
Khi kích thích nguyên tử hiđrô ở trạng thái cơ bản, bán kính quỹ đạo dừng của electron tăng lên 9 lần. Tính các bước sóng của các bức xạ mà nguyên tử hiđrô có thể phát ra sau đó, biết rằng năng lượng của các trạng thái dừng của nguyên tử hiđrô là E n = - 13 , 6 n 2 e V với n = 1, 2,...
A. 0,103mm, 0,121μm, 0,657μm
B. 0,103mm, 0,421μm, 0,558μm
C. 0,203mm, 0,321μm, 0,517μm
D. 0,155mm, 0,421μm, 0,837μm
Đáp án: A
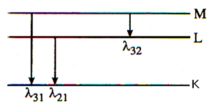
Nguyên tử hiđrô ở trạng thái kích thích, electron ở trạng thái dừng ứng với n2 = 9 => n = 3.
Sau đó electron trở về các lớp trong cơ thể phát ra các bức xạ có bước sóng l31, l32, l21 như hình vẽ.
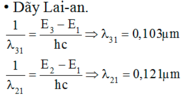
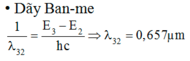
Cho cấu hình electron nguyên tử (ở trạng thái cơ bản) các nguyên tố như sau:
(1): ls22s22p63s23p64s1;
(2) ls22s22p63s23p3
(3) ls22s22p63s23p1
(4) ls22s22p3
(5) ls22s22p63s2
(6) 1s22s22p63s1
Các cấu hình electron không phải của kim loại là
A. (2), (4).
B. (2), (4), (5), (6)
C. (2), (3), (4).
D. (1), (2), (3), (4).
Chọn đáp án A
Có thể dùng đặc điểm cấu hình electron kim loại thường có 1, 2 hoặc 3 electron lớp ngoài cùng nhưng điều này chưa đúng 100% nên tốt nhất là nhớ số proton để tìm chính xác nguyên tố
(1) có Z = 19 là cấu hình của kali Þkim loại
(2) có Z = 15 là cấu hình của photpho Þ phi kim
(3) có Z = 13 là cấu hình của nhôm Þ kim loại
(4) có Z = 7 là cấu hình của nitơ Þ phi kim
(5) có Z = 12 là cấu hình của magie Þ kim loại
(6) có Z = 11 là cấu hình của natri Þ kim loại
Hợp chất Natri cacbonat có công thức hóa học là Na 2 CO 3 thì tỉ lệ số nguyên tử các nguyên tố theo thứ tự Na : C : O là
A.2 : 0 : 3.
B.2 : 1 : 3.
C.1 : 2 : 3.
D.3 : 2 : 1
Năng lượng của nguyên tử hiđrô ở các trạng thái dừng được xác định bằng công thức: E n = − 13 , 6 n 2 e V , với n = 1, 2, 3,... ứng với trạng thái dừng có electron chuyển động trên quỹ đạo K, L, M,... Năng lượng ion hóa (năng lượng cần thiết để biến nguyên tử trung hòa về điện thành ion dương) của nguyên tử hiđrô khi nó đang ở trạng thái cơ bản là bao nhiêu ? Lấy e = 1 , 6 . 10 - 19 C
A. 2 , 024 . 10 - 18 J
B. 1 , 476 . 10 - 18 J
C. 4 , 512 . 10 - 18 J
D. 2 , 176 . 10 - 18 J