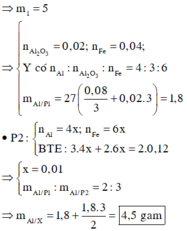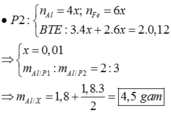Những câu hỏi liên quan
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần. - Phần một: Cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một. - Phần hai: Cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là A. 4,5 gam B. 7,2 gam C. 5,4 gam D. 8,1 gam
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần.
- Phần một: Cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một.
- Phần hai: Cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là
A. 4,5 gam
B. 7,2 gam
C. 5,4 gam
D. 8,1 gam
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần: - Phần một: Cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một. - Phần hai: Cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là A. 8,1 gam. B. 7,2 gam. C. 5,4 gam. D. 4,5 gam.
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần:
- Phần một: Cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một.
- Phần hai: Cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là
A. 8,1 gam.
B. 7,2 gam.
C. 5,4 gam.
D. 4,5 gam.
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần. - Phần một: cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một. - Phần hai: cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là A. 8,1 gam. B. 7,2 gam. C. 5,4 gam. D. 4,5 gam.
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần.
- Phần một: cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một.
- Phần hai: cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là
A. 8,1 gam.
B. 7,2 gam.
C. 5,4 gam.
D. 4,5 gam.
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần. - Phần một: Cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một. - Phần hai: Cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là A. 8,1 gam B. 7,2 gam C. 5,4 gam D. 4,5 gam
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm (Al và Fe2O3) trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Chia Y thành hai phần.
- Phần một: Cho tác dụng với dung dịch NaOH (dư), thu được 0,896 lít khí (đktc) và còn lại chất rắn không tan chiếm 44,8% khối lượng phần một.
- Phần hai: Cho tác dụng với dung dịch HCl (dư), thu được 2,688 lít khí (đktc). Khối lượng nhôm đem trộn là
A. 8,1 gam
B. 7,2 gam
C. 5,4 gam
D. 4,5 gam
Lấy 1 hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm (không không khí). Để nguội sản phẩm sau đó chia thành 2 phần không đều nhau. P1 cho tác dụng với dd NaOH dư thu 8,96 (lit) H2(đktc) và phần ko tan có khối lượng 44,8% khối lượng P1. P2 hoà tan hoàn toàn trong dd HCl thu 2,688 (lit) H2 (đktc). Tính m hh ban đầu. A. 83,21 B. 53,20 C. 50,54 D. 57,5
Đọc tiếp
Lấy 1 hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm (không không khí). Để nguội sản phẩm sau đó chia thành 2 phần không đều nhau. P1 cho tác dụng với dd NaOH dư thu 8,96 (lit) H2(đktc) và phần ko tan có khối lượng = 44,8% khối lượng P1. P2 hoà tan hoàn toàn trong dd HCl thu 2,688 (lit) H2 (đktc). Tính m hh ban đầu.
A. 83,21
B. 53,20
C. 50,54
D. 57,5
Đáp án : D
P1 : nH2 = 0,4 mol => nAl = 0,8/3 (mol)
Vì có Al dư nên Fe2O3 chuyển hết thành Fe
Gọi số mol các chất trong phần 1 là : 2a mol Fe ; a mol Al2O3 ; b mol Al
Phần hai sẽ có thành phần các chất là : 2ak mol Fe ; ak mol Al2O3 ; bk mol Al
P1 : nAl = b = 0,8/3 (mol)
Và mFe = 44,8%.mP1 => 112a = 0,448( 112a + 102a + 27b) => 4a = 3b
P2 : nH2 = 2ak + 1,5bk = 0,12 mol
Giải hệ 3 phương trình 3 ẩn trên ta được :
,a = 0,2 mol ; k = 0,15
=> m2 = 0,15m1
=> m = 1,15m1 = 57,5g
Đúng 0
Bình luận (0)
Lấy 1 hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm (không không khí). Để nguội sản phẩm sau đó chia thành 2 phần không đều nhau. P1 cho tác dụng với dd NaOH dư thu 8,96 (lit) H2 đktc) và phần ko tan có khối lượng bằng 44,8% khối lượng P1. P2 hoà tan hoàn toàn trong dd HCl thu 2,688 (lit) H2 (đktc). Tính m hh ban đầu. A. 57,5 B. 83,21 C. 53,20 D. 50,54
Đọc tiếp
Lấy 1 hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm (không không khí). Để nguội sản phẩm sau đó chia thành 2 phần không đều nhau. P1 cho tác dụng với dd NaOH dư thu 8,96 (lit) H2 đktc) và phần ko tan có khối lượng bằng 44,8% khối lượng P1. P2 hoà tan hoàn toàn trong dd HCl thu 2,688 (lit) H2 (đktc). Tính m hh ban đầu.
A. 57,5
B. 83,21
C. 53,20
D. 50,54
Đáp án A
P 1 : n H 2 = 0 , 4 m o l → n A l = 0 , 8 3 m o l
Vì có Al dư nên Fe2O3 chuyển hết thành Fe
Gọi số mol các chất trong phần 1 là: 2a mol Fe; a mol Al2O3; b mol Al
Phần hai sẽ có thành phần các chất là: 2ak mol Fe; ak mol Al2O3; bk mol Al
P 1 : n A l = b = 0 , 8 3 m o l
Và m F e = 44 , 8 % . m P 1 → 112 a = 0 , 448 ( 112 a + 102 a + 27 b ) → 4 a = 3 b
P 2 : n H 2 = 2 a k + 1 , 5 b k = 0 , 12 m o l
Giải hệ 3 phương trình 3 ẩn trên ta được:
a = 0,2 mol ; k = 0,15
→ m2= 0,15m1
→ m = 1,15m1 = 57,5g
Đúng 0
Bình luận (0)
Lấy 1 hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm (không không khí). Để nguội sản phẩm sau đó chia thành 2 phần không đều nhau. P1 cho tác dụng với dd NaOH dư thu 8,96 (lit) H2 đktc) và phần ko tan có khối lượng bằng 44,8% khối lượng P1. P2 hoà tan hoàn toàn trong dd HCl thu 2,688 (lit) H2 (đktc). Tính m hh ban đầu. A. 57,5 B. 83,21 C. 53,20 D. 50,54
Đọc tiếp
Lấy 1 hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm (không không khí). Để nguội sản phẩm sau đó chia thành 2 phần không đều nhau. P1 cho tác dụng với dd NaOH dư thu 8,96 (lit) H2 đktc) và phần ko tan có khối lượng bằng 44,8% khối lượng P1. P2 hoà tan hoàn toàn trong dd HCl thu 2,688 (lit) H2 (đktc). Tính m hh ban đầu.
A. 57,5
B. 83,21
C. 53,20
D. 50,54

Giải hệ 3 phương trình 3 ẩn trên ta được:
a = 0,2 mol; k = 0,15
→ m2= 0,15m1
→ m = 1,15.m1 = 57,5g
Đúng 0
Bình luận (0)
nung m (g) hh X gồm Fe3O4 và Al trong điều kiện không có không khí. sau khi pứ xảy ra hoàn toàn thu được hh Y. chia hh Y thành 2 phần
P1: cho tác dụng với dd NaOH dư thu được 0,06mol H2, dd Z và 20,16g chất rắn không tan.
P2: cho tác dụng với dd HCl dư thu được 0,63mol H2
Tính thành phần % khối lượng các chất trong hh X
PTHH: 3Fe3O4 + 8Al --to--> 4Al2O3 + 9Fe
=> \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{9}{4}\)
P1: Gọi (nAl; nFe; nAl2O3) = (a;b;c)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,04<---------------------------------0,06
=> a = 0,04 (mol)
Chất rắn không tan là Fe
\(b=\dfrac{20,16}{56}=0,36\left(mol\right)\)
Có: \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{b}{c}=\dfrac{9}{4}\) => c = 0,16 (mol)
P2: Gọi (nAl; nFe; nAl2O3) = (ak;bk;ck)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
ak------------------>1,5ak
Fe + 2HCl --> FeCl2 + H2
bk------------------>bk
=> 1,5ak + bk = 0,63
=> k = 1,5
Bảo toàn Fe: \(n_{Fe_3O_4\left(X\right)}=\dfrac{b+bk}{3}=\dfrac{0,36+0,36.1,5}{3}=0,3\left(mol\right)\)
Bảo toàn Al: \(n_{Al\left(X\right)}=a+2c+ak+2ck=0,9\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{Fe_3O_4}=\dfrac{0,3.232}{0,3.232+0,9.27}.100\%=74,12\%\\\%m_{Al}=\dfrac{0,9.27}{0,3.232+0,9.27}.100\%=25,88\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hỗn hợp X gồm Al và Fe2O3. Lấy 85,6 gam X đem nung nóng để thực hiện phản ứng nhiệt nhôm, sau một thời gian thu được m gam chất rắn Y. Chia Y làm 2 phần bằng nhau: Phần 1: Hòa tan trong dung dịch NaOH dư thấy thoát ra 3,36 lít khí (đktc) và còn lại m1 gam chất không tan. Phần 2: Hòa tan hết trong dung dịch HC1 thấy thoát ra 10,08 lít khí (đktc). Thành phần chất rắn Y gồm các chất là? A. Al, Fe2O3, Fe, Al2O3 B. Al, Fe, Al2O3 C. Fe, Al2O3 D. Cả A, C đúng.
Đọc tiếp
Hỗn hợp X gồm Al và Fe2O3. Lấy 85,6 gam X đem nung nóng để thực hiện phản ứng nhiệt nhôm, sau một thời gian thu được m gam chất rắn Y. Chia Y làm 2 phần bằng nhau:
Phần 1: Hòa tan trong dung dịch NaOH dư thấy thoát ra 3,36 lít khí (đktc) và còn lại m1 gam chất không tan.
Phần 2: Hòa tan hết trong dung dịch HC1 thấy thoát ra 10,08 lít khí (đktc). Thành phần chất rắn Y gồm các chất là?
A. Al, Fe2O3, Fe, Al2O3
B. Al, Fe, Al2O3
C. Fe, Al2O3
D. Cả A, C đúng.
Đáp án A
2 Al + Fe 2 O 3 → t o Al 2 O 3 + 2 Fe
Vì chia hỗn hợp Y thành hai phần bằng nhau nên số mol mỗi chất trong hai phần đều bằng nhau.
Vì phần 1 tác dụng với dung dịch NaOH có xuất hiện khí nên Y có Al.
Do đó Y có Al, Fe, A12O3 và có thể có Fe2O3.

Đúng 0
Bình luận (0)