trộn 200g dung dịch Na2CO3 13,25% vào 300g dung dịch BaCl2 20,8%
Tính nồng độ % của dung dịch sau khi phản ứng. Biết :
Na2CO3 + BaCl2 -> 2NaCl + BaCl
trộn 200g dung dịch Na2CO3 13,25% vào 300g dung dịch BaCl2 20,8%
a, Chất nào hết? Chất nào dư?
b, Tính nồng độ % của dung dịch sau khi phản ứng. Biết BaCO3 kết tủa
Trộn 200g dung dịch Na2Co3 13,25% vào 350g dung dịch BaCl2 20,8%
a)Chất nào còn dư
b)Tính C% dung dịch sau phản ứng
Ta có :
nNa2CO3=200.13,25%\106=0,25(mol)
nBaCl2=350.20,8%\208=0,35(mol)
Na2CO3+BaCl2→BaCO3+2NaCl
Ta thấy : nNa2CO3=0,25<nBaCl2=0,35
nên BaCl2dư
Theo phương trình , có :
nBaCl2(pư)=nBaCO3=nNa2CO3=0,25(mol)
nNaCl=2nNa2CO3=0,25.2=0,5(mol)
⇒nBaCl2(dư)=0,35−0,25=0,1(mol)
Sau phản ứng,
mdd=ndd Na2CO3+mdd BaCl2−mBaCO3
=200+350−0,25.197=500,75(gam)
Vậy :
C%BaCl2(dư)=0,1.208\500,75.100%=4,15%
C%NaCl=0,5.58,5\500,75.100%=5,84%
%tk
trộn 100g dung dịch chứa muối sunfat của kim loại kiềm nồng độ 13,2% với 100g dung dịch NaHCO3 4,2%..sau phản ứng thu được dung dịch A có khối lượng là m gam (m<200g)..cho 100g dung dịch BaCl2 20,8% vào dung dịch A ,, sau khi phản ứng xong vẫn thấy dư dung dịch muối sunfat .. lại thêm 20g dung dịch BaCl2 20,8% nữa thì lại dư BaCl2 và lúc này được dung dịch D..hãy xác định công thức hóa học muối sunfat của kim loại kiềm ban đầu
. Do trộn 100g với 100g mà lượng dung dịch thu được < 200g thì muối sunfat kim loại là muối axit.( do sự thất thoát khí )
pt : 2MHSO4 + 2NaHCO3 = M2SO4 + Na2SO4 + 2CO2 + 2H2O
Sự thoát khí CO2 làm giảm khối lượng ( số mol CO2 = số mol NaHCO3 0,05mol)
gọi số mol của MHSO4 là x ta có:
(M + 97) x = 13,2 => x = 13,2/ (M + 97)
Theo phương trình sự tạo kết tủa với BaCl2 là muối sunfat:
MNaSO4 + BaCl2 = BaSO4 + MCl + NaCl
=> Với 0,1 < x < 0,1 + 0,02 thì 13< M < 35 thoả mãn Na = 23 Vậy công thức sunfat là NaHSO4
Câu 1. Cho 50 gam dung dịch BaCl2 20,8 % vào 100 gam dung dịch Na2CO3, lọc bỏ kết tủa được dung dịch X. Tiếp tục cho 50 gam dung dịch H2SO4 9,8% vào dung dịch X thấy ra 0,448 lít khí (đktc). Biết các phản ứng xảy ra hoàn toàn. Nồng độ % của dung dịch Na2CO3 và khối lượng dung dịch thu được sau cùng là:
A. 8,15% và 198,27 gam. B. 7,42% và 189,27 gam.
C. 6,65% và 212,5 gam. D. 7,42% và 286,72 gam
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m < 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn.
a) Xác định công thức muối sunfat của kim loại kiềm ban đầu.
b) Tính nồng độ % của các chất tan trong dung dịch A.
c) Dung dịch muối sunfat của kim loại kiềm ban đầu có thể tác dụng được với các chất nào sau đây: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Ag, Fe, CuS, Fe(NO3)2? Viết phương trình hóa học của các phản ứng xảy ra.
a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
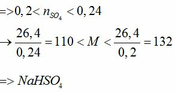
b)
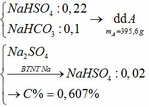
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O
Trộn 400ml Na2CO3 1M với 600ml dung dịch HCl, phản ứng vừa đủ. Phản ứng theo sơ đồ: Na2CO3 + 2HCl → 2NaCl + CO2 + H2O a, Tính nồng độ CM của dung dịch HCl b, Tính khối lượng NaCl và thể tích khí CO2 sinh ra (đktc) c, Tính nồng độ CM của dung dịch thu được (coi Vdd thu được là tổng thế tích 2 dung dịch trên)
Ta có: \(n_{Na_2CO_3}=0,4.1=0,4\left(mol\right)\)
PT: \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
a, \(n_{HCl}=2n_{Na_2CO_3}=0,8\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,8}{0,6}=\dfrac{4}{3}\left(M\right)\)
b, \(n_{NaCl}=2n_{Na_2CO_3}=0,8\left(mol\right)\Rightarrow m_{NaCl}=0,8.58,5=46,8\left(g\right)\)
\(n_{CO_2}=n_{Na_2CO_3}=0,4\left(mol\right)\Rightarrow V_{CO_2}=0,4.24,79=9,916\left(l\right)\)
c, \(C_{M_{NaCl}}=\dfrac{0,8}{0,4+0,6}=0,8\left(M\right)\)
Trộn 100 gam dung dịch H2SO4 19,6% với 300 gam dung dịch BaCl2 20,8% thu được m gam kết tủa
và dung dịch Y.
1.Viết phương trình phản ứng? Tính m?
2.Tính nồng độ % của mỗi chất trong dung dịch Y?
\(\begin{cases} m_{H_2SO_4}=\dfrac{100.19,6\%}{100\%}=19,6(g)\\ m_{BaCl_2}=\dfrac{300.20,8\%}{100\%}=62,4(g) \end{cases} \Rightarrow \begin{cases} n_{H_2SO_4}=\dfrac{19,6}{98}=0,2(mol)\\ n_{BaCl_2}=\dfrac{62,4}{208}=0,3(mol) \end{cases}\\ a,PTHH:BaCl_2+H_2SO_4\to BaSO_4\downarrow +2HCl\)
Vì \(\dfrac{n_{H_2SO_4}}{1}<\dfrac{n_{BaCl_2}}{1}\) nên \(BaCl_2\) dư
\(\Rightarrow n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{BaSO_4}=0,2.233=46,6(g)\)
\(b,n_{HCl}=n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{CT_{HCl}}=0,2.36,5=7,3(g)\\ m_{dd_{HCl}}=100+300-46,6=353,4(g)\\ \Rightarrow C\%_{HCl}=\dfrac{7,3}{353,4}.100\%\approx 2,07\%\)
trộn 300ml dung dịch hỗn hợp gồm Na2CO3 0,1M và NaHCO3 0,15M với 250ml dung dịch BaCl2 0,1M. Sau phản ứng thu được m gam kết tủa và dung dịch X
a. Tính m?
b. Cho từ 200ml dung dịch H2SO4 0,1M vào dung dịch X. Sau phản ứng hoàn toàn thu được Vlít khí (đo ở đktc). Tính V?
mong mọi người lm nhanh giúp mik vs ạ
Cho các cặp chất sau: Cu và dung dịch FeCl3, dung dịch CuSO4 và H2S, dung dịch FeCl2 và H2S, dung dịch FeCl3 và H2S, dung dịch Fe(NO3)2 và HCl, dung dịch BaCl2 và dung dịch NaHCO3, dung dịch KHSO4 và dung dịch Na2CO3. Số cặp chất xảy ra phản ứng khi trộn lẫn vào nhau là:
A. 7
B. 4
C. 5
D. 6