đốt cháy hoàn toàn 2,3g A bằng khí oxi.sau phản ứng thu được 2,24 lít khí CO2(đktc) và 2,7g H2O.Hỏi A được cấu tạo từ những nguyên tố nào?Tính khối lượng của từng nguyên tố trong 2,3 g hợp chất A
giải giùm mk vs ạ
Đốt cháy hoàn toàn 2,3 gam X bằng khí oxi, sau phản ứng thu được 2,24 lít C O 2 đktc và 2,7 gam nước. Hỏi A được cấu tạo từ những nguyên tố hóa học nào. Tính khối lượng từng nguyên tố trong 2,3 gam X.
Vì A cháy sinh ra C O 2 và H 2 O nên A chứa C, H, và có thể có O.
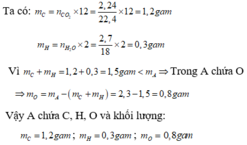
Đốt cháy hoàn toàn 2,3 gam A bằng khí Oxi sau phản ứng thu hồi được 2,42 lít khí CO2 ở điều kiện tiêu chuẩn và 2,7 gam nước Hỏi a được cấu tạo từ nguyên tử nào tính khối lượng nguyên tố trong 2,3 g hợp chất A
Đốt cháy hoàn toàn 2,3 gam A bằng khí Oxi sau phản ứng thu hồi được 24,2 lít khí CO2 ở điều kiện tiêu chuẩn và 2,7 gam nước Hỏi a được cấu tạo từ nguyên tử nào tính khối lượng nguyên tố trong 2,3 g hợp chất A
PTHH: A + O2 ---> CO2 + H2O
Ta có: \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) (Phần nầy mik sửa lại đề nhé.)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\)
Ta lại có:
\(m_{O_{\left(CO_2\right)}}=0,1.16.2=3,2\left(g\right)\)
\(m_{O_{\left(H_2O\right)}}=0,15.16=2,4\left(g\right)\)
Áp dụng định luật bảo toàn khối lượng, ta được:
\(m_{O_2}=2,7+\left(0,1.44\right)-2,3=4,8\left(g\right)\)
Ta thấy:
\(m_{O_{\left(VPhải\right)}}=2,4+3,2=5,6\left(g\right)\)
\(m_{O_2}=4,8\left(g\right)\)
Ta lại thấy: 5,6 > 4,8
Vậy trong A có: C, H và O
Gọi CTHH của A là: CxHyOz
Ta có: \(m_{C_{\left(CO_2\right)}}=m_{C_{\left(A\right)}}=0,1.12=1,2\left(g\right)\)
\(m_{H_{\left(H_2O\right)}}=m_{H_{\left(A\right)}}=0,15.1.2=0,3\left(g\right)\)
\(m_{O_{\left(A\right)}}=5,6-4,8=0,8\left(g\right)\)
=> \(x:y:z=\dfrac{1,2}{12}:\dfrac{0,3}{1}:\dfrac{0,8}{16}=0,1:0,3:0,05=2:6:1\)
Vậy CTHH của A là: C2H6O
Đốt cháy hoàn toàn 2,3 gam một hợp chất bằng khí oxi, sau phản ứng thu được 2,24 lít CO2 (dktc) và 2,7 gam H2O.
a: Xác định thành phần định tính các nguyên tố trong hợp chất.
b: Tính khối lượng từng nguyên tố trong 2,3 gam hợp chất
Bài 7: Đốt cháy hoàn toàn 3,2 gam hợp chất A cần 8,96 lít khí O2 (đktc) thu được khí CO2 và H2O theo tỉ lệ mol là 1:2.
a. Tính khối lượng của từng nguyên tố trong hợp chất A.
b. Xác định CTPT của hợp chất A biết M = 16.
a)
Do \(\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1}{2}\)
=> \(\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
Giả sử A có CTHH là CxH4xOy
Gọi số mol của A là a (mol)
=> 12ax + 4ax + 16ay = 3,2
=> ax + ay = 0,2 (1)
Bảo toàn C: nCO2 = ax (mol)
Bảo toàn H: nH2O = 2ax (mol)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn O: \(ay+0,4.2=2ax+2ax\)
=> 4ax - ay = 0,8 (2)
(1)(2) => ax = 0,2 (mol); ay = 0 (mol)
=> A chỉ chứa C và H
\(\left\{{}\begin{matrix}n_C=ax\left(mol\right)\\n_H=4ax\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_C=12.ax=2,4\left(g\right)\\m_H=1.4ax=0,8\left(g\right)\end{matrix}\right.\)
b)
Xét \(\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
=> CTPT: (CH4)n
Mà M = 16 g/mol
=> n = 1
=> CTPT: CH4
Đề 15:
1) Nguyên tử Y nặng gấp hai lần nguyên tử Canxi. Tính nguyên tử khối của Y và cho biết Y thuộc nguyên tố nào ? Viết kí hiệu hóa học của nguyên tố đó.
2) Thế nào là đơn chất ? Cố những loại đơn chất nào ? Cho VD. Nêu đặc điểm cấu tạo của đơn chất ?
3) Thế nào là khối lượng mol ? Tính khối lượng mol của:
a) Khí metan biết phan tử gồm 2C và 4H.
b) khí sunfua biết phân tử gồm 2H và 1S.
4) Đốt cháy m gam kim loại ngôm trong không khí cần tiêu tốn 9,6g oxi người ta thu được 20,4g nhôm oxit
a) Viết phương trình phản ứng
b) Tìm khối lượng
Đề 16:
1) Hòa tan hoàn toàn 5,6g sắ ( Fe) vào dung dịch Axit clohidric ( HCl ) thu được sắt ( II ) clorua ( FeCl2 ) và khí Hidro ( H2)
a) Tính khối lượng của FeCl2 tạo thành sau phản ứng ?
b) Tính thể tích khí Hidro ( ở đktc ) tạo thành sau phản ứng ?
2) Để đốt cháy 16g chất X cần dùng 44,8 lít oxi ( ở đktc ) Thu được khí Co2 vào hơi nước theo tỉ lệ số mol 1:2. Tính khối lượng khí CO2 và hơi nước tạo thành ?
3) Thế nào là nguyên tử khối ? Tính khối lượng bằng nguyên tử cacbon của 5C, 11Na, 8Mg
4)Nguyên tử X nặng gấp 1,25 lần nguyên tử oxi. Tính nguyên tử khối của X và cho biết X thuộc nguyên tố nào? Viết kí hiệu hóa học của nguyên tố đó.
5) Hãy so sánh xem nguyên tử oxi nặng hay nhẹ hơn, bằng bao nhiêu lần so với :
a) Nguyên tử đồng
b) Nguyên tử C
6) Cho 5,6g sắt tác dụng hết với dung dịch axit clohidric ( HCl). Sau phản ứng thu được 12,7g sắt (II) clorua ( FeCl2) và 0,2g khí hidro ( đktc)
a) Lập PTHH của phản ứng trên.
b) Viết phương trình khối lượng của Phản ứng đã xảy ra
c) Tính khối lượng của axit sunfuric đã phản ứng theo 2 cách
Đề 15:
1) Theo đề bài , ta có:
NTK(Y)= 2.NTK(Ca)= 2.40=80 (đvC)
=> Nguyên tố Y là brom, KHHH là Br.
2) - Đơn chất là chất do 1nguyên tố tạo thành.
VD: O3; Br2 ; Cl2;......
- Hợp chất là những chất do 2 hay nhiều nguyên tố hóa học trở lên tạo thành.
VD: NaCl, KMnO4, CuSO4, H2O;....
3) Khôi lượng mol? tự trả lời đi !
a) Khối lượng mol của phân tử gồm 2C và 4H
Có nghĩa là khối lượng mol của C2H4
\(M_{C_2H_4}\)= 2.12+4.1=28 (g/mol)
\(M_{H_2S}\)=2.1+32=34(g/mol)
Bài 7: Đốt cháy hoàn toàn a g một hợp chất A thu được 4.4g khí cacboniic và 1.8g
nước.
a. A có thể có những nguyên tố nào?
b. Biết rằng khối lượng oxi đã tham gia phản ứng là 3.2g. Hãy tính tỉ lệ số nguyên tử
các nguyên tố trong phân tử hợp chất A.
giúp mình với🙏
Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X (chứa C, H, O) bằng lượng O2 vừa đủ, sau phản ứng tạo ra 10,752 lít khí CO2 (đo ở đkc) và 0,6 mol H2O. Biết tỉ khối hơi của X so với khí hiđro bằng 45. Tính khối lượng từng nguyên tố có trong 10,8 gam X. Tìm công thức phân tử của X
Đốt cháy hoàn toàn 2.25 gam một chất hữu cơ X thu được 3.36 lít khí co2(đo ở đktc) và 4.05 gam h2o
a)Chất X có những nguyên tố nào?
b)xác định công thức phân tử và viết công thức cấu tạo của X.Biết khối lượng mol của X nhỏ hơn 40gam/mol
a) Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{4,05}{18}=0,45\left(mol\right)\)
Xét mC + mH = 0,15.12 + 0,45 = 2,25 (g)
=> X gồm C và H
b, CTPT của X có dạng CxHy
=> x : y = 0,15 : 0,45 = 1 : 3
=> (CH3)n < 40
=> n = 2
CTPT: C2H6
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{3,36}{22,4}=0,15mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{4,05}{18}=0,45mol\)
\(n_O=\dfrac{2,25-\left(0,15.12+0,45.1\right)}{16}=0mol\)
=> X chỉ có C và H
\(CTHH:C_xH_y\)
\(\rightarrow x:y=0,15:0,45=1:3\)
\(\rightarrow CTPT:CH_3\)
\(CTĐG:\left(CH_3\right)n< 40\)
\(\rightarrow n=1;2\)
\(n=1\rightarrow CTPT:CH_3\left(loại\right)\)
\(n=2\rightarrow CTPT:C_2H_6\left(nhận\right)\)
\(CTCT:CH_3-CH_3\)
\(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
=> X gồm có nguyên tố C , H.
\(nCO_2=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
=> nC = 0,15(mol)
mC = 0,15 .12 = 1,8(g)
\(nH_2O=\dfrac{4,05}{18}=0,225\left(mol\right)\)
=> nH = 0,225 . 2 = 0,45(mol)
mH = 0,45 . 1 = 0,45 (g)
Vì mH + mC = 1,8 + 0,45 = 2,25 (g) = mX
=> X không có nguyên tố O.
Gọi CTHH đơn giản của X là CxHy
ta có : x : y = 0,15 : 0,45 = 1 : 3
=> CTHH đơn giản của X là CH3
ta có:
(CH3)n < 40
=> n = 2
=> CTPT của X là C2H6
CTCT của X là CH3 - CH3