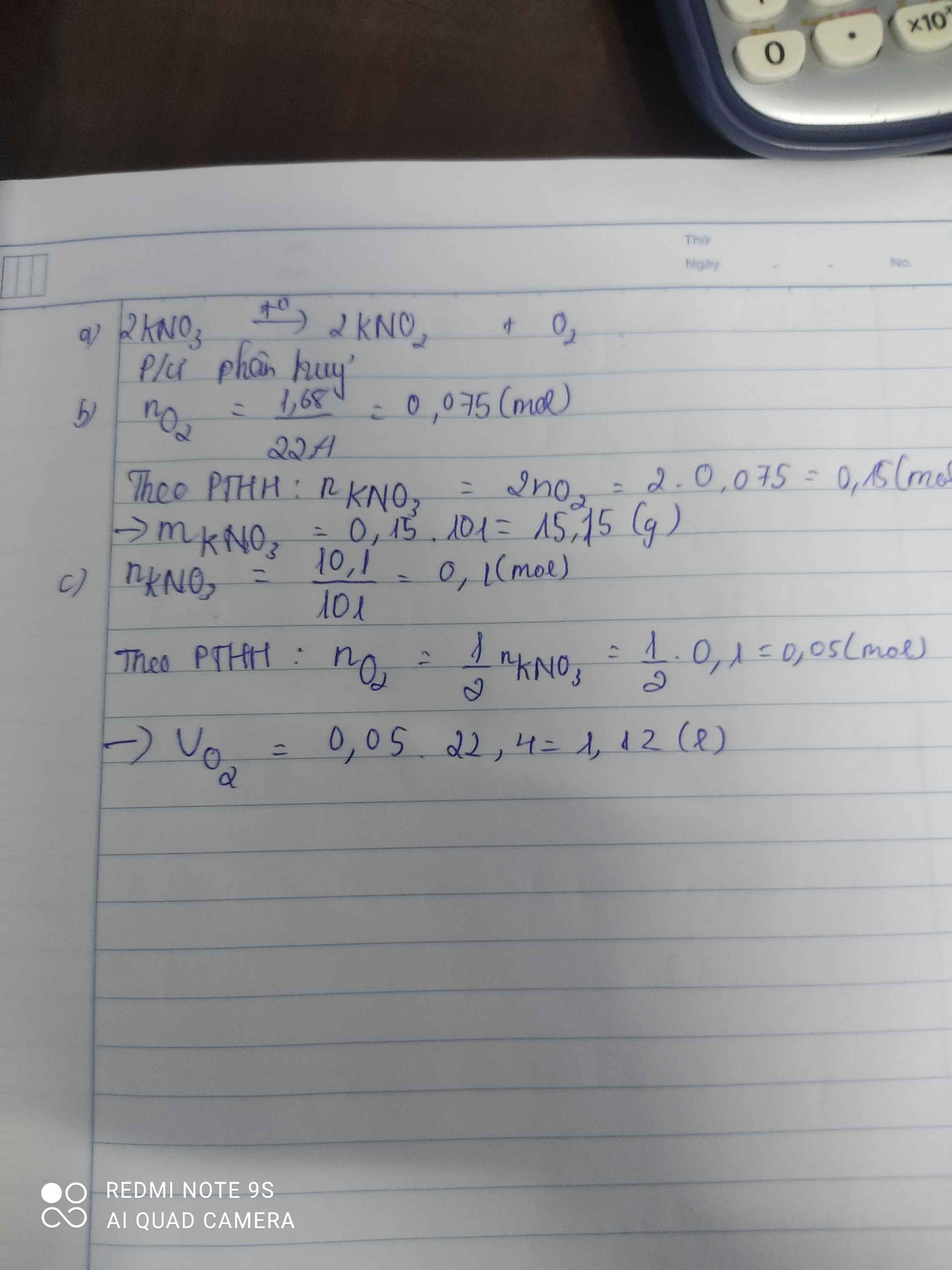Cho sơ đồ phản ứng sau: K + H2O --> KOH + H2
Khối lượng kali cần dùng để điều chế được 2,24 lít H2 (đktc) là (Cho K=39)

Những câu hỏi liên quan
Cho sơ đồ phản ứng sau : KClO3——-> KCl + O2 a, hãy hoàn thành phương trình phản ứng b, Tính số mol và khối lượng Kaliclorat (KClO3) cần dùng để điều chế 11,2 lít khí oxi(O2) (đktc) ( biết : K = 39, Cl= 35,5 ,O=16)
\(n_{O_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ PTHH:2KClO_3-^{t^o}>2KCl+3O_2\)
tỉ lệ 2 : 2 : 3
n(mol) `1/3`<------------`1/3`<-----`0,5`
\(m_{KClO_3}=n\cdot M=\dfrac{1}{3}\cdot\left(39+35,5+16\cdot3\right)\approx40,83\left(g\right)\)
Đúng 3
Bình luận (0)
Nung nóng ( kali nitrat )KNO3 tạo thành KNO2 ( Kali nitrit) và khí O2 a) Viết PTHH cho biết thuộc loại phản ứng nào. b) Tính lượng KNO3 cần dùng để điều chế được 1,68 lít O2 ở đktc biết H = 85% c) Tính VO2 ở đktc điều chế được khi phân hủy 10,1 gam KNO3 biết H = 80%
a) \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
Phản ứng phân hủy
b) \(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
PTHH: 2KNO3 --to--> 2KNO2 + O2
0,15<--------------------0,075
=> \(m_{KNO_3\left(PTHH\right)}=0,15.101=15,15\left(g\right)\)
=> mKNO3 (thực tế) = \(\dfrac{15,15.100}{85}=17,824\left(g\right)\)
c) \(n_{KNO_3\left(pư\right)}=\dfrac{10,1.80\%}{101}=0,08\left(mol\right)\)
=> nO2 = 0,04 (mol)
=> VO2 = 0,04.22,4 = 0,896(l)
Đúng 4
Bình luận (0)
Cho 3,9g Kali (K) tác dụng với nước, sau phản ứng thu được kali hiđroxit (KOH) và khí hiđro (H2).
a. Viết phương trình hóa học
b. Tính khối lượng kali hiđroxit (KOH) tạo thành
c. Tính thể tích hiđro (H2) sinh ra ở đktc
(K=39, H=1, O=16)
\(n_K=\dfrac{3,9}{39}=0,1mol\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
0,1 0,1 0,05 ( mol )
\(m_{KOH}=0,1.56=5,6g\)
\(V_{H_2}=0,05.22,4=1,12l\)
Đúng 4
Bình luận (1)
2K+2H2O->2KOH+H2
0,1-----------------0,1---0,05
n K=0,1 mol
=>m KOH=0,1.56=5,6g
VH2=0,05.22,4=1,12l
Đúng 2
Bình luận (1)
Cho 3,9g Kali (K) tác dụng với nước, sau phản ứng thu được kali hiđroxit (KOH) và khí hiđro (H2).( ở đktc)
a. Viết phương trình hóa học
b. Tính khối lượng kali hiđroxit (KOH) tạo thành ( cho biết nguyên tử khối các nguyên tố:CU=64;O=16;H=1;K=39)
Giúp mik vs ạ mik cần gấp
C.ơn
a, \(2K+2H_2O\rightarrow2KOH+H_2\)
b, \(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
Theo PT: \(n_{KOH}=n_K=0,1\left(mol\right)\Rightarrow m_{KOH}=0,1.56=5,6\left(g\right)\)
Đúng 1
Bình luận (0)
\(n_K=\dfrac{m}{M}=\dfrac{3,9}{39}=0,1\left(mol\right)\\ PTHH:2K+2H_2O->2KOH+H_2\)
tỉ lệ 2 : 2 : 2 ; 1
n(mol) 0,1---.0,1------>0,1------>0,05
\(m_{KOH}=n\cdot M=0,1\cdot\left(39+16+1\right)=5,6\left(g\right)\)
Đúng 1
Bình luận (0)
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi. a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này. b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
Đọc tiếp
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi.
a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này.
b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.
c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
2KClO3-to\xt->2KCl+3O2
0,1------------------0,1
n KClO3=\(\dfrac{12,25}{122,5}\)=0,1 mol
=>m KCl=0,1.74,5=7,45g
H=\(\dfrac{6,8}{7,45}.100\)=91,275%
b)
2KClO3-to\xt->2KCl+3O2
0,2-------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
H=85%
=>m KClO3=0,2.122,5.\(\dfrac{100}{85}\)=28,82g
c)
2KClO3-to\xt->2KCl+3O2
0,2------------------------0,3
n KClO3=\(\dfrac{24,5}{122,5}\)=0,2 mol
H=80%
=>m O2=0,3.32.\(\dfrac{80}{100}\)=10,4g
Đúng 3
Bình luận (0)
Cho sơ đồ phản ứng sau: Fe + O2 --->Fe3O4
Thể tích khí oxi (ở đktc) cần dùng để điều chế được 37,12g Fe3O4 là bao nhiêu?
\(PTHH:Fe+O_2\) → \(Fe_3O_4\)
Cân bằng: \(3Fe+2O_2\) → \(Fe_3O_4\)
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{37,12}{232}=0,16\left(mol\right)\)
\(n_{O_2}=2.n_{Fe_3O_4}=2.0,16=0,32\left(mol\right)\)
\(V_{O_2\left(đktc\right)}=n.22,4=0,32.22,4=7,168\left(l\right)\)
Đúng 1
Bình luận (0)
1.Đốt cháy 6,2g photpho trong bình chứa 6,4g oxi. Sau phản ứng hoàn toàn,chất nào còn dư? (P=31,O=16) * Oxi Hai chất đều dư Hai chất phản ứng vừa đủ Photpho
2.Số gam KMnO4 cần dùng để đièu chế được 2,24 lít khí oxi (đktc) là: (K=39,Mn=55,O=16) * 31,6 gam 20,7 gam 40,8 gam 14,3 gam
nP= 6,2 : 31 = 0,2 (MOL)
nO2 = 6,4 : 32= 0,2 (mol)
pthh : 4P+5O2 -t--> 2P2O5
LTL
0,2/4 > 0,2/5
=> P du
2
nO2 = 2,24 : 22,4 =0,1 (mol)
pthh : KMnO4 -t-> K2MnO4 + MnO2 + O2
0,2 <-------------------------------0,1 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g)
Đúng 0
Bình luận (1)
1, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: 4P+5O2 \(\underrightarrow{t^o}\) 2P2O5
Vì \(\dfrac{0,2}{4}>\dfrac{0,2}{5}\) nên P dư, Oxi hết
2,\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH : 2KMnO4 \(\underrightarrow{t^o}\) K2MnO4 + MnO2 + O2
0,2 0,1 (mol)
\(m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 37,6g K2O tác dụng hoàn toàn với 500ml H2O. Sau phản ứng thua được sản phẩm là KOH
a) Tính khối lượng KOH thu được sau phản ứng ?
b) Tính nồng độ mol/1Cm của dung dịch KOH thu được ?
c) Tính thể tích Oxygen cần dùng để điều chế ra lượng K2O nói trên ?
a) \(n_{K_2O}=\dfrac{37,6}{94}=0,4\left(mol\right)\)
PTHH: K2O + H2O --> 2KOH
0,4------------>0,8
=> mKOH = 0,8.56 = 44,8 (g)
b) \(C_M=\dfrac{0,8}{0,5}=1,6M\)
c)
PTHH: 4K + O2 --to--> 2K2O
0,2<----0,4
=> VO2 = 0,2.22,4 = 4,48 (l)
Đúng 1
Bình luận (2)
nKK 2O = 37,6\94 = 0,4 mol
K2O+H2O --> 2KOH
0,4 0,4 0,8 ( mol )
mKOH= 0,8.56=44,8g
CMMKOH = 0,80,50,80,5 = 1,6M
c.
4K+O2 --to> 2K2O
0,4 0,1 ( mol )
VO2 = 0,1.22,4=2,24lít
Đúng 1
Bình luận (0)
Số gam KMnO4 cần dùng để điều chế được 2,24 lít khí oxi (đktc) là (K = 39, Mn = 55, O = 16) A. 20,7g B. 42,8g C. 14,3g D. 31,6g
Ko cần giải thích học ngu lắm :))
\(pthh:2KMnO_4\overset{t^o}{--->}K_2MnO_4+MnO_2+O_2\uparrow\)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo pt: \(n_{KMnO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
Chọn D
Đúng 1
Bình luận (0)