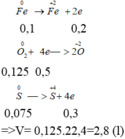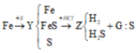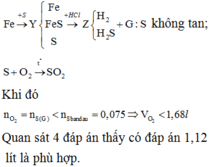Trong giờ thực hành, bạn lan thực hiện các thí nghiệm sau
TN1) Trộn 5.6g sắt với 3,2g lưu huỳnh rồi nung nóng thu được chất rắn duy nhất là sắt sunfat
TN2) Bạn Lan trộn 39,2g sắt với 16g lưu huỳnh rồi nugn nóng trên thu được chất rắn X. Tính khối lượng từng chất trong hợp chất