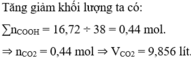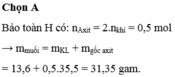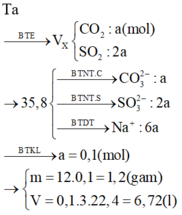Những câu hỏi liên quan
Cho V lít khí clo (đktc) tác dụng với 0,56 gam sắt vừa đủ ở nhiệt độ thích hợp. Sau phản ứng thu được m gam muối. Tính V và m.
\(n_{Fe}=\dfrac{0,56}{56}=0,01\left(mol\right)\)
PTHH: 2Fe + 3Cl2 --to--> 2FeCl3
0,01-->0,015----->0,01
=> V = 0,015.22,4 = 0,336 (l)
mFeCl3 = 0,01.162,5 = 1,625 (g)
Đúng 6
Bình luận (0)
Cho m gam hỗn hợp gốm axit axetic và axit oxalic tác dụng vừa đủ với KHCO3, sau phản ứng thu được m + 16,72 gam muối và V lít khí CO2 (đktc). Giá trị của V là
A. 19,712
B. 34,048
C. 9,856
D. 17,024
Cho m gam hỗn hợp gốm axit axetic và axit oxalic tác dụng vừa đủ với KHCO3, sau phản ứng thu được m + 16,72 gam muối và V lít khí CO2 (đktc). Giá trị của V là
A. 19,712.
B. 34,048.
C. 9,856.
D. 17,024.
Đáp án C
Tăng giảm khối lượng ta có:
∑nCOOH = 16,72 ÷ 38 = 0,44 mol.
⇒ nCO2 = 0,44 mol ⇒ VCO2 = 9,856 lít
Đúng 0
Bình luận (0)
Câu 14: Cho 11,9 gam hỗn hợp gồm Al, Mg ,Fe tác dụng vừa đủ V lít dd HNO3 1M.Sau phản ứng thu được 6,72lit (đkc) gồm NO & N2 có dhh/H2 = 43/3 và dd X trong đó có 0,05mol NH4NO3.Cô cạn dd X được m gam muối khan. Giá trị V& m lần lượt là
A. 3,3lit , 183,3 gam
B. 3,1lit ,120,3gam
C.3,3lit, 178,8gam
D.3,25lit, 183,3gam
Có; \(n_{NO}+n_{N_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(\dfrac{30n_{NO}+28n_{N_2}}{n_{NO}+n_{N_2}}=\dfrac{43}{3}.2=\dfrac{86}{3}\)
=> nNO = 0,1 (mol); nN2 = 0,2(mol)
Al0 -3e --> Al+3
a-->3a--->a
Mg0 -2e --> Mg+2
b---->2b---->b
Fe0 -3e --> Fe+3
c--->3c---->c
4H+ + NO3- +3e --> NO + 2H2O
0,4<----------0,3<----0,1
12H+ + 2NO3- +10e--> N2 + 6H2O
2,4<---------------2<-----0,2
10H+ + 2NO3- +8e--> NH4NO3 + 3H2O
0,5<-------------0,4<-----0,05
=> nHNO3 = nH+ = 0,4 + 2,4 + 0,5 = 3,3 (mol)
=> \(V_{dd}=\dfrac{3,3}{1}=3,3\left(l\right)\)
Bảo toàn H: \(n_{H\left(HNO_3\right)}=n_{H\left(NH_4NO_3\right)}+n_{H\left(H_2O\right)}\)
=> 3,3 = 4.0,05 + 2.nH2O
=> nH2O = 1,55(mol)
Theo ĐLBTKL:
\(m_{hh\left(bd\right)}+m_{HNO_3}=m_{muoi}+m_{NH_4NO_3}+m_{NO}+m_{N_2}+m_{H_2O}\)
=> hh muỗi khan = \(m_{muoi}+m_{NH_4NO_3}=11,9+3,3.63-30.0,1-28.0,2-18.1,55=183,3\left(g\right)\)
=> A
Đúng 3
Bình luận (0)
Đặt \(n_{NO}=a(mol);n_{N_2}=b(mol)\)
\(\Rightarrow \begin{cases} a+b=\dfrac{6,72}{22,4}=0,3(mol)\\ \dfrac{30a+28b}{a+b}=2.\dfrac{43}{3}=\dfrac{86}{3} \end{cases}\Rightarrow \begin{cases} a=0,1(mol)\\ b=0,2(mol) \end{cases}\\ \Rightarrow \Sigma n_{HNO_3}=4n_{NO}+12n_{N_2}+10n_{NH_4NO_3}=3,3(mol)\\ \Rightarrow V_{dd_{HNO_3}}=\dfrac{3,3}{1}=3,3(l)\\ n_{NO_3-(muối)}=3n_{NO}+10n_{N_2}+8n_{NH_4NO_3}=2,7(mol)\\ \Rightarrow m_{muối}=m_{NO_3-(muối)}+m_{KL}+m_{NH_4NO_3}=2,7.62+11,9+0,05.80=183,3(g) \)
Chọn A
Đúng 2
Bình luận (2)
Cho 13,6g hỗn hợp Fe và Cr tác dụng hết với dung dịch HCl nóng thấy có 5,6 lít khí H 2 thoát ra (đktc). Đem cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị m là
A. 31,35.
B. 31,75.
C. 22,48.
D. 22,45.
Cho 5,4 gam Al tác dụng vừa đủ với 150ml dung dịch HCl aM. Sau phản ứng thu được m gam muối khan và V lít H2(đktc).
a. Giá trị của a là:
A. 3M B. 4M C. 1,5M D. 2,5M
b. Khối lượng muối khan m là:
A. 26,7g B. 15,45g C. 22,1g D. 18,4g
c. Thể tích khí H2 (V) là:
A. 13,44l B. 2,24l C. 6,72l D. 3,36l
Đọc tiếp
Cho 5,4 gam Al tác dụng vừa đủ với 150ml dung dịch HCl aM. Sau phản ứng thu được m gam muối khan và V lít H2(đktc). a. Giá trị của a là: A. 3M B. 4M C. 1,5M D. 2,5M b. Khối lượng muối khan m là: A. 26,7g B. 15,45g C. 22,1g D. 18,4g c. Thể tích khí H2 (V) là: A. 13,44l B. 2,24l C. 6,72l D. 3,36l
\(\text{Ta có PTHH}\\2Al+6HCl \rightarrow 2AlCl_3+3H_2 \uparrow\\n_{Al}=\dfrac{5,4}{27}=0,2(mol)\\\Rightarrow n_{HCl}=3n_{Al}=0,6(mol)\\\Rightarrow C_{M_{HCl}}=n/V=\dfrac{0,6}{0,15}=4(M)\\\text{ Câu hỏi 1 : B}\\\Rightarrow n_{AlCl_3}=n_{Al}=0,2(mol)\\\Rightarrow m_{AlCl_3} = 0,2.133,5=26,7(gam)\\\text{ Câu hỏi 2 : A}\\\Rightarrow n_{H_2}=3/2n_{Al}=0,3(mol)\Rightarrow V_{H_2}(đktc)=0,3.22,4=6,72(lít)\\\text{ Câu hỏi 3 : C} \)
Đúng 1
Bình luận (0)
Cho m gam cacbon tác dụng hết với dung dịch H2SO4 đặc, nóng thu được V lít ở đktc hỗn hợp khí X gồm CO2 và SO2 .Hấp thụ hết X bằng dung dịch NaOH vừa đủ thu được dung dịch Y chỉ chứa hai muối trung hòa. Cô cạn dung dịch Y thu được 35,8 gam muối khan. Giá trị của m và V lần lượt là : A. 2,4 và 6,72 B. 2,4 và 4,48 C. 1,2 và 22,4 D. 1,2 và 6,72
Đọc tiếp
Cho m gam cacbon tác dụng hết với dung dịch H2SO4 đặc, nóng thu được V lít ở đktc hỗn hợp khí X gồm CO2 và SO2 .Hấp thụ hết X bằng dung dịch NaOH vừa đủ thu được dung dịch Y chỉ chứa hai muối trung hòa. Cô cạn dung dịch Y thu được 35,8 gam muối khan. Giá trị của m và V lần lượt là :
A. 2,4 và 6,72
B. 2,4 và 4,48
C. 1,2 và 22,4
D. 1,2 và 6,72
Cho 7,8 gam kali tác dụng với 1 lít dung dịch HCl 0,1M, sau phản ứng thu được dung dịch X và V lít H2 (đktc). Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của V và m lần lượt là A. 2,24 và 7,45. B. 1,12 và 3,725. C. 1,12 và 11,35. D. 2,24 và 13,05.
Đọc tiếp
Cho 7,8 gam kali tác dụng với 1 lít dung dịch HCl 0,1M, sau phản ứng thu được dung dịch X và V lít H2 (đktc). Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của V và m lần lượt là
A. 2,24 và 7,45.
B. 1,12 và 3,725.
C. 1,12 và 11,35.
D. 2,24 và 13,05.
Đáp án D
+ B C P Ư : K ( 0 , 2 m o l ) + H C l ( 0 , 1 m o l ) H 2 O → K + , C l - O H - ⏟ d u n g d ị c h X + H 2 ↑ + B T E : n K = 2 n H 2 B T Đ T c h o X : n K + = n C l - + n O H - ⇒ n H 2 = 0 , 1 n O H - = 0 , 1 ⇒ V H 2 = 2 , 24 l í t m c h ấ t r ắ n = 13 , 05 g a m
Đúng 0
Bình luận (0)
cho 11,2 gam fe tác dụng với HNO3 loãng dư thu được V lít khí NO (đktc). a) tính giá trị của V. b) cô cạn dung dịch thu được sau phản ứng thu được m gam muối. Tính giá trị của m
a) $n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$Fe^0 \to Fe^{+3} + 3e$
$N^{+5} + 3e \to N^{+2}$
Bảo toàn electron : $3n_{Fe} = 3n_{NO}$
$\Rightarrow n_{NO} = 0,2(mol)$
$\Rightarrow V = 0,2.22,4 = 4,48(lít)$
b) $n_{Fe(NO_3)_3} = n_{Fe} = 0,2(mol)$
$\Rightarrow m = 0,2.242 = 48,4(gam)$
Đúng 1
Bình luận (0)