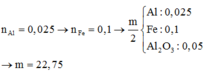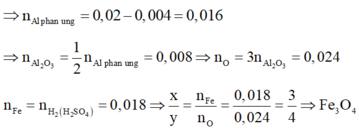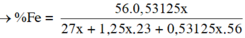Chia 15,57g hỗn hợp gồm Al, Fe, Ag làm 2 phần bằng nhau:
- Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thì được 3,528 lít H2và 3,24g một chất rắn.
- Phần 2: Tác dụng với dung dịch H2SO4 đặc nóng dư.
a. Tính khối lượng mỗi kim loại.
b. Tính thể tích SO2 thu được ở phần 2. (các thể tích đo đktc).