Oxit của một nguyên tố ở 2 mức hóa trị chứa 50% và 60% khối lượng oxi. Tìm nguyên tử khối và viết công thức hóa học của 2 oxit trên

Những câu hỏi liên quan
Oxit của một nguyên tố có hóa trị 2 chứa 20% oxi ( về khối lượng ) Tìm công thức hóa học của oxit đó .?
Oxit của một nguyên tố có hóa trị II chứa 20% oxi về khối lượng. Công thức hóa học của oxit trên là
A.
CuO.
B.
CaO
C.
MgO
D.
FeO
Gọi CTHH là $R_2O_n$
Ta có : $\%O = \dfrac{16n}{2R + 16n}.100\% =2 0\%$
$\Rightarrow R = 32n$
Với n = 2 thì R = 64(Cu)
Vậy Chọn đáp án A
Đúng 1
Bình luận (0)
Oxit của một nguyên tố có hóa trị (II) chứa 20% oxi ( về khối lượng). Công thức hóa học của oxit đó là:
A.CuO. B. FeO. C.CaO. D.ZnO
Tìm công thức đúng.
Công thức hóa học của oxit cần tìm là MO.
Khối lượng mol của MO = M + 16
Và trong 100g MO có 20g oxi.
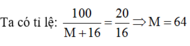
Vậy M là kim loại Cu, công thức hóa học của oxit là CuO.
Đúng 0
Bình luận (0)
. Một nguyên tử X kết hợp với 2 nguyên tử O tạo thành hợp chất oxit. Trong phân tử oxit đó oxi chiếm 50% về khối lượng. Xác định tên của nguyên tố X và công thức hóa học của hợp chất?
Gọi công thức tổng quát là $XH_4$
\(\%H=25\%\\ \Rightarrow \dfrac{4}{X+4}.100\%=25\%\\ \Rightarrow X=12\\ Tên:\ Cacbon\\ CTHH:\ CH_4\)
Đúng 0
Bình luận (0)
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy: a) Tính lượng khí H2 tạo ra ở đktc ? b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ? c) Tính nồng độ của các chất sau phản ứng ?
Đọc tiếp
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.
2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?
3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy:
a) Tính lượng khí H2 tạo ra ở đktc ?
b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ?
c) Tính nồng độ của các chất sau phản ứng ?
1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?
Đúng 1
Bình luận (1)
Hic giúp mình với
Hợp chất khí với hidro của một nguyên tố là RH3. Trong oxit cao nhất của nó có chứa 74,074% oxi về khối lượng. Tìm nguyên tử khối của nguyên tố đó.
a/ Cho biết hóa trị của R với oxi? Viết công thức hợp chất oxit cao nhất của R.
b/ Xác định tên của nguyên tố R.
a)
Do R có hóa trị III trong hợp chất với hidro
=> R có hóa trị V trong oxit cao nhất
Oxit cao nhất của R là: R2O5
b) Có \(\%O=\dfrac{16.5}{2.M_R+16.5}.100\%=74,074\%\)
=> MR = 14
=> R là N(Nitơ)
Đúng 2
Bình luận (0)
Oxit của một nguyên tố có hóa trị II chứa 19,753% oxi (về khối lượng). Công thức hóa học của oxit đó là
A. CuO.
B. FeO.
C. CaO.
D. ZnO.
Oxit của một nguyên tố hóa trị III chứa 0% oxi về khối lượng. Công thức hóa học của oxit đó là :A. Cl2O3B. Fe2O3C. Cr2O3D. Al2O3
Xem chi tiết
Sửa đề : chứa 30% oxi về khối lượng :
Oxit : \(R_2O_3\)
\(\%O = \dfrac{16.3}{2R + 16.3}.100\% = 30\%\\ \Rightarrow R = 56(Fe)\)
Vậy Oxit cần tìm : Fe2O3
Đáp án : B
Đúng 3
Bình luận (3)
a,Oxit của một nguyên tố hóa trị V trong đó có 74,07 % khối lượng là oxi . Tìm công thức hóa học của oxit
b, Một oxit của sắt có 77,78 % khối lượng là Fe và có khối lượng mol bằng 72 g/mol . Tìm CTHH của oxit


























