Tính khối lượng bari sunsat tạo thành khi cho 3,12 gam bariclorua phản ứng với 5,68 gam natri sunfat ?

Những câu hỏi liên quan
Xét thí nghiệm khi cho 208 g Bari clorua BaCl2 tác dụng với 142 g natri sunfat Na2SO4 thì tạo thành bari sunfat BaSO4 và natri clorua NaCl.
a) Viết phương trình chữ của phản ứng này.
b) Viết công thức khối lượng của phản ứng vừa xảy ra.
c) Tổng khối lượng các chất sau phản ứng là bao nhiêu?
d) Nếu thu được 233 g BaSO4, tính khối lượng NaCl thu được.
e) Biết trước khi phản ứng xảy ra có 137 g nguyên tử bari, thì sau phản ứng có bao nhiêu gam nguyên tử bari?
f) Nếu sau khi phản ứng thu được 71 g...
Đọc tiếp
Xét thí nghiệm khi cho 208 g Bari clorua BaCl2 tác dụng với 142 g natri sunfat Na2SO4 thì tạo thành bari sunfat BaSO4 và natri clorua NaCl.
a) Viết phương trình chữ của phản ứng này.
b) Viết công thức khối lượng của phản ứng vừa xảy ra.
c) Tổng khối lượng các chất sau phản ứng là bao nhiêu?
d) Nếu thu được 233 g BaSO4, tính khối lượng NaCl thu được.
e) Biết trước khi phản ứng xảy ra có 137 g nguyên tử bari, thì sau phản ứng có bao nhiêu gam nguyên tử bari?
f) Nếu sau khi phản ứng thu được 71 g nguyên tử clo, thì trước phản ứng đã có bao nhiêu gam nguyên tử clo tham gia phản ứng.
giúp mình nha
a) Bari clorua + Natri sunfat → Bari sunfat + Natri clorua
b) mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
c) Tổng khối lượng các chất sau phản ứng là: 350g
d) mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
⇔208 + 142 = 233 + mNaCl
⇒mNaCl= 117(g)
e) Khi phản ứng xảy ra có 137g nguyên tử Bari, thì sau phản ứng sẽ có 137g nguyên tử Bari.
f) Khi phản ứng thu được 71g nguyên tử Clo, thì trước phản ứng đã có 71g nguyên tử Clo tham gia phản ứng.
Đúng 1
Bình luận (0)
Trong phản ứng hóa học : bari clorua +natri sunphat->bari sunphat + natri clorua. Cho bt khối lượng của natri sunphat (na2so4)là 14,2 gam, khối lượng cua bari sunphat (baso4) và natri clorua (nacl) lân lượt là : 23,3 gam và 11,7 gam. Hãy tính khối lượng của bari clorua bacl2 đã phản ứng.
Phương trình chữ của phản ứng:
Natri sunfat + Bari clorua →→ Bari sunfat + Natri clorua mBaCl2= mBaSO4 + mNaCl - mNa2SO4 mBaCl2 =23,3+11,7-14,2=20,8gCho 20 gam sắt(III) sunfat
F
e
2
S
O
4
3
tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit
F
e
2
S
O
4
3
v...
Đọc tiếp
Cho 20 gam sắt(III) sunfat F e 2 S O 4 3 tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit F e 2 S O 4 3 và 21,3 gam natri sunfat N a 2 S O 4 Tính khối lượng natri hiđroxit tham gia phản ứng.
Trong phản ứng ở thí nghiệm trên, cho biết khối lượng của natri sunfat Na2SO4 là 14,2g khối lượng của các sản phẩm bari sunfat BaSO4 và natri clorua NaCl theo thứ tự là 23,3g và 11,7g.
Hãy tính khối lượng của Bari clorua BaCl2 đã phản ứng.
Phương trình chữ của phản ứng:
Natri sunfat + Bari clorua → Bari sunfat + Natri clorua
Theo định luật bảo toàn khối lượng
mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
⇒ mBaCl2 = mBaSO4 + mNaCl - mNa2SO4 = 23,3 + 11,7 - 14,2 = 20,8g.
Đúng 0
Bình luận (0)
Cho 58,5 gam nhôm hidroxit tác dụng với 49 gam dd axit sunfuric, sau phản ứng thu
được nhôm sufat và nước.
a. Viết PTHH
b. Sau phản ứng chất nào còn dư ? Khối lượng dư là bao nhiêu gam?
c. Tính khối lượng nhôm sunfat tạo thành.
a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\)
Vậy \(Al\left(OH\right)_3\) dư.
\(m_{dư}=0,75.78-98.0,5=9,5\left(g\right)\)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 58,5 gam nhôm hidroxit tác dụng với 49 gam dd axit sunfuric, sau phản ứng thu
được nhôm sufat và nước.
a. Viết PTHH
b. Sau phản ứng chất nào còn dư ? Khối lượng dư là bao nhiêu gam?
c. Tính khối lượng nhôm sunfat tạo thành.
a, \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right);n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
PTHH: 2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
Mol: \(\dfrac{1}{3}\) 0,5 \(\dfrac{1}{6}\)
b, Ta có: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\) ⇒ Al(OH)3 dư, H2SO4 hết
⇒ \(m_{Al\left(OH\right)_3}=\left(0,75-\dfrac{1}{3}\right).78=32,5\left(g\right)\)
c, \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
Đúng 5
Bình luận (2)
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Không có chất dư (hoặc có thể bn cho sai 49(g) dung dịch là 49(g) H2SO4)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al\left(OH\right)_3}=\dfrac{1}{2}.0,75=0,375\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,375.342=128,25\left(g\right)\)
Đúng 0
Bình luận (1)
Cho 20 gam sắt III sunfat
F
e
2
S
O
4
3
tác dụng với natri hidroxit NaOH, thu được 10,7 gam sắt III hidroxit
F
e
(
O
H
)
3
và 21,3 gam natri sunfat
N
a
2
S
O
4
. Xác định...
Đọc tiếp
Cho 20 gam sắt III sunfat F e 2 S O 4 3 tác dụng với natri hidroxit NaOH, thu được 10,7 gam sắt III hidroxit F e ( O H ) 3 và 21,3 gam natri sunfat N a 2 S O 4 . Xác định khối lượng natri hidroxit tham gia vào phản ứng.
Sơ đồ
Sắt (III) sunfat + Natri hidroxit → Sắt (III) hidroxit + natri sunfat
Áp dụng ĐLBTKL, ta có
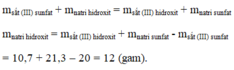
Đúng 0
Bình luận (0)
Cho 3,1 g natri oxit phản ứng với nước thu được 4 g natri hiđroxit.
Cho natri hiđroxit phản ứng hoàn toàn với axit sunfuric tạo thành natri sunfat và nước.
a) Viết phương trình chữ của phản ứng?
b) Tính khối lượng nước tham gia phản ứng?
a)
Natri Oxi + Nước → Natri Hidroxit
Natri hidroxit + axit sunfuric → Natri sunfat + nước
b)
Bảo toàn khối lượng :
$m_{H_2O} = 4 - 3,1 = 0,9(gam)$
Đúng 4
Bình luận (0)
Biết rằng bari hidroxit tác dụng với natri sunfat tạo thành chất kết tủa là bari sunfit và natri hidroxit? a) phương trình hoá học? b) nếu có 17,1 bari hidroxit phản ứng thì khối lượng natri hidro tạo thành bao nhiêu? Tính khối lượng chất kết tủa? c) tính khối lượng natri sunfit(2 cách)
\(n_{Ba\left(OH\right)_2}=\dfrac{17,1}{171}=0,1\left(mol\right)\)
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
0,1 -----------> 0,1------------>0,1----------> 0,2
\(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{BaSO_4}=0,1.233=23,3\left(g\right)\)
C1: \(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
c2: theo đlbtkl \(m_{Na_2SO_4}=23,3+8-17,1=14,2\left(g\right)\)
Đúng 0
Bình luận (0)