Những câu hỏi liên quan
Cho 8.9g hỗn hợp muối cacbonat của hai kim loại kiềm thuộc hai chu kì kế tiếp tác dụng với HCL thứ được 2,24 l khí ở đkc. hai Kim loại là
Xem chi tiết
\(CT:\overline{M}_2CO_3\)
\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\overline{M}_2CO_3+2HCl\rightarrow2MCl+CO_2+H_2O\)
\(0.1.........................................0.1\)
\(M_{\overline{M}_2CO_3}=\dfrac{8.9}{0.1}=89\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow2\overline{M}+60=89\)
\(\Leftrightarrow\overline{M}=14.5\)
Vì : thuộc hai chu kì liên tiếp nên hai kim loại là : \(Li,Na\)
Đúng 2
Bình luận (0)
Cho 9,1 gam hỗn hợp hai muối cacbonat của hai kim loại kiềm ở hai chu kì liên tiếp tác dụng hết với dung dịch HCl dư thu được 2,24 lít CO2 (đktc). Hai kim loại đó là A. Li, Na. B. Na, K. C. K, Rb. D. Rb, Cs.
Đọc tiếp
Cho 9,1 gam hỗn hợp hai muối cacbonat của hai kim loại kiềm ở hai chu kì liên tiếp tác dụng hết với dung dịch HCl dư thu được 2,24 lít CO2 (đktc). Hai kim loại đó là
A. Li, Na.
B. Na, K.
C. K, Rb.
D. Rb, Cs.
Đáp án A
Phân tử khối trung bình: 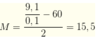
Vậy, 2 kim loại là Li và Na
Đúng 0
Bình luận (0)
Cho 6,08 gam hỗn hợp gồm hai hiđroxit của hai kim loại kiềm (thuộc hai chu kì kế tiếp nhau) tác dụng với một lượng dư HCl thu được 8,3 gam muối khan. Thành phần phần trăm về khối lượng của hiđroxit có khối lượng phân tử nhỏ hơn là
A. 73,68%
B. 52,63%
C. 36,84%
D. 26,32%
Cho 3 gam hỗn hợp X gồm hai kim loại kiềm thuộc hai chu kì kế tiếp nhau tác dụng với dung dịch HCl dư, thu được 2,24 lít khí H2 (đktc). Hai kim loại trong X là A. Na và K. B. Li và Na. C. Rb và Cs D. K và Rb
Đọc tiếp
Cho 3 gam hỗn hợp X gồm hai kim loại kiềm thuộc hai chu kì kế tiếp nhau tác dụng với dung dịch HCl dư, thu được 2,24 lít khí H2 (đktc). Hai kim loại trong X là
A. Na và K.
B. Li và Na.
C. Rb và Cs
D. K và Rb
: Cho 8,7 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại nằm kế tiếp nhau trong nhóm IA, tác dụng với dung dịch HCl dư, toàn bộ khí CO2 sinh ra được dẫn vào dung dịch nước vôi trong, thu được 7 gam kết tủa. Khối lượng của muối cacbonat có nguyên tử khối lớn hơn trong X là: A. 3,46 gam. B. 4,13 gam. C. 3,18 gam. D. 5,52 gam.
Đọc tiếp
: Cho 8,7 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại nằm kế tiếp nhau trong nhóm IA, tác dụng với dung dịch HCl dư, toàn bộ khí CO2 sinh ra được dẫn vào dung dịch nước vôi trong, thu được 7 gam kết tủa. Khối lượng của muối cacbonat có nguyên tử khối lớn hơn trong X là:
A. 3,46 gam. B. 4,13 gam. C. 3,18 gam. D. 5,52 gam.
cho 18,4g hỗn hợp hai muối cacbonat của hai kim loại thuộc hai chu kì liên tiếp tác dụng với HCL thu được 4,48 lít khí cacbonic ( đktc) . xác định hai kim loại kiềm trong muối , tính khối lượng clorua thu được sau phản ứng
Cho 18,4 hỗn hợp hai muối cacbonat của hai kim loại thuộc nhóm IIA ở hai chu kỳ liên tiếp tác dụng hết vs dd HCl. Cô cạn dd sau phản ứng thu được 20.6 g muối khan. Hai kim loại đó là
Ap dụng tăng giảm khối lượng
\(n_{MCO_3}=\frac{20,6-18,4}{35,5.2-60}=0,2\)
\(M+60=18,4:0,2=92\Leftrightarrow M=32\)suy ra 2 nguyên tố đó là Mg và Ca
Đúng 0
Bình luận (0)
cho 7,16 gam hỗn hợp 2 muối cacbonat của 2 kim loại kiềm tác dụng vừa đủ với dung dịch H2 SO4 10% thu được 1,344 lít khí ở điều kiện tiêu chuẩn và dung dịch X biết 2 kim loại ở 2 chu kì liên tiếp xác định hai kim loại và phần trăm khối lượng mỗi muối trong hỗn hợp đầu b Tính khối lượng dung dịch H2 SO4 đặc tính nồng độ phần trăm muối trong dung dịch X
Xem chi tiết
Cho 3,1 g hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước thu được 1,12 lít H2 ở đktc và dung dịch kiềm. Tính thể tích dd HCl 2M cần dùng để trung hòa dd kiềm và khối lượng muối clorua thu được.
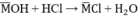
Theo pt: nHCl = nMOH = 0,1 (mol)
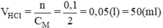
m(MCl) = 0,1.(31 + 35,5) = 6,65(g)
Đúng 0
Bình luận (0)