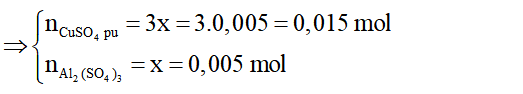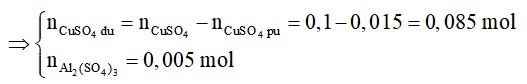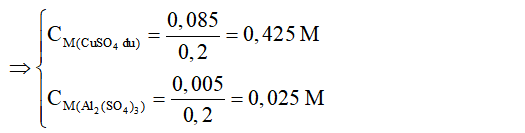Bài 1: Nhúng một lá nhôm vào 200ml dung dịch CuSO4, đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch CuSO4 đã dùng là?

Những câu hỏi liên quan
Nhúng một lá nhôm vào 200ml dung dịch
C
u
S
O
4
, đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch
C
u
S
O
4
đã dùng là: A. 0,05 M B. 0,15 M C.0,2 M D. 0,25 M
Đọc tiếp
Nhúng một lá nhôm vào 200ml dung dịch C u S O 4 , đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch C u S O 4 đã dùng là:
A. 0,05 M
B. 0,15 M
C.0,2 M
D. 0,25 M
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x…….x…3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 -2x.27 = 1,38 ⇔ 138x = 1,38
⇔ x = 0,01 mol
⇒ n C u S O 4 = 3x = 3.0,01 = 0,03 mol
⇒ C M C u S O 4 = 0,03/0,2 = 0,15 mol
⇒ Chọn B.
Đúng 0
Bình luận (0)
Nhúng một lá nhôm vào dung dịch CuSO 4 . Sau một thời gian, lấy lá nhôm ra khỏi dung dịch thì thấy khối lượng dung dịch giảm 1,38 gám. Khối lượng của Al đã tham gia phản ứng là
A. 0,27 gam ; B. 0,81 gam ; C. 0,54 gam ; D. 1,08 gam.
Đáp án C.
Gọi khối lượng miếng Al là a gam, lượng nhôm đã phản ứng là x gam :
2Al + 3 CuSO 4 → Al 2 SO 4 3 + 3 Cu
Gọi x là khối lượng Al phản ứng.
![]()
So với khối lượng miếng Al ban đầu thì khối lượng miếng Al sau phản ứng tăng 1,38 gam.
Đúng 0
Bình luận (0)
Nhúng một lá nhôm vào 200ml dung dịch CuSO4, đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch CuSO4 đã dùng là bao nhiêu?
2Al + 3CuSO4 → Al2(SO4)3+ 3Cu
2x………3x…………..x………………3x (mol)
theo bài ta có:
mCu bám vào – mAl tan = mAl tăng
⇔ 3x.64 -2x.27 = 1,38
⇔ 138x = 1,38
⇔ x = 0,01 mol
⇒n\(CuSO_4\)= 3x = 3.0,01 = 0,03 mol
⇒ \(C_{M_{CuSO_4}}\)=\(\frac{0,03}{0,02}\) = 0,15 mol
Đúng 0
Bình luận (1)
2Al + 3CuSO4 → Al2(SO4)3+ 3Cu
2x………3x…………..x………………3x (mol)
theo bài ta có:
mCu bám vào – mAl tan = mAl tăng
⇔ 3x.64 -2x.27 = 1,38
⇔ 138x = 1,38
⇔ x = 0,01 mol
⇒nCuSO4CuSO4= 3x = 3.0,01 = 0,03 mol
⇒ CMCuSO4CMCuSO4=0,030,020,030,02 = 0,15 mol
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Nhúng một lá Zn vào 200 ml dung dịch CuSO4 nồng độ x (mol/l) đến khi dung dịch mất màu hoàn toàn thấy khối lượng lá Zn giảm 0,15 gam so với ban đầu (coi kim loại tạo thành bán hết vào lá kẽm). Giá trị của x là: A. 0,75 B. 0,25 C. 0,35 D. 0,30
Đọc tiếp
Nhúng một lá Zn vào 200 ml dung dịch CuSO4 nồng độ x (mol/l) đến khi dung dịch mất màu hoàn toàn thấy khối lượng lá Zn giảm 0,15 gam so với ban đầu (coi kim loại tạo thành bán hết vào lá kẽm). Giá trị của x là:
A. 0,75
B. 0,25
C. 0,35
D. 0,30
Đáp án A
Zn + CuSO4 → ZnSO4 + Cu
Đặt nZn pứ = a mol → nCu = a mol
Sau khi dung dịch CuSO4 mất màu hoàn toàn thì CuSO4 phản ứng hết.
→ Khối lượng lá Zn giảm là mchất rắn giảm = mZn pứ - mCu sinh ra = 65a - 64a = a = 0,15
→ x = CM CuSO4 = n/Vdd = 0,15: 0,2 = 0,75M
Đúng 0
Bình luận (0)
Nhúng một lá nhôm nặng 16,2g vào 512g dung dịch CUSO4, 25%. Sau một thời gian lấy lá nhôm ra khỏi dung dịch, cân lại thấy nặng 32,85g. Còn lại dung dịch A.
a. Tính khôi lượng Al dã pu và khôi luợng Cu sinh ra.
b. Tinh nồng độ C°o của ddA. Coi thể tích ddA ko đối.
Giả sử toàn bộ lượng Cu sinh ra bám hết vào lá nhôm
a) \(m_{tăng}=32,85-16,2=16,65\left(g\right)\\3 CuSO_4+2Al\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
Gọi x là số mol Al phản ứng
=> \(n_{Cu}=\dfrac{3}{2}n_{Al}=1,5x\left(mol\right)\)
Ta có: \(m_{tăng}=1,5x.64-27x=16,65\left(g\right)\)
=> \(x=\dfrac{111}{460}\left(mol\right)\)
=> \(m_{Al\left(pứ\right)}=\dfrac{111}{460}.27=6,52\left(g\right)\); \(m_{Cu}=\dfrac{111}{460}.1,5.64=23,17\left(g\right)\)
b) \(m_{ddsaupu}=6,52+512-23,17=495,35\left(g\right)\)
\(n_{CuSO_4\left(pư\right)}=\dfrac{512.25\%}{160}=0,8\left(mol\right)\)
=> \(n_{CuSO_4\left(dư\right)}=0,8-\dfrac{111}{460}.1,5=\dfrac{403}{920}\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{111}{920}\left(mol\right)\)
=> \(C\%_{CuSO_4}=14,15\%;C_{Al_2\left(SO_4\right)_3}=8,33\%\)
Đúng 1
Bình luận (0)
Bài 2: Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch CuSO4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của CuSO4 và Al2 (SO4)3 trong dung dịch sau phản ứng lần lượt là?
\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\\ Đặt:n_{Al\left(pứ\right)}=x\left(mol\right)\\ m_{tăng}=m_{Cu\left(sinhra\right)}-m_{Al\left(pứ\right)}=\dfrac{3}{2}x.64-x.27=25,69-25\\ \Rightarrow x=0,01\left(mol\right)\\ \Rightarrow n_{CuSO_4\left(dư\right)}=0,2.0,5-0,01.\dfrac{3}{2}=0,085\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=0,01\left(mol\right)\\ CM_{Al_2\left(SO_4\right)_3}=\dfrac{0,01}{0,2}=0,05\left(M\right)\\ CM_{CuSO_4\left(dư\right)}=\dfrac{0,085}{0,2}=0,475M\)
Đúng 3
Bình luận (0)
nCuSO4= 0,5.0,2 = 0,1 mol
2Al+3CuSO4→Al2(SO4)3+3Cu
2x……3x……..x……3x (Mol)
Theo bài ta có:
mCu bámvào−mAl tan=mAl tăng
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
*Tham khảo
Đúng 4
Bình luận (2)
Nhúng một lá nhôm nặng 16,2g vào 512g dung dịch CUSO4, 25%. Sau một thời gian lấy lá nhôm ra khỏi dung dịch, cân lại thấy nặng 32,85g. Còn lại dung dịch A. a. Tính khôi lượng Al dã pu và khôi luợng Cu sinh ra. b. Tinh nổng độ C°o của ddA. Coi thể tích ddA ko đối. Giả sử toàn bộ lượng Cu sinh ra bám hết vào lá nhôm
Câu này mình trả lời rồi, bạn xem ở link sau :
https://hoc24.vn/cau-hoi/nhung-mot-la-nhom-nang-162g-vao-512g-dung-dich-cuso4-25-sau-mot-thoi-gian-lay-la-nhom-ra-khoi-dung-dich-can-lai-thay-nang-3285g-con-lai-dung-dich-aa-tinh-khoi-luong-al-da-pu-va-khoi-luong-cu.1706643518303
Đúng 0
Bình luận (0)
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch
C
u
S
O
4
0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của
C
u
S
O
4
và
A
l
2
S
O
4
trong dung dịch sau phản ứng lần lượt là...
Đọc tiếp
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch C u S O 4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của C u S O 4 và A l 2 S O 4 trong dung dịch sau phản ứng lần lượt là
A. 0,425M và 0,2M
B. 0,425M và 0,3M
C. 0,4M và 0,2M
D. 0,425M và 0,025M.
n C u S O 4 = 0,5.0,2 = 0,1 mol
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x……..x……3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
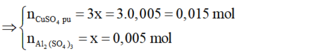

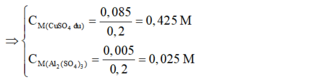
⇒ Chọn D.
Đúng 0
Bình luận (0)
Nhúng một thanh nhôm nặng 25g vào 200ml dung dịch CuSO4 0,5M. Sau một thời gian cân lại thanh nhôm thấy nặng 25,96g. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng.