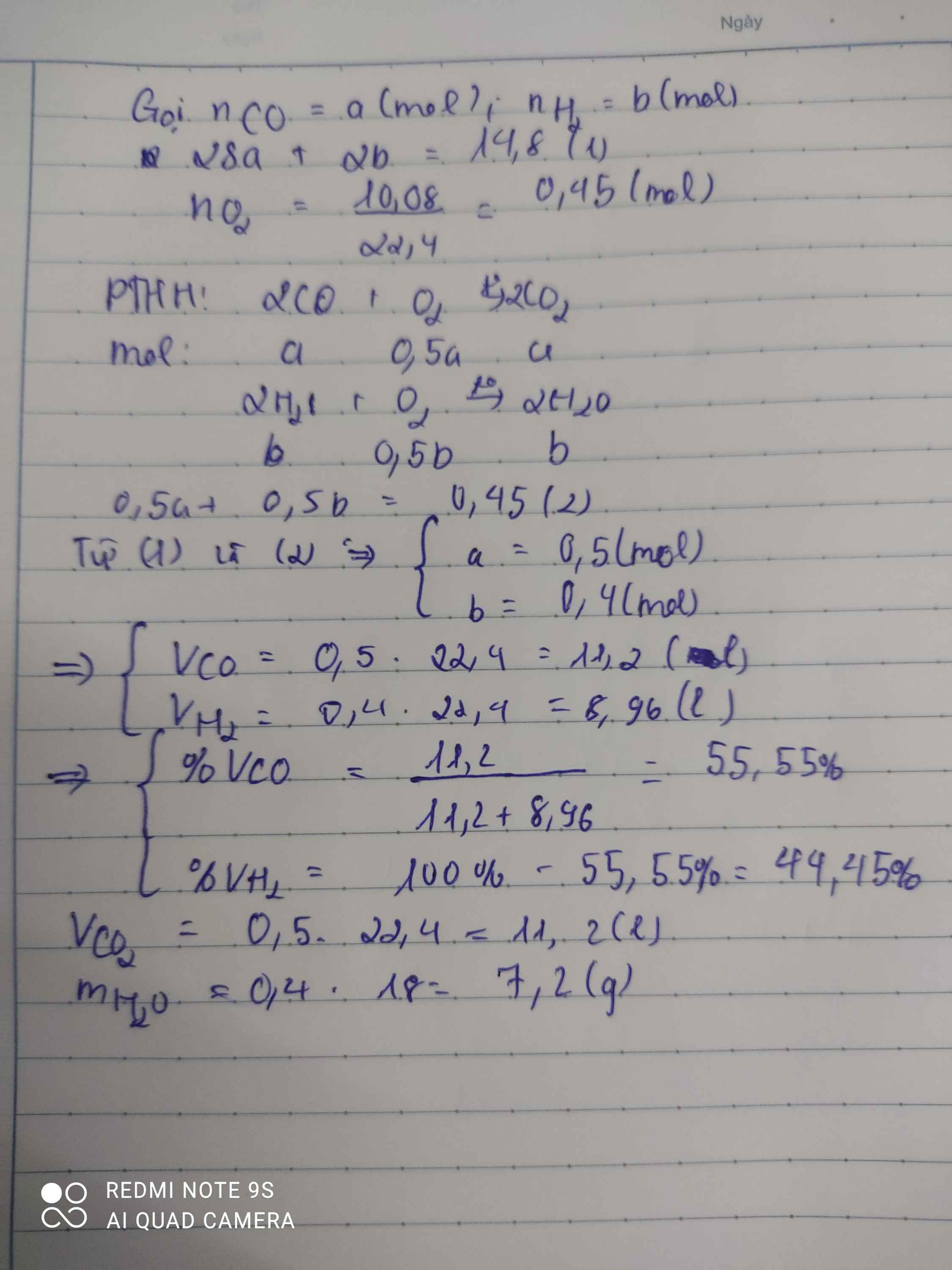Đốt cháy hoàn toàn 1 hỗn hợp khí gồm CO và H2 cần dùng 6,72L O2 . Khí sinh ra có 4,48L khí CO2 . Biết các khí ở ĐKTC . Tính thành phần trăm theo thể tích của các khí trong hỗn hợp

Những câu hỏi liên quan
Đốt cháy hoàn toàn một hỗn hợp khí gồm có CO và H2 cần dùng 6,72 lit khí O2. Khí sinh ra có 4,48 lit khí CO2. Hãy tính thành phần % của hỗn hợp khí ban đầu theo thể tích hỗn hợp( các thể tích khí đều đo ở cùng đktc)
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
2CO + O2 --to--> 2CO2
0,2<---0,1<--------0,2
2H2 + O2 --to--> 2H2O
0,4<--0,2<-------0,2
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,2+0,4}.100\%=33,33\%\\\%V_{H_2}=100\%-33,33\%=66,67\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2CO + O2 --to--> 2CO2
0,3<--0,15<------0,3
2H2 + O2 --to--> 2H2O
0,1<--0,05
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\%n_{CO}=\dfrac{0,3}{0,3+0,1}.100\%=75\%\\\%V_{H_2}=100\%-75\%=25\%\end{matrix}\right.\)
Đốt cháy hoàn toàn một hỗn hợp khí Z gồm CO và H 2 cần dùng 4,48 lít khí O 2 (đktc). Thể tích khí sinh ra chứa 3,36 lít C O 2 . Hãy tính thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp ban đầu.
Đốt cháy hoàn toàn một hỗn hợp khí gồm có CO và H2 cần dùng 7,437 lít khí O2 khí sinh ra có 4,958 lít khí CO2. Thành phần phần trăm theo thể tích của khí H2 trong hỗn hợp bạn đầu là
\(n_{CO_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
PTHH:
2CO + O2 --to--> 2CO2
0,2 0,1 0,2
-> nO2 = 0,3 - 0,1 = 0,2 (mol)
2H2 + O2 --to--> 2H2O
0,4 0,2
\(\rightarrow n_{hhkhí}=0,1+0,4=0,5\left(mol\right)\\ \rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,5}=40\%\\\%V_{H_2}=100\%-40\%=60\%\end{matrix}\right.\)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn một hỗn hợp khí gồm CO và H2 cần dùng 6,72(l) khí oxi. Khí sinh ra có 4,48(l) khí CO2. Hãy tính thành phần % của hỗn hợp khí ban đầu theo thể tích.
PTHH: \(2CO+O_2\underrightarrow{t^o}2CO_2\) (1)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\) (2)
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CO}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow n_{O_2\left(1\right)}=0,1\left(mol\right)\\\Sigma n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(2\right)}=0,2\left(mol\right)\) \(\Rightarrow n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow\%V_{H_2}=\dfrac{0,4}{0,4+0,2}\cdot100\%\approx66,67\%\)
\(\Rightarrow\%V_{CO}=33,33\%\)
Đúng 1
Bình luận (0)
các bạn giúp mình câu hỏi này với, khổ qua, huhu
đốt cháy hoàn toàn một hỗn hợp khí gồm có CO và H2 cần dùng 6.72 lít khí O2. khi sinh ra có 4.48 lít khí CO2. hãy tính thành phần phần trăm của hỗn hợp khí ban đầu theo thể tích hỗn hợp.
Mong các bạn giúp mình nhanh nha, mình cần gấp lắm rùi!
Cảm ơn các bạn!
CO +1/2 O2 = CO2
x 1/2x x
H2 + 1/2O2 = H2O
y 1/2y y
gọi số mol của CO và H2 lần lượt là x và y
theo pt ta có hệ : \(\begin{cases}\frac{1\left(x+y\right)}{2}=0,3\\x=0,2\end{cases}\)
giải pt ra và tính phần trăm hh khí
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 14,8 g hỗn hợp khí gồm CO và H2 cần dùng 10,08 l khí O2 Tính:
a. Thành phần % về thể tích mỗi khí trong hỗn hợp ban đầu(đktc)
b. Thể tích khí CO2 và khối lượng nước thu được(đktc)
Đốt cháy hoàn toàn một hỗn hợp khí gồm có CO và H2 cần dùng 9,6g khí oxi . Khí sinh ra có 8,8g CO2 . Phần trăm theo khối lượng của CO trong hỗn hợp khí ban đầu là
nO2 = 9.6/32 = 0.3 (mol)
nCO2 = 8.8/44 = 0.2 (mol)
CO + 1/2O2 -to-> CO2
0.2_____0.1______0.2
H2 + 1/2O2 -to-> H2O
0.4__0.3-0.1
%CO = 0.2*28/(0.2*28 + 0.4*2) * 100% = 87.5%
Chúc bạn học tốt !!!
Đúng 3
Bình luận (1)
Đốt cháy hoàn toàn một hỗn hợp gồm H2 và CO thì dùng hết 89,6l khí O2 ở đktc. Biết tỉ lệ số mol của hai sản phẩm là 3:1
a/ Viết các PT phản ứng xảy ra
b/ Tính thành phần phần trăm theo thể tích và khối lượng mỗi khí trong hỗn hợp ban đầu
\(n_{O_2}=\dfrac{89.6}{22.4}=4\left(mol\right)\)
\(n_{H_2O}=3a\left(mol\right)\)
\(n_{CO_2}=a\left(mol\right)\)
\(2H_2+O_2\underrightarrow{^{^{t^0}}}2H_2O\)
\(2CO+O_2\underrightarrow{^{^{t^0}}}2CO_2\)
\(n_{O_2}=1.5a+0.5a=4\left(mol\right)\)
\(\Leftrightarrow a=2\)
\(n_{H_2}=3\left(mol\right),n_{CO}=1\left(mol\right)\)
\(\%V_{H_2}=\dfrac{3}{4}\cdot100\%=75\%\)
\(\%V_{CO}=25\%\)
\(\%m_{H_2}=\dfrac{3\cdot2}{3\cdot2+1\cdot28}\cdot100\%=17.64\%\)
\(\%m_{CO}=100-17.64=82.36\%\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp khí gồm có CO và H2 cần dùng 9,6 gam khí oxi sinh ra 8,8 gam khí CO2. Tính % theo khối lượng và % theo thể tích của mỗi khí có trong hỗn hợp ban đầu.
\(2CO + O_2 \xrightarrow{t^o} 2CO_2\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ n_{CO} = n_{CO_2} = \dfrac{8,8}{44} = 0,2(mol)\\ n_{O_2} = \dfrac{n_{CO} + n_{H_2}}{2}=\dfrac{0,2+n_{H_2}}{2} = \dfrac{9,6}{32} = 0,3(mol)\\ \Rightarrow n_{H_2} = 0,4(mol)\\ \%V_{CO} = \dfrac{0,2}{0,2 + 0,4}.100\% = 33,33\%\\ \%V_{H_2} = 100\% - 33,33\% = 66,67\%\\ \%m_{CO} = \dfrac{0,2.28}{0,2.28+0,4.2}.100\%=87,5\%\\ \%m_{H_2} = 100\% - 87,5\% = 12,5\%\)
Đúng 3
Bình luận (0)