Hòa tan 5,4g một kim loại hóa trị III vào dung dịch H2SO4 lượng dư. Sau p/ứ thu được 6,72 lít khí H2 (đktc). Xác định tên kim loại.

Những câu hỏi liên quan
Hòa tan 5,4g một kim loại A hóa trị III vào dung dịch H2SO4 lượng dư. Sau p/ứ thu được 6,72 lít khí H2 (đktc). a) Xác định kim loại A b) tính thể tích dung dịch axit sunfuric 0,2M cần dùng cho phản ứng c) nếu dẫn lượng khí thu được ở phản ứng trên qua bình đựng 46,4g fe2o3. tính khối lượng chất rắn th...
Đọc tiếp
Hòa tan 5,4g một kim loại A hóa trị III vào dung dịch H2SO4 lượng dư. Sau p/ứ thu được 6,72 lít khí H2 (đktc). a) Xác định kim loại A b) tính thể tích dung dịch axit sunfuric 0,2M cần dùng cho phản ứng c) nếu dẫn lượng khí thu được ở phản ứng trên qua bình đựng 46,4g fe2o3. tính khối lượng chất rắn thu được sau phản ứng
\(2A+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\Rightarrow n_A=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ a,M_A=\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Nhôm\left(Al=27\right)\\ b,n_{H_2SO_4}=n_{H_2}=0,3\left(mol\right)\\ V_{ddH_2SO_4}=\dfrac{0,3}{0,2}=1,5\left(lít\right)\\ c,\\ 3H_2+Fe_2O_3\rightarrow\left(t^o\right)2Fe+3H_2O\\ n_{Fe_3O_4}=\dfrac{46,4}{232}=0,2\left(mol\right)\\ n_{H_2}=0,3\left(mol\right)\\ Vì:\dfrac{0,3}{3}< \dfrac{0,2}{1}\Rightarrow Fe_3O_4dư\\ n_{Fe}=\dfrac{2}{3}.n_{H_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ n_{Fe_3O_4\left(dư\right)}=0,2-\dfrac{1}{3}.0,3=0,1\left(mol\right)\\ m_{rắn}=m_{Fe_3O_4\left(dư\right)}+m_{Fe}=0,1.232+0,2.56=34,4\left(g\right)\)
Đúng 1
Bình luận (0)
Này mới đúng nè em!
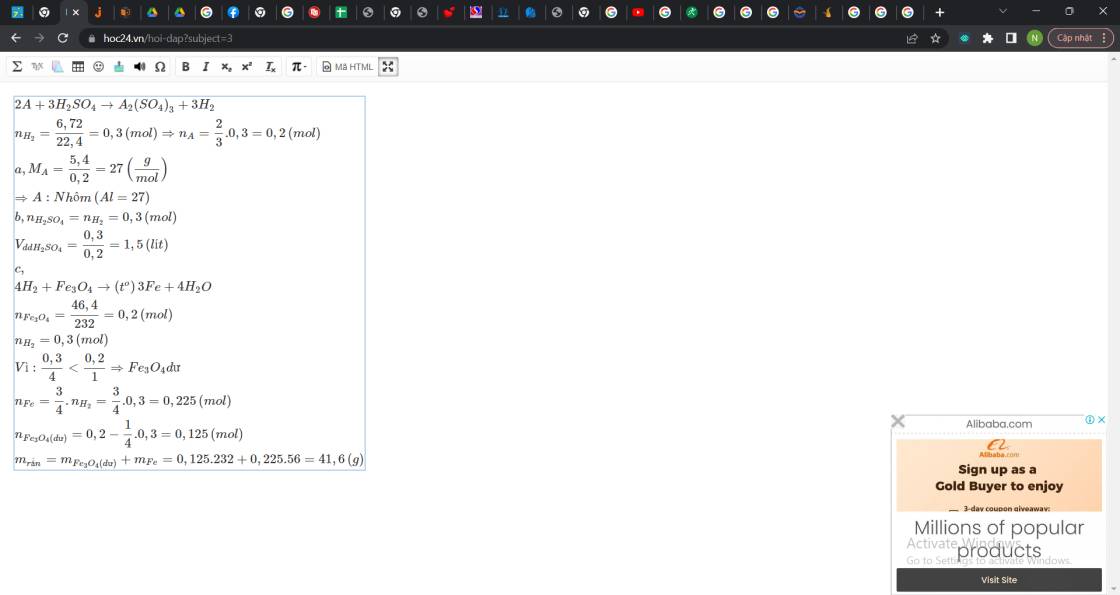
Đúng 0
Bình luận (0)
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại ABài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Đọc tiếp
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại A
Bài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Bài 24:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:A+2HCl\rightarrow ACl_2+H_2\uparrow\)
Theo pthh: nA = nH2 = 0,15 (mol)
=> MA = \(\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\)
=> A là Mg
Bài 25:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\ PTHH:2A+6HCl\rightarrow2ACl_3+3H_2\uparrow\\ Mol:0,3\leftarrow0,9\leftarrow0,3\leftarrow0,45\\ \rightarrow\left\{{}\begin{matrix}M_A=\dfrac{8,1}{0,3}=27\left(\dfrac{g}{mol}\right)\Rightarrow A:Al\\m_{HCl}=0,9.36,5=32,85\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Bài 24.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_A=\dfrac{3,6}{M_A}\) mol
\(A+2HCl\rightarrow ACl_2+H_2\)
0,15 0,15 ( mol )
\(\Rightarrow\dfrac{3,6}{M_A}=0,15mol\)
\(\Leftrightarrow M_A=24\) ( g/mol )
=> A là Magie ( Mg )
Bài 25.
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(n_A=\dfrac{8,1}{M_A}\) mol
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,3 0,45 ( mol )
\(\Rightarrow\dfrac{8,1}{M_A}=0,3\)
\(\Leftrightarrow M_A=27\) g/mol
=> A là nhôm ( Al )
Đúng 1
Bình luận (0)
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
\(n_{H2\left(dktc\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,2 0,3
\(n_R=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\left(dvc\right)\)
Vậy kim loại R là nhôm
b) \(2Al+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(n_{SO2}=\dfrac{0,3.3}{2}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
a) PTHH: \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_R=0,2\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,4}{0,2}=27\) \(\Rightarrow\) R là Nhôm (Al)
b) PTHH: \(2Al+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
Theo PTHH: \(n_{SO_2}=0,3\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,3\cdot22,4=6,72\left(l\right)\)
Đúng 2
Bình luận (0)
Hòa tan 5,4 gam kim loại X (hóa trị III) trong dung dịch H2SO4 dư thu được 6,72 lít H2(đktc). Xác định
kim loại X?
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2A + 3H2SO4 --> A2(SO4)3 + 3H2
_____0,2<---------------------------------0,3______(mol)
=> \(M_A=\dfrac{5,4}{0,2}=27\left(g/mol\right)=>Al\)
Đúng 2
Bình luận (0)
Bài tập 1: Hòa tan hoàn toàn 2,8 gam kim loại A (chưa rõ hóa trị) bằng dung dịch H2SO4 loãng, dư. sau phản ứng thu được 6,72 lít khí H2(đktc). Xác định kim loại A.
nH2 = 0,3 mol
2A + nH2SO4 → A2(SO4)n + nH2
0,6/n ← 0,3 mol
mA = 2,8 gam, nA = 0,6/n
→ MA = 2,8.n/0,6 = 14n/3, xét các giá trị n = 1, 2, 3 để suy ra MA
Với đề bài này thì không ra được đáp án nhé.
Đúng 4
Bình luận (0)
Cho 5,4 gam kim loại X hóa trị III hòa tan hết vào dung dịch HCl thu được 6,72 lít khí H2 (đktc)
a)Lập PTHH của phản ứng.
b)Xác định kim loại X.
c) Tính khối lượng muối XCl3 tạo thành
\(a,PTHH:2X+6HCl\to 2XCl_3+3H_2\\ b,n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ \Rightarrow n_{X}=\dfrac{2}{3}n_{H_2}=0,2(mol)\\ \Rightarrow M_{X}=\dfrac{5,4}{0,2}=27(g/mol)\)
Vậy X là nhôm (Al)
\(c,n_{AlCl_3}=n_{Al}=0,2(mol)\\ \Rightarrow m_{AlCl_3}=0,2.133,5=26,7(g)\)
Đúng 0
Bình luận (0)
Bài tập 1: Hòa tan hoàn toàn 2,8 gam kim loại A (chưa rõ hóa trị) bằng dung dịch H2SO4 loãng, dư. sau phản ứng thu được 6,72 lít khí H2(đktc). Xác định kim loại A. Bài tập 2: Ngâm 1 lá đồng vào dung dịch AgNO3. Sau một thời gian phản ứng thấy khối lượng lá đồng tăng thêm 0,76 gam. Tính khối lượng đồng bị hòa tan và khối lượng bạc sinh ra. Cho rằng toàn bộ lượng bạc sinh ra bám hết vào lá đồng.
Đọc tiếp
Bài tập 1: Hòa tan hoàn toàn 2,8 gam kim loại A (chưa rõ hóa trị) bằng dung dịch H2SO4 loãng, dư. sau phản ứng thu được 6,72 lít khí H2(đktc). Xác định kim loại A.
Bài tập 2: Ngâm 1 lá đồng vào dung dịch AgNO3. Sau một thời gian phản ứng thấy khối lượng lá đồng tăng thêm 0,76 gam. Tính khối lượng đồng bị hòa tan và khối lượng bạc sinh ra. Cho rằng toàn bộ lượng bạc sinh ra bám hết vào lá đồng.
1,Khi hòa tan 7,2 gam một kim loại R hóa trị II vào dung dịch H2SO4 loãng dư sinh 6,72 lít khí H2 ở đktc. Tìm tên kim loại R.
Xem chi tiết
\(N_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
Bảo toàn e ta có:
\(\dfrac{7,2}{M_R}.n=0,3.2=0,6\)
\(\Rightarrow7,2n=0,6.M_R\Leftrightarrow12n=M_R\)
Nếu n =1 => M = 12 ( loại)
Nếu n = 2 => M = 24 (Mg)
Đúng 3
Bình luận (0)






















