
Những câu hỏi liên quan
Hãy vẽ những hình khối chữ nhật để so sánh thể tích các khí sau (đktc): 1gH2 ; 8g O2 ; 3,5gN2 ; 33gCO2
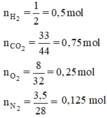
Sơ đồ biểu thị về tỉ lệ thể tích của các khí.
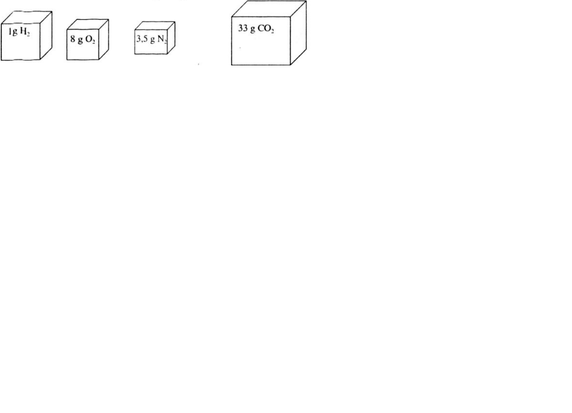
Tỉ lệ số mol các chất khí cũng chính là tỉ lệ về thể tích các khí nên thể tích khí VCO2 > VH2 > VO2 > VN2.
Đúng 0
Bình luận (0)
Cho hỗn hợp khí A gồm N2 và O2 có tỉ lệ thể tích tương ứng là 5:3
a/ tính tỉ khối của hỗn hợp khí A đối với không khí
b/ Tính thể tích (đktc) của 3,54 g khí A
c/ Phải trộn thêm vào 20lit hỗn hợp A ở trên bao nhiêu lít khí hidro để được hỗn hợp mới có tỉ khối so với hidro bằng 6,5.Biết các thể tích đo ở cùng điều kiện nhiệt đọ và áp suất.
a/ Tỉ khối của hỗn hợp khí A đối với không khí là:
\(d_{A:kk}=\dfrac{M_A}{29}=\dfrac{60}{29}=2\)
b/ Thể tích khí A là:
\(V=22,4.3,54=79,296\left(l\right)\)
Câu c mình không biết làm :V mà 2 câu trên có đúng hay không mình cũng không biết nốt :V
Đúng 0
Bình luận (0)
Cho 19,55 g hỗn hợp 2 kim loại Cu, Al vào 200 g dung dịch H2SO4 18,375 % thu được dung dịch A, chất rắn B và chất khí D. a. Viết PTHH và xác định các chất A, B, D. b. Tính thể tích khí D (ở đktc). c. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu. d. Tính nồng độ % dung dịch muối thu được sau phản ứng.
\(a.2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ A:Al_2\left(SO_4\right)_3\\ B:Cu\\ D:H_2\\ b.n_{H_2}=n_{H_2SO_4}=\dfrac{200.18,375\%}{100\%.98}=0,375mol\\ V_{H_2}=0,375.22,4=8,4l\\ c.n_{Al}=\dfrac{0,375.2}{3}=0,25mol\\ m_{Al}=0,25.27=6,75g\\ m_{Cu}=19,55-6,75=12,8g\\ d.n_{Al_2\left(SO_4\right)_3}=\dfrac{0,375}{3}=0,125mol\\ m_{dd}=6,75+200-0,375.2=206g\\ m_{Al_2\left(SO_4\right)_3}=0,125.342=42,75g\\ C_{\%_{Al_2\left(SO_4\right)_2}}=\dfrac{42,75}{206}\cdot100\%=20,75\%\)
Đúng 1
Bình luận (0)
Hòa tan hết 33g hỗn hợp Mg, MgCO3 trong 800ml dung dịch HCl 2M (d=1,1g/ml) thu được 11,2l hỗn hợp khí A(đktc)
1.Tính % thể tích các chất khí trong A
2.Tính C% các chất trong dung dịch sau phản ứng
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
a, \(n_A=0,5\left(mol\right)=n_{H_2}+n_{CO_2}\)
\(m_{hh}=33=24n_{Mg}+84n_{MgCO_3}=84n_{CO_2}+24n_{H_2}\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,15\left(30\%\right)\\n_{CO_2}=0,35\left(70\%\right)\end{matrix}\right.\) ( mol )
b, Có \(n_{HCl}=2n_{H_2}+2n_{CO_2}=1\left(mol\right)\)
Mà \(n_{HClbd}=1,6\left(mol\right)\)
\(\Rightarrow n_{HCldu}=0,6\left(mol\right)\)
Lại có : \(m_{ddsau}=m_{hh}+m_{ddHCl}-m_{hhkhi}=33+880-0,15.2-0,35.44=897,3\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,5.\left(24+71\right)}{897,3}.100\%\approx5,3\%\\C\%_{HCldu}=\dfrac{0,6\left(35,5+1\right)}{897,3}.100\%\approx2,44\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho hỗn hợp gồm 2,6 gam kẽm và 0,81 gam nhôm tan hết trong 120 ml dung dịch HCl 2M. a) Tính thể tích khí thoát ra ở đktc b) Tính CM,C% các chất sau phản ứng.(Coi thể tích dung dịch không đổi,khối lượng riêng của dung dịch HCl = 1,072 g/ml.
Cho 13 kẽm tác dụng với 109,5 g dùng dịch HCl 20%. a, Tính thể tích khí thu được (ở đktc) a, Tính khối lượng muối thu được c, Tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{109,5.20\%}{36,5}=0,6\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,2}{1}< \dfrac{0,6}{2}\Rightarrow HCldư\\ n_{H_2}=n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\\ n_{HCl\left(dư\right)}=0,6-0,2.2=0,2\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ b,m_{ZnCl_2}=136.0,2=27,2\left(g\right)\\ c,m_{ddsau}=13+109,5-0,2.2=122,1\left(g\right)\\ C\%_{ddZnCl_2}=\dfrac{27,2}{122,1}.100\approx22,277\%\\ C\%_{ddHCl\left(dư\right)}=\dfrac{0,2.36,5}{122,1}.100\approx5,979\%\)
Đúng 1
Bình luận (1)
Zn + 2HCl -> ZnCl2 + H2
a, nZn = 13/65= 0,2(mol)
mHCl= 109,5.20%/100%=21.9(g)
nHCl=21,9/36,5=0,6(mol)
Theo PT nHCl = 2nZn= 2.0,2= 0,4(mol)<0,6(mol)
=> HCl pư dư, Zn pư hết
Theo PT: nH2= nZn =0,2(mol)
VH2=0,2.22,4=4,48(l)
b, Theo PT: nZnCl2=nZn=0,2(mol)
mZnCl2= 0,2.136=27,2(g)
c, mdd sau pư= 13+109,5-0,2.2=122,1(g)
C%dd ZnCl2=27,2.100%/122,1=22,28%
nHCl dư= 0,6-0,4=0,2(mol)
mHcl
Đúng 1
Bình luận (1)
đốt cháy hoàn toàn 54.6g hỗn hợp FeS và ZnS sau phản ứng thu được 48.2 hỗn hợp Fe2O3 và ZnO
a) Tính % theo khối lượng của các chất trong hỗn hợp ban đầu
b) Tính thể tích O2 tham gia phản ứng ở đktc
c) Tính thể tích SO2 thu được sau phản ứng ở đktc
Xem chi tiết
PTHH: \(4FeS+7O_2\underrightarrow{t^o}2Fe_2O_3+4SO_2\) (1)
\(2ZnS+3O_2\underrightarrow{t^o}2ZnO+2SO_2\) (2)
a) Gọi số mol của FeS là \(a\) \(\Rightarrow n_{Fe_2O_3}=\dfrac{1}{2}a\left(mol\right)\)
Gọi số mol của ZnS là \(b\) \(\Rightarrow n_{ZnO}=b\left(mol\right)\)
Ta lập được hệ phương trình
\(\left\{{}\begin{matrix}88a+97b=54,6\\80a+81b=48,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,4\\b=0,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{FeS}=0,4\cdot88=35,2\left(g\right)\\m_{ZnS}=19,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{FeS}=\dfrac{35,2}{54,6}\cdot100\%\approx64,47\text{%}\\\%m_{ZnS}=35,53\%\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{O_2\left(1\right)}=\dfrac{7}{4}n_{FeS}=0,7\left(mol\right)\\n_{O_2\left(2\right)}=\dfrac{3}{2}n_{O_2\left(2\right)}=0,3\left(mol\right)\\n_{SO_2\left(1\right)}=n_{FeS}=0,4\left(mol\right)\\n_{SO_2\left(2\right)}=n_{ZnS}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\Sigma n_{O_2}=1\left(mol\right)\\\Sigma n_{SO_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=1\cdot22,4=22,4\left(l\right)\\V_{SO_2}=0,6\cdot22,4=13,44\left(l\right)\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Cho 13(g) Zn tác dụng với 182,5g) dung dịch Hcl 10% .
a,Chất nào còn dư sau phản ứng?tính khối lượng chất dư ?
b, Tính thể tích khí H2 sinh ra (ĐKTC)?
c, Dung dịch sau phản ứng có những chất tan nào? Tính nồng độ phần trăm của các chất đó?
\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(n_{HCl}=\dfrac{182.5\cdot10}{100\cdot36.5}=0.5\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2......0.4..........0.2........0.2\)
\(n_{HCl\left(dư\right)}=0.5-0.4=0.1\left(mol\right)\)
\(m_{HCl\left(dư\right)}=0.1\cdot36.5=3.65\left(g\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{\text{dung dịch sau phản ứng}}=13+182.5-0.2\cdot2=195.1\left(g\right)\)
\(C\%_{HCl\left(dư\right)}=\dfrac{3.65}{195.1}\cdot100\%=1.87\%\)
\(C\%_{ZnCl_2}=\dfrac{0.2\cdot136}{195.1}\cdot100\%=13.94\%\)
Đúng 1
Bình luận (0)
nung 19,5 g zn và 1,6 g s trong môi trường không có không khí sau phản ứng thu đc chất rắn a cho dung dịch hcl 0,5m tác dụng vừa đủ cới a thu được hỗn hợp kí b tính phân trăm thể tích hôc hợp trong khí b
a tính % thế tích các khí trong b
b tính thể tích dung dịc HCl đã tham gia phản ứng
Trời nhanh hộ mình nha mình đang cần gấp
a, Ta có: \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
\(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
PT: \(Zn+S\underrightarrow{t^o}ZnS\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,05}{1}\), ta được Zn dư.
Theo PT: \(n_{Zn\left(pư\right)}=n_{ZnS}=n_S=0,05\left(mol\right)\)
\(\Rightarrow n_{Zn\left(dư\right)}=0,3-0,05=0,25\left(mol\right)\)
- Chất rắn A gồm Zn dư và ZnS.
PT: \(ZnS+2HCl\rightarrow ZnCl_2+H_2S\)
_____0,05___0,1________________0,05 (mol)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,25____0,5__________0,25 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2S}=\dfrac{0,05.22,4}{\left(0,05+0,25\right).22,4}.100\%\approx16,67\%\\\%V_{H_2}\approx83,33\%\end{matrix}\right.\)
b, \(V_{HCl}=\dfrac{0,1+0,5}{0,5}=1,2\left(l\right)\)
Đúng 3
Bình luận (0)























