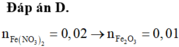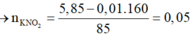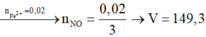Tiến hành điện phân (với điện cực trơ, màng ngăn xốp) một dung dịch chứa hỗn hợp KCl và Cu(NO3)2 cho tới khi nước bắt đầu điện phân ở cả 2 cực thì dừng lại. Ở anot thu được 1,68 lít (đktc) hỗn hợp khí. Thêm tiếp 3,6 gam Fe(NO3)2 vào dung dịch sau điện phân thu được V ml (đktc) khí NO duy nhất và dung dịch A. Cô cạn A rồi nung nóng trong không khí đến khối lượng không đổi thu được 5,85 gam chất rắn. Giá trị gần nhất của V là
A. 250
B. 200
C. 100
D. 150