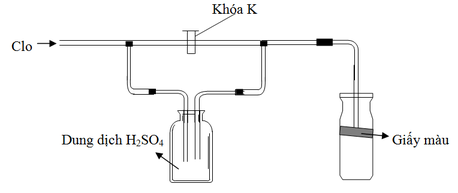
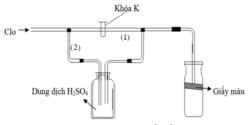
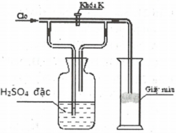
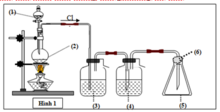
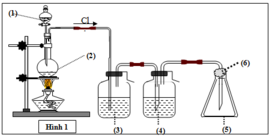
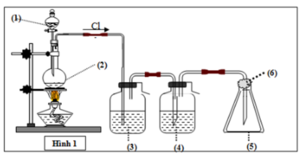
Trong thí nghiệm ở hình bên người ta dẫn khí clo mới điều chế từ MnO2 rắn và dung dịch axit HCl đặc. Trong ống hình trụ có đặt một miếng giấy màu. Hiện tượng gì xảy ra với giấy màu khi lần lượt:
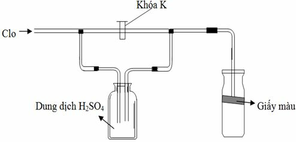
a) Đóng khóa K ; b) Mở khóa K
A. a) Mất màu; b) Không mất màu
B. a) Không mất màu; b) Mất màu
C. a) Mất màu; b) Mất màu
D. a) Không mất màu; b) Không mất màu