Cho 2a mol bột Fe vào dung dịch chứa 5a mol AgNO3, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch gồm các chất
A. Fe(NO3)2và AgNO3
B. Fe(NO3)3 và Fe(NO3)2
C. Fe(NO3)3
D. Fe(NO3)3và AgNO3
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3, khi cá phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm ba muối) và chất rắn Y là một kim loại. Có các nhận định sau:
(a) Dung dịch X chứa: Fe(NO3)3, Mg(NO3)2 và Fe(NO3)2.
(b) Dung dịch X chứa: Fe(NO3)3, AgNO3 và Fe(NO3)2.
(c) Dung dịch X chứa: AgNO3, Mg(NO3)2 và Fe(NO3)2.
(d) Dung dịch X chứa: Fe(NO3)3, Mg(NO3)2 và AgNO3.
Số nhận định đúng là
A. 3.
B. 4.
C. 1.
D. 2.
Đáp án D
Phương pháp: Dựa vào dãy điện hóa (quy tắc α)
Hướng dẫn giải:
Kim loại thu được là Ag. Do thu được 1 KL nên Fe, Mg hết.
Thứ tự các kim loại phản ứng với AgNO 3 : Mg, Fe
TH1:
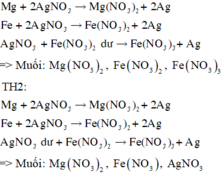
Cho 13,0 gam bột Zn vào dung dịch có chứa 0,1 mol Fe(NO3)3 ; 0,1 mol Cu(NO3)2 và 0,1 mol AgNO3. Khuấy đều cho phản ứng xảy ra hoàn toàn. Tính khối lượng kết tủa thu được sau phản ứng ?
A. 17,2 gam
B. 14,0 gam
C. 19,07 gam
D. 16,4 gam
Chọn đáp án A
Với bài toán kim loại tác dụng với muối các bạn cứ quan niệm là kim loại mạnh nhất sẽ đi nuốt anion của thằng yếu nhất trước.
Ta có
![]()
lượng NO3 này sẽ phân bổ dần cho:
Đầu tiên
![]()
![]()
Và Cu + Ag bị cho ra ngoài hết
![]()
Cho bột Fe vào dung dịch gồm AgNO3 và Fe(NO3)3. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và chất rắn Y gồm hai kim loại. Thành phần muối trong X là
A. Fe(NO3)3 ,Fe(NO3)2
B. AgNO3
C. Fe(NO3)3
D. Fe(NO3)2
Đáp án D
Ta có dãy điện hóa: Fe2+/Fe > Fe3+/Fe2+ > Ag+/Ag.
Thu được 2 kim loại ⇒ Fe và Ag ⇒ X chỉ chứa Fe(NO3)2
cho hỗn hợp rắn gồm Cu và Fe tỉ lệ mol (1:1) vào dung dịch chứa 0,1 mol AgNO3 và 0,14 mol Fe(NO3)3. sau khi các phản ứng xảy ra hoàn toàn, thu được 15,92 gam chất rắn và dung dịch Y. thêm tiếp dung dịch HCl dư vào Y, thu được V lít khí N. biết NO là sản phẩm khử duy nhất của N+5. Gía trị của V là
A.2.016 B. 1.680 C. 1,792 D.1,344
Chất rắn gồm : Ag,Cu dư
\(n_{Ag} = n_{AgNO_3} = 0,1(mol)\\ \Rightarrow n_{Cu} = \dfrac{15,92-0,1.108}{64} = 0,08(mol)\)
Gọi \(n_{Cu} = n_{Fe} = a(mol)\)
Dung dịch sau phản ứng :
\(Fe^{2+} : a + 0,14\\ Cu^{2+} : a - 0,08\\ NO_3^- : 0,1 + 0,14.3 = 0,52(mol)\)
Bảo toàn điện tích : 2(a+0,14) + 2(a -0,08) = 0,52
⇒ a = 0,1
Vậy \(n_{Fe^{2+}} = a + 0,14 = 0,24(mol)\)
Bảo toàn e :
\(n_{Fe^{2+}} = 3n_{NO}\\ \Rightarrow n_{NO} = \dfrac{0,24}{3} = 0,08(mol)\\ \Rightarrow V = 0,08.22,4 = 1,792(lít)\)
Đáp án C
Cho một mảnh Mg vào dung dịch chứa hỗn hợp các muối: Al(NO3)3, Cu(NO3)2, Zn(NO3)2, NaNO3, Fe(NO3)3, AgNO3. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch A và chất rắn B chứa hỗn hợp kim loại. Hãy xác định thành phần các chất có trong dung dịch A và các chất trong B, viết các phương trình phản ứng xảy ra trong các trường hợp sau:
a) Dung dịch A chứa 3 muối.
b) Chất rắn B chứa 4 kim loại.
a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
B chứa các kim loại: Ag, Cu, Fe, Zn
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2
a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
\(3Mg+2Al\left(NO_3\right)_3\rightarrow3Mg\left(NO_3\right)_2+2Al\)
B chứa các kim loại: Ag, Cu, Fe, Zn và có thể có Al
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2
Trộn 8,1 gam bột Al với 35,2 gam hỗn hợp rắn X gồm Fe, Fe3O4, FeO, Fe2O3 và Fe(NO3)2 thu được hỗn hợp Y. Hòa tan hoàn toàn Y vào dung dịch chứa 1,9 mol HCl và 0,15 mol HNO3 khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Z (không chứa ion NH 4 + ) và 0,275 mol hỗn hợp khí T gồm NO và N2O. Cho dung dịch AgNO3 đến dư vào dung dịch Z. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch M; 0,025 mol khí NO (sản phẩm khử duy nhất của N+5) và 280,75 gam kết tủa. Phần trăm khối lượng của Fe(NO3)2 trong Y là
A. 76,70%.
B. 41,57%.
C. 51,14%.
D. 62,35%.
Đáp án B
+ Dung dịch Z phản ứng với dung dịch AgNO3 dư thu được khí NO, chứng tỏ trong Z có Fe2+, H+ và không còn NO 3 -
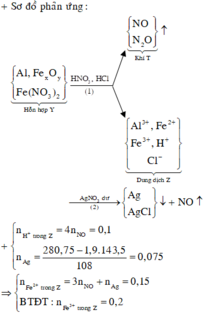

Trộn 8,1 gam bột Al với 35,2 gam hỗn hợp rắn X gồm Fe, Fe3O4, FeO, Fe2O3 và Fe(NO3)2 thu được hỗn hợp Y. Hòa tan hoàn toàn Y vào dung dịch chứa 1,9 mol HCl và 0,15 mol HNO3 khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Z (không chứa ion N H 4 + ) và 0,275 mol hỗn hợp khí T gồm NO và N2O. Cho dung dịch AgNO3 đến dư vào dung dịch Z. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch M; 0,025 mol khí NO (sản phẩm khử duy nhất của N+5) và 280,75 gam kết tủa. Phần trăm khối lượng của Fe(NO3)2 trong Y là
A. 76,70%.
B. 41,57%.
C. 51,14%.
D. 62,35%.
Cho 0,03 mol Al và 0,05 mol Fe tác dụng với 100ml dung dịch X chứa Cu(NO3)2 và AgNO3. Sau phản ứng thu được dung dịch Y và 8,44 gam chất rắn Z gồm 3 kim loại. Cho chất rắn Z tác dụng với dung dịch HCl dư thu được 0,84 lít H2 (đkc). Cho biết các phản ứng xảy ra hoàn toàn. CM của Cu(NO3)2 và AgNO3 trong X là
A. 0,4M và 0,2M
B. 0,5M và 0,3M
C. 0,3M và 0,7M
D. 0,4M và 0,35M
Đáp án D
Z chứa 3 kim loại là Cu, Ag và Fe dư.
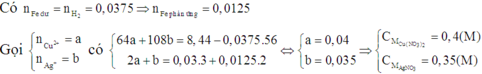
Cho bột Cu vào dung dịch Fe(NO3)3 (dư), sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X. Cho các chất sau: Cl2, AgNO3, HCl, Fe, BaO, KOH. Số chất tác dụng được với dung dịch X là
A. 3
B. 4
C. 5
D. 6
Trộn 8,1g bột Al với 35,2g hỗn hợp rắn X gồm Fe, Fe3O4 ,FeO, Fe2O3 và Fe(NO3)2 thu được hỗn hợp Y. Hoà tan hoàn toàn Y vào dung dịch chứa 1,9mol HCl và 0,15mol HNO3 khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Z (không chứa ion NH4+) và 0,275 mol hỗn hợp khí T gồm NO và N2O.Cho dung dịch AgNO3 đến dư vào dung dịch Z. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch M; 0,025mol khí NO( sản phẩm khử duy nhất của N+5) và 280,75g kết tủa. Phần trăm khối lượng của Fe(NO3)2 trong Y là:
A. 76,70%
B. 41,57%
C. 51,14%
D. 62,35%
Đáp án : B
Z + AgNO3 -> NO => H+ dư , NO3- hết ; Z có Fe2+
Kết tủa gồm : nAgCl = nHCl = 1,9 mol => nAg = 0,075 mol
Bảo toàn e : nFe2+ = 3nNO + nAg = 0,15 mol
, nH+ dư = 4nNO = 0,1 mol
Trong dung dịch Z gồm : Al3+ ; Fe2+ ; Fe3+ ; H+ ; Cl-
Bảo toàn điện tích : nAl + 2nFe2+ + 3nFe+ + nH+ = nCl- => nFe3+ = 0,2 mol
=> nFe (Y) = 0,35 mol
Bảo toàn H : nH2O = ½ nH+ pứ = 0,975 mol
Bảo toàn O : nO(Y) + nHNO3 = nO(T) + nH2O
=> nO(Y) = 0,8 mol
Ta có : mY = mAl + mnguyên tố Fe + mO + mN
=> nN = 0,2 mol => nFe(NO3)2 = 0,1 mol
=> %mFe(NO3)2 = 41,57%