Khử hoàn toàn một oxit sắt ở nhiệt độ cao cần vừa đủ V lít khí CO dư (đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Công thức của X và giá trị V lần lượt là
A. Fe3O4 và 0,224
B. FeO và 0,224
C. Fe2O3 và 0,448
D. Fe3O4 và 0,448
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí C O 2 . Công thức của X và giá trị V lần lượt là
A. F e 3 O 4 và 0,224.
B. F e 3 O 4 và 0,448.
C. FeO và 0,224.
D. F e 2 O 3 và 0,448.
Đặt X:
F e x O y T a c ó n O ( x ) = n C O 2 = n C O = 0 , 02 m o l → V = 0 , 02 . 22 , 4 = 0 , 448 l í t . x : y = n F e : n O ( X ) = 0 , 015 : 0 , 02 = 3 : 4 . V ậ y X l à F e 3 O 4 .
Chọn đáp án B.
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Oxit sắt X và giá trị của V lần lượt là:
A. Fe3O4 và 0,224
B. Fe3O4 và 0,448
C. FeO và 0,224
D. Fe2O3 và 0,448
Đáp án B
Đặt công thức oxit sắt là FexOy
FexOy+ yCO → xFe + yCO2
nFe= 0,84/56= 0,015 mol
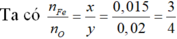
→Công thức oxit là Fe3O4
Ta có: nCO= nCO2= 0,02 mol
→ V= 0,02.22,4= 0,448 lít
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở điều kiện tiêu chuẩn), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. a. Tìm công thức của X và giá trị V. b. Hỗn hợp Y gồm X, FeO và Ag (trong đó nguyên tố oxi chiếm 19,2% theo khối lượng). Cho m gam Y tác dụng với 1500 ml dung dịch HCl 3M (dư), thu được dung dịch Z và còn lại 0,248m gam chất rắn không tan. Cho dung dịch Z tác dụng với dung dịch NaOH dư thu được kết tủa T. Đem nung T ngoài không khí đến khối lượng không đổi thu được 100 gam chất rắn khan. Tính m và phần trăm khối lượng từng chất trong hỗn hợp Y. Giúp e với👉👈
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 1,12 gam Fe và 0,03 mol khí CO2. Công thức của X và giá trị V lần lượt là
A. Fe3O4 và 0,224
B. Fe2O3 và 0,672
C. Fe3O4 và 0,448
D. FeO và 0,224
Đáp án B.
Đặt công thức oxit sắt là FexOy
Ta có: nFe= 1,12/56= 0,02mol
FexOy+ yCO → xFe+ yCO2
Theo PTHH:
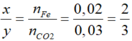
→ Oxit là Fe2O3
Ta có: nCO= nCO2= 0,03 mol→ V= 0,03.22,4= 0,672 lít
Cho11,6 gam oxit sắt từ Fe3O4 phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Fe và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V. b/ Tính khối lượng Fe thu được sau phản ứng.
Theo gt ta có: $n_{Fe_3O_4}=0,05(mol)$
$Fe_3O_4+4H_2\rightarrow 3Fe+4H_2O$
Ta có: $n_{H_2}=0,05.4=0,2(mol)\Rightarrow V_{H_2}=4,48(l)$
\(Fe3O4+4h2->3Fe+4H2O\)
a) n \(Fe3O4\\\)=\(\dfrac{11.6}{232}\)=0.05 mol
V\(H2=0,05.22,4=1,12l\)
b)n \(Fe=\dfrac{0.05\cdot3}{1}=0.15mol\)
m\(Fe=n.M=0,15\cdot56=8,4gam\)
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là:
A. 18,560; 19,700 và 0,91 mol.
B. 20,880; 19,700 và 0,81 mol.
C. 18,560; 20,685 và 0,81 mol.
D. 20,880; 20,685 và 0,91 mol.
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m 1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N + 5 , đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là
A. 18,560; 19,700 và 0,91
B. 20,880; 19,700 và 0,81
C. 18,560; 20,685 và 0,81
D. 20,880; 20,685 và 0,91
Đáp án D
Quy đổi A chỉ gồm Fe3O4 + CO → 19,2 gam (Fe : x mol + O : y mol) + CO2
19,2 gam (Fe : x mol + O : y mol) + HNO3 → Fe(NO3)3 + NO + H2O
Ta có hệ phương trình
(1) 56x + 16y = 19,2
(2) ĐLBT mol e : 3x = 2y + 0,1*3
→ x = 0,27 ; y = 0,255 → n(Fe3O4) = 0,09 mol → m1 = 20,880 gam
→ n(CO2) = n(CaCO3) = 0,09*4 – 0,255 = 0,105 → m2 = 20,685 gam
n(HNO3) = 0,27*3 + 0,1 = 0,91 mol
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là:
A. 18,560; 19,700 và 0,91 mol.
B. 20,880; 19,700 và 0,81 mol.
C. 18,560; 20,685 và 0,81 mol.
D. 20,880; 20,685 và 0,91 mol.
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là:
A. 18,560; 19,700 và 0,91 mol.
B. 20,880; 19,700 và 0,81 mol.
C. 18,560; 20,685 và 0,81 mol.
D. 20,880; 20,685 và 0,91 mol.
Đáp án là D.
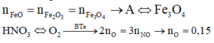
![]()
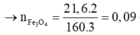
![]()
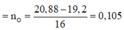
=> m 2 = 20,865 gam
![]()
= 3,3.0,09 + 0,1 = 0,91 mol