Cho phản ứng oxi hóa khử giữa Al và HNO3 tạo sản phẩm khử duy nhất là N2O .Tỉ lệ số phân tử HNO3 tạo muối với số phân tử HNO3 làm chất oxi hóa là
A. 1 : 6
B. 8 : 3
C. 4 : 1
D. 5: 1
Cho phản ứng oxi hóa – khử giữa Al và HNO3 tạo sản phẩm khử duy nhất là N2O. Tỉ lệ số phân tử HNO3 tạo muối với số phân tử HNO3 đóng vai trò oxi hóa là?
A. 1:6
B. 4: 1
C. 5: 1
D. 8:3
Đáp án B
Phương pháp : Cân bằng phương trình bằng phương pháp thăng bằng electron.
Hướng dẫn giải:
8Al + 30HNO3 → 8Al(NO3)3 + 3N2O+ 15H2O
Số phân tử HNO3 môi trường = 24
Số phân tử HNO3 oxi hóa = 6
=> Tỉ lệ 4 :1
Cho phản ứng oxi hóa – khử giữa Al và HNO3 tạo sản phẩm khử duy nhất là N2O. Tỉ lệ số phân tử HNO3 tạo muối với số phân từ HNO3 đóng vai trò oxi hóa là?
A. 1:6
B. 8:3
C. 4:1
D. 5:1
Đáp án là C
Ta có PTPƯ:
8Al +30HNO3 → 8Al(NO3)3 +3N2O + 15H2O
Số phân tử HNO3 môi trường là 8x3=24
Sô phân tử HNO3 oxi hóa là 6
→Tỉ lệ 4:1
Cho phản ứng oxi hóa – khử giữa Al và HNO3 tạo sản phẩm khử duy nhất là N2O. Tỉ lệ số phân tử HNO3 tạo muối với số phân từ HNO3 đóng vai trò oxi hóa là?
A. 1:6
B. 8:3
C. 4:1
D. 5:1
Đáp án là C
Ta có PTPƯ:
8Al +30HNO3 → 8Al(NO3)3 +3N2O + 15H2O
Số phân tử HNO3 môi trường là 8x3=24
Sô phân tử HNO3 oxi hóa là 6
→Tỉ lệ 4:1
Cho phản ứng oxi hóa khử giữa M(chỉ có hóa trị 2) và HNO3 tạo ra sản phẩm khử duy nhất là NO. Tỉ lệ số phân tử HNO3 tạo muối với số phân tử HNO3 đóng vai trò oxi hóa là: A. 3:1 B. 5:1 C. 1:6 D. 8:3
3M + 8HNO3 --> 3M(NO3)2 + 2NO + 4H2O
=> Số phân tử HNO3 tạo muối = 6
=> Số phân tử HNO3 đóng vai trò chất oxh = 2
=> Tỉ lệ 3 : 1
=> A
3M + 8HNO3 --> 3M(NO3)2 + 2NO + 4H2O
=> Số phân tử HNO3 tạo muối = 6
=> Số phân tử HNO3 đóng vai trò chất oxh = 2
=> Tỉ lệ 3 : 1
=> A
Trong phản ứng: Al + HNO3 (loãng) → Al(NO3)3 + N2O + H2O, tỉ lệ giữa số nguyên tử Al bị oxi hoá và số phân tử HNO3 bị khử (các số nguyên, tối giản) là
A. 8 và 30
B. 4 và 15
C. 8 và 6
D. 4 và 3
Đáp án D
Số phân tử bị khử chính bằng số phân tử N2O
8Al + 30HNO3 (loãng) → 8Al(NO3)3 + 3N2O + 15H2O
Trong phản ứng: Al + HNO3 (loãng à Al(NO3)3 + N2O + H2O, tỉ lệ giữa số nguyên tử Al bị oxi hoá và số phân tử HNO3 bị khử (các số nguyên, tối giản) là:
A. 8 và 6
B. 4 và 15
C. 4 và 3
D. 8 và 30
Đáp án : A
Số phân tử bị khử chính bằng số phân tử N2O
8Al + 30HNO3 à 8Al(NO3)3 + 3N2O + 15H2O
Trong phản ứng: Al + HNO 3 loãng → Al ( NO 3 ) 3 + N 2 O + H 2 O , tỉ lệ giữa số nguyên tử Al bị oxi hoá và số phân tử HNO 3 bị khử (các số nguyên, tối giản) là
A. 4 và 3
B. 8 và 30
C. 4 và 15
D. 8 và 6
Cho phương trình phản ứng:
Mg + HNO3→Mg(NO3)2+ NO + N2O + H2O.
Tỉ khối của hỗn hợp NO và N2O đối với H2 là 19,2. Tỉ lệ số phân tử bị khử và bị oxi hóa trong phản ling trên là:
A. 8 :15.
B. 6:11.
C. 11 : 28.
D. 38 : 15.
Đáp ánA
Chọn 1 mol hỗn hợp khí NO và N2O.
Gọi

Theo định luật bảo toàn mol electron:
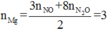
Áp dụng định luật bảo toàn nguyên tố cho nitơ có:
![]()
Vậy tỉ lệ số phân tử bị khử và bị oxi hóa trong phản
ứng là: ![]()
Cho phương trình phản ứng: Mg + HNO3 → Mg(NO3)2 + NO + N2O + H2O. Nếu tỉ khối của hỗn hợp NO và N2O đối với H2 là 19,2. Ti lệ số phân tử bị khử và bị oxi hóa là
A. 11 : 28
B. 8 : 15
C. 38 : 15
D. 6 : 11
Phương trình:
15 Mg + 38 HNO3 -> 15 Mg[NO3]2 + 2NO + 3 N2O + 19 H2O => ti lệ: (3.2 + 2)/15 = 8/15
=> Đáp án B