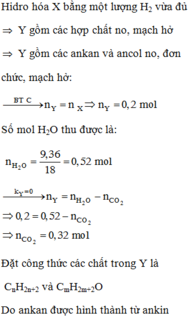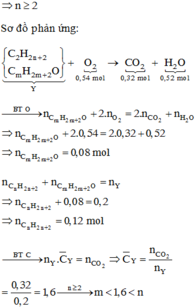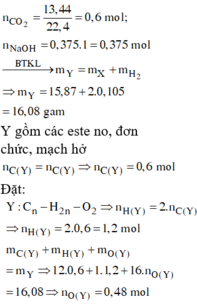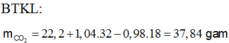X, Y là hai axit đều đơn chức, Z là este thuần chức, mạch hở được tạo bởi X, Y và glixerol. Đốt cháy hoàn toàn 22,72 gam hỗn hợp E chứa X, Y, Z cần dùng 1,05 mol O2, thu được 11,88 gam nước. Mặt khác hidro hóa hoàn toàn 22,72 gam E cần dung 0,19 mol H2 ( xúc tác Ni, t0), thu được hỗn hợp T. Đun nóng toàn bộ T với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được m gam rắn khan. Giá trị của m là : A. 30,46 B. 30,84 C. 28,32 D. 28,86
Đọc tiếp
X, Y là hai axit đều đơn chức, Z là este thuần chức, mạch hở được tạo bởi X, Y và glixerol. Đốt cháy hoàn toàn 22,72 gam hỗn hợp E chứa X, Y, Z cần dùng 1,05 mol O2, thu được 11,88 gam nước. Mặt khác hidro hóa hoàn toàn 22,72 gam E cần dung 0,19 mol H2 ( xúc tác Ni, t0), thu được hỗn hợp T. Đun nóng toàn bộ T với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được m gam rắn khan. Giá trị của m là :
A. 30,46
B. 30,84
C. 28,32
D. 28,86