Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hòa của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Số muối của kim loại M thỏa mãn là
A. 2
B. 3
C. 1
D. 0
Nhúng thanh Mg vào dung dich chứa 0,1 mol muối sunfat trung hòa của một kim loại M , sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Số muối của kim loại M thỏa mãn là
A. 2
B. 0.
C. 3
D. 1
Muối sunfat có thể mang hóa trị 1, 2 hoặc 3.
Xét lần lượt 3 trường hợp:
TH1: muối sunfat hóa tri II
Mg + XSO4 -> MgSO4 + X2+
0,1 0,1 0,1
Khối lượng tăng lên là 4 gam nên MX = 4 : 0,1 + 24 = 64 => Cu => Thỏa mãn
TH2: muối sunfat hóa tri I:
Mg + XSO4 -> MgSO4 + 2X+
0,1 0,2
=>MX = 4 : 0,2 + 24 = 44 => không thỏa mãn
Tương tự TH muối sunfat hóa tri III, không có kim loại thỏa mãn => Đáp án D
Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hòa của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Sô muối của kim loai M thoả mãn là
A. 1
B. 0
C. 3
D. 2
TH1: Nếu M có hóa trị II
ta có Mg + MSO4 → MgSO4 + M
=> m tăng = mM – mMg => 0,1M -2,4 = 4 => M=64 (Cu)
TH2: Nếu M có hóa trị khác II
ta có xMg + M2(SO4)x →x MgSO4 + 2M
=> m tăng = 0,2M – 2,4x = 4 + Nếu x=1
=> M = 32 (loại) + Nếu x=3 => M = 56 (Fe)
TH3: nếu M có hóa trị IV
=> tạo muối M(SO4)2 m tăng = 0,1M – 4,8 = 4
=> M= 88 (loại) Chỉ có 2 kim loại thỏa mãn =>D
Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hoà của một kim loại R, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Số muối của kim loại R thoả mãn là
$nMg + R_2(SO_4)_n \to nMgSO_4 + 2R$
Theo PTHH :
$n_R = 0,2(mol)$
$n_{Mg} = 0,1n(mol)$
Suy ra: $0,2.R - 0,1n.24 = 4$
$\Rightarrow R - 12n = 20$
Với n = 1 thì R = 32(loại)
Với n = 2 thì R = 44(loại)
Với n = 3 thì R = 56(Fe)
\(\text{TH1: Muối hoá trị 2}\\ Mg+RSO_4 \to MgSO_4+R\\ n_{Mg}=n_R=0,1(mol)\\ m_{tăng}=0,1.M_R+24.0,1=4\\ \Rightarrow M_r=64(Cu) \text{TH1: Muối hoá trị 3}\\ nMg+R_2(SO_4)_n \to nMgSO_4+2R\\ n_{Mg}=\frac{0,2}{n}(mol)\\ m_{tăng}=0,2.M_R+24.0,1.n=4\\ n=3; R=56 (Fe) \)
Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hòa của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Phản trăm khối lượng của M trong oxit cao nhất là
A. 35%.
B. 29%.
C. 40%.
D. 80%.
Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hòa của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Phản trăm khối lượng của M trong oxit cao nhất là
A. 35%.
B. 29%.
C. 40%.
D. 80%.
Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hòa của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Phần trăm khối lượng của M trong oxit cao nhất là
A. 35%
B. 29%
C. 40%
D. 70%
Nhúng thanh kim loại Mg có khối lượng m gam vào dung dịch chứa 0,2 mol CuSO4, sau một thời gian lấy thanh kim loại ra, thấy khối lượng CuSO4đã tham gia phản ứng là 80%. Thanh kim loại sau khi lấy ra đem đốt cháy trong O2dư, thu được (m + 12,8) gam chất rắn (cho rằng Cu giải phóng bám hết vào thanh Mg). Khối lượng thanh kim loại sau khi lấy ra khỏi dung dịch CuSO4 là
A. 10,24 gam
B. 12,00 gam
C. 16,00 gam
D. 9,60 gam

Số mol: 0,16......0,16.............................0,16
Sau phản ứng với dung dịch CuSO4 khối lượng thanh kim loại là
![]()
Thanh kim loại sau khi lấy ra có x mol Mg dư và 0,16 mol Cu
Khi đốt trong oxi dư:
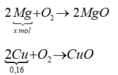
mO2 = (m + 12,8) – (m + 6,4) = 6,4 → nO2 = 0,2 mol
0,5 x + 0,08 = 0,2 → x = 0,24 mol
Khối lượng thanh kim loại sau khi lấy ra khỏi dung dịch CuSO4 là
0,24 . 24 + 0,16 . 64 = 16 gam
Đáp án C
Nhúng thanh kim loại Mg có khối lượng m gam vào dung dịch chứa 0,2 mol CuSO4, sau một thời gian lấy thanh kim loại ra, thấy khối lượng CuSO4đã tham gia phản ứng là 80%. Thanh kim loại sau khi lấy ra đem đốt cháy trong O2dư, thu được (m + 12,8) gam chất rắn (cho rằng Cu giải phóng bám hết vào thanh Mg). Khối lượng thanh kim loại sau khi lấy ra khỏi dung dịch CuSO4 là
A. 10,24 gam
B. 12,00 gam
C. 16,00 gam
D. 9,60 gam
Nhúng một thanh Mg vào dung dịch có chứa 0,8 mol Fe NO 3 3 và 0,05 mol Cu NO 3 2 . Sau một thời gian, lấy thanh kim loại ra, rửa sạch, cân lại thấy khối lượng tăng 11,6 gam so với thanh kim loại ban đầu. Khối lượng Mg đã phản ứng là:
A. 20,88 gam
B. 6,96 gam
C. 24 gam
D. 25,2 gam