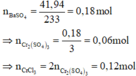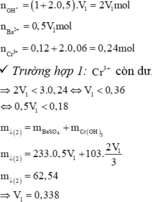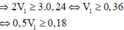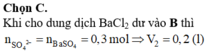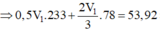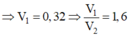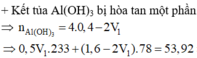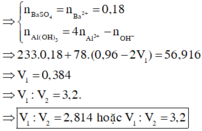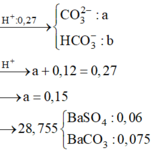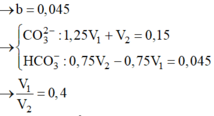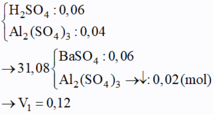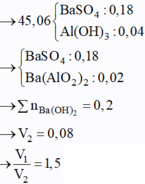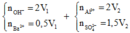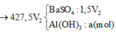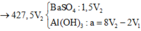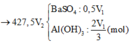Cho hai dung dịch : dung dịch A chứa NaOH 1M và Ba(OH)2 0,5M, dung dịch B chứa CrCl3 1M và Cr2(SO4)3 0,5M
- Cho V1 lít dung dịch A vào V2 lít dung dịch B thu được 62,54 gam kết tủa
- Cho BaCl2 dư vào dung dịch B thì thu được 41,94 gam kết tủa.
Giá trị nhỏ nhất của V1 gần nhất với giá trị nào sau đây ?
A. 0,38
B. 0,26
C. 0,28
D. 0,34