Cho từ từ đến dư dung dịch NaOH vào dung dịch CuSO4, ta thấy:
A. Có kết tủa xanh, kết tủa không tan
B. Có kết tủa trắng và có khí bay ra
C. Tạo kết tủa trắng xanh sau chuyển thành kết tủa đỏ nâu.
D. Tạo kết tủa xanh sau đó kết tủa tan.
Tiến hành thí nghiệm với các dung dịch muối clorua riêng biệt của các cation: X2+, Y3+, Z3+, T2+. Kết quả ghi được ở bảng sau:
Mẫu thử chứa Thí nghiệm Hiện tượng
X2+ Tác dụng với Na2SO4 trong H2SO4 loãng. Có kết tủa trắng.
Y3+ Tác dụng với dung dịch NaOH. Có kết tủa nâu đỏ.
Z3+ Nhỏ từ từ dung dịch NaOH loãng vào đến dư. Có kết tủa keo trắng, sau đó kết tủa tan.
T2+ Nhỏ từ từ dung dịch NH3 vào đến dư. Có kết tủa xanh, sau đó kết tủa tan tạo thành dung dịch có màu xanh lam.
Các cation X2+, Y3+, Z3+, T2+ lần lượt là:
A. Ba2+, Cr3+, Fe2+, Mg2+.
B. Ba2+, Fe3+, Al3+, Cu2+.
C. Ca2+, Au3+, Al3+, Zn2+.
D. Mg2+, Fe3+, Cr3+,Cu2+.
Chọn đáp án B.
Mẫu thử chứa Thí nghiệm Hiện tượng
Ba2+ Tác dụng với Na2SO4 trong H2SO4 loãng.
Có kết tủa trắng.
Fe3+ Tác dụng với dung dịch NaOH.
Có kết tủa nâu đỏ.
Al3+ Nhỏ từ từ dung dịch NaOH loãng vào đến dư.
Có kết tủa keo trắng, sau đó kết tủa tan.
Cu2+ Nhỏ từ từ dung dịch NH3 vào đến dư.
Có kết tủa xanh, sau đó kết tủa tan tạo thành dung dịch có màu xanh lam.
Tiến hành thí nghiệm với các dung dịch muối clorua riêng biệt của các cation: X2+, Y3+, Z3+, T2+ . Kết quả ghi được ở bảng sau:
| Mẫu thử chứa |
Thí nghiệm |
Hiện tượng |
| X2+ |
Tác dụng với Na2SO4 trong H2SO4 loãng. |
Có kết tủa trắng. |
| Y3+ |
Tác dụng với dung dịch NaOH. |
Có kết tủa nâu đỏ. |
| Z3+ |
Nhỏ từ từ dung dịch NaOH loãng vào đến dư. |
Có kết tủa keo trăng, sau đó kết tủa tan. |
| T2+ |
Nhỏ từ từ dung dịch NH3 vào đến dư. |
Có kết tủa xanh, sau đó kết tủa tan tạo thành dung dịch có màu xanh lam.
|
Các cation X2+, Y3+, Z3+, T2+ lần lượt là:
A. Ba2+ , Cr3+, Fe2+, Mg2+.
B. Ba2+, Fe3+ , Al3+ , Cu2+.
C.Ca2+, Au3+, Al3+, Zn2+.
D. Mg2+, Fe3+, Cr3+ ,Cu2+.
Tiến hành thí nghiệm với các dung dịch muối clorua riêng biệt của các cation: X2+, Y3+, Z3+, T2+. Kết quả ghi được ở bảng sau:
| Mẫu thử chứa |
Thí nghiệm |
Hiện tượng |
| X2+ |
Tác dụng với Na2SO4 trong H2SO4 loãng |
Có kết tủa trắng |
| Y3+ |
Tác dụng với dung dịch NaOH |
Có kết tủa nâu đỏ |
| Z3+ |
Nhỏ từ từ dung dịch NaOH loãng vào đến dư |
Có kết tủa keo trăng, sau đó kết tủa tan. |
| T2+ |
Nhỏ từ từ dung dịch NH3 vào đến dư |
Có kết tủa xanh, sau đó kết tủa tan tạo thành dung dịch có màu xanh lam |
Các cation X2+, Y3+, Z3+, T2+ lần lượt là:
A. Ba2+, Cr3+, Fe3+, Mg2+.
B. Ba2+, Fe3+, Al3+, Cu2+.
C. Ca2+, Au+, Al3+, Zn2+.
D. Mg2+, Fe3+, Cr3+, Cu2+.
Tiến hành thí nghiệm với các dung dich muối clorua riêng biệt của các cation: X2+, Y3+, Z3+, T2+. Kết quả được ghi ở bảng sau:
| Mẫu thử chứa |
Thí nghiệm |
Hiện tượng |
| X2+ |
Tác dụng với Na2SO4 trong H2SO4 loãng |
Có kết tủa trắng |
| Y3+ |
Tác dụng với dung dịch NaOH. |
Có kết tủa nâu đỏ |
| Z3+ |
Nhỏ từ từ dung dịch NaOH loãng vào đến dư |
Có kết tủa keo trắng, sau đó kết tủa tan |
| T2+ |
Nhỏ từ từ dung dịch NH3 vào đến dư. |
Có kết tủa xanh, sau đó kết tủa tan tạo dung dịch màu xanh lam. |
Các cation X2+, Y3+, Z3+, T2+ lần lượt là
A. Ba2+, Fe3+, Al3+, Cu2+
B. Ca2+, Au3+, Al3+, Zn2+.
C. Ba2+, Cr2+, Fe3+, Mg2+
D. Mg2+, Fe3+, Cr3+, Cu2+
Đáp án A
Ta thấy X2+ chỉ có thể là Ba2+ do tạo kết tủa sunfat là BaSO4 màu trắng và không tan trong axit.
Y3+ chỉ có thể là Fe3+ do tạo kết tủa Fe(OH)3 màu nâu đỏ.
Z3+ là Al3+ do ban đầu tạo kết tủa keo trắng Al(OH)3 và kết tủa này tan trong kiềm dư.
T3+ là Cu2+ do ban đầu tạo kết tủa xanh Cu(OH)2 nhưng bị hoà tan bởi NH3 do tạo phức.
Tiến hành thí nghiệm với các dung dich muối clorua riêng biệt của các cation: X 2 + , Y 3 + , Z 3 + , T 2 + . Kết quả được ghi ở bảng sau:
| Mẫu thử chứa |
Thí nghiệm |
Hiện tượng |
| X 2 + |
Tác dụng với Na2SO4 trong H2SO4 loãng. |
Có kết tủa trắng. |
| Y 3 + |
Tác dụng với dung dịch NaOH. |
Có kết tủa nâu đỏ. |
| Z 3 + |
Nhỏ từ từ dung dịch NaOH loãng đến dư. |
Có kết tủa keo trắng, sao đó kết tủa tan. |
| T 2 + |
Nhỏ từ từ dung dịch NH3 vao đến dư. |
Có kết tủa xanh, sau đó kết tủa tan tạo dung dịch mau xanh lam. |
Các cation X 2 + , Y 3 + , Z 3 + , T 2 + lần lượt là
![]()
![]()
![]()
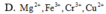
Chọn C.
Phản ứng: a, b, d, f,
(a). 2NaHCO3 + KOH → Na2CO3 + K2CO3 + 2H2O
(b). Fe + 2AgNO3 → Fe(NO3)2 + 2Ag; Fe(NO3)2 + AgNO3 → Ag + Fe(NO3)3.
(c). CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O.
Ngoài ra có NaOH dư.
(d). ClNH3-CH2-COOH + 2NaOH → NaCl + 2H2O + NH2CH2COONa.
(e). Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O; 2FeCl3 + Cu → 2FeCl2 + CuCl2,
Ngoài ra còn có HCl dư.
(f). CO2 + 2NaOH → Na2CO3 + H2O
CO2 + Na2CO3 + H2O → 2NaHCO3.
Có Na2CO3 dư và NaHCO3.
(g). 14HCl + K2Cr2O7 → 3Cl2 + 2CrCl3 + 2KCl + 7H2O
Cho dung dịch NaOH vào dung dịch CuSO4,hiện tượng quan sát được là: A. Xuất hiện kết tủa xanh. B. Xuất hiện kết tủa trắng,khí thoát ra. C. sủi bọt khí. D. .Xuất hiện kết tủa nâu đỏ.
Cho dung dịch NaOH vào dung dịch CuSO4,hiện tượng quan sát được là: A. Xuất hiện kết tủa xanh. B. Xuất hiện kết tủa trắng,khí thoát ra. C. sủi bọt khí. D. .Xuất hiện kết tủa nâu đỏ.
Kết tủa là \(Cu\left(OH\right)_2\downarrow\) màu xanh.
Cho kim loại A tác dụng với một dd Muối B. Viết PTHH xảy ra trong trường hợp sau: Sau khi phản ứng kết thúc, được chất khí và dung dịch K. Chia dung dịch K làm 2 phần: Sục từ từ khí \(_{CO_2}\)đến dư vào phần 1 thấy tạo thành kết tủa. Sục từ từ khí HCl vào phần 2 cũng thấy tạo thành kết tủa, sau đó kết tủa tan khi HCl dư tạo thành dung dịch Y trong suốt. Nhỏ tiếp dung dịch NaOH từ từ vào Y thấy kết tủa tạo thành, sau đó tan trong dung dịch NaOH dư.
Kim loại A : Natri hoặc Canxi hoặc Bari hoặc Kali (chọn Natri làm VD)
Muối B : Muối tan của Al hoặc Zn ( chon AlCl3 làm VD)
PTHH : \(2Na+2H_2O-->2NaOH+H_2\uparrow\)
\(NaOH+AlCl_3-->NaCl+Al\left(OH\right)_3\downarrow\)
\(NaOH+Al\left(OH\right)_3-->NaAlO_2+2H_2O\)
Phần 1 : \(CO_2+NaAlO_2+2H_2O-->NaHCO_3+Al\left(OH\right)_3\downarrow\)
Phần 2 : \(HCl+NaAlO_2+H_2O-->NaCl+Al\left(OH\right)_3\)
\(3HCl+Al\left(OH\right)_3-->AlCl_3+3H_2O\)
\(NaOH+AlCl_3-->NaCl+Al\left(OH\right)_3\downarrow\)
\(NaOH+Al\left(OH\right)_3-->NaAlO_2+2H_2O\)
cái này chỉ là VD thôi, các trường hợp kia viết pthh tương tự
hòa tan chất bột ít màu trắng dùng nhiều trong xây dựng vào nước ta được dung dịch A có tính kiềm ,thải khí CO2 dư vài dung dịch A ban đầu thấy xuất hiện kết tủa ,sau đó kết tủa tan tạo thành dd B. Cho dd NaOH dư vào dd B xuất hiện kết tủa I. Nung kết tủa I thì thu được chất bột ít .Xác định các chất X,Y,A,B và viết PTHH cho các hiện tượng trên Giải giúp mik vs mik cần gấp
Có các nhận xét sau:
(a) Nhúng thanh Fe vào dung dịch FeCl3 xảy ra ăn mòn điện hóa.
(b) Sục khí H2S vào dung dịch CuSO4 thấy xuất hiện kết tủa xanh nhạt.
(c) Nhỏ dung dịch Na2CO3 vào dung dịch FeCl3 thấy xuất hiện kết tủa nâu đỏ và khí.
(d) Nhúng thanh Al vào dung dịch NaOH loãng nguội, thấy thanh Al tan dần.
(e) Đốt dây sắt trong khí Cl2 thấy tạo thành muối Fe (II) bám trên dây sắt.
Số nhận xét đúng là
A. 1
B. 2
C. 3
D. 4
Chọn B.
(a) Sai, Nhúng thanh Fe vào dung dịch FeCl3 xảy ra ăn mòn hoá học.
(b) Sai, Sục khí H2S vào dung dịch CuSO4 thấy xuất hiện kết tủa đen của CuS.
(c) Đúng, 3Na2CO3 + 2FeCl3 + 3H2O ® 2Fe(OH)3 + 3CO2 + 6NaCl.
(d) Đúng.
(e) Sai, Đốt dây sắt trong khí Cl2 thấy tạo thành muối Fe (III) bám trên dây sắt.
Cho các dung dịch sau: Ba(HCO3)2, NaOH, AlCl3, KHSO4 được đánh số ngẫu nhiên là X, Y, Z, T. Tiến hành các thí nghiệm sau:
| Hóa chất |
X |
Y |
Z |
T |
| Quỳ tím |
Xanh |
Đỏ |
Xanh |
Đỏ |
| Dung dịch HCl |
Khí bay ra |
Đồng nhất |
Đồng nhất |
Đồng nhất |
| Dung dịch Ba(OH)2 |
Kết tủa trắng |
Kết tủa trắng |
Đồng nhất |
Kết tủa trắng, sau tan |
Dung dịch chất Y là
A. AlCl3.
B. KHSO4.
C. Ba(HCO3)2.
D. NaOH.
Đáp án B
X là Ba(HCO3)2
Y là KHSO4
Z là NaOH
T là AlCl3