Hòa tan hoàn toàn 10 gam hỗn hợp X gồm 2 kim loại (đứng trước H trong dãy điện hóa) bằng dung dịch HCl dư thu được 2,24 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được lượng muối khan là:
A. 1,71
B. 17,1
C. 13,55
D. 34,2
Hỗn hợp X gồm 2 kim loại A và B thuộc phân nhóm chính nhóm II, ở 2 chu kỳ liên tiếp. Cho 1,76 gam X tan hoàn toàn trong dung dịch HCl dư thu được 1,344 lít khí H 2 (đktc). Cô cạn dung dịch sau phản ứng, khối lượng muối khan thu được là
A. 6,02 gam
B. 3,98 gam
C. 5,68 gam
D. 6,58 gam
Hoà tan hoàn toàn 11,2 gam hỗn hợp 2 kim loại A, B trong dung dịch HCl dư thu được 8.96 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. a, Tính m?
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ \Rightarrow n_{HCl}=2.n_{H_2}=2.0,4=0,8\left(mol\right)\\ Ta.có:m=m_{muối}=m_{kl}+\left(m_{HCl}-m_{H_2}\right)=11,2+\left(0,8.36,5-0,4.2\right)=39,6\left(g\right)\)
Hòa tan hoàn toàn 10g hỗn hợp 2 kim loại trong dung dịch HCl dư thấy tạo ra 2,24 lít khí H2(đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị m là:
Áp dụng định luật bảo toàn khối lượng ta có:
\(m=m_{ACl_n}+m_{BCl_m}=m_{A+B}+m_{HCl}-m_{H_2}\)
Áp dụng bảo toàn nguyên tố:
nHCl phản ứng = 2nH2 = 0,2 mol
Ta có m = 10 + 0,2 x 36,5 - 0,2 = 17,1 (g)
Chọn đáp án B
Hòa tan hoàn toàn 23,8 gam hỗn hợp một muối cacbonat của các kim loại hóa trị I và muối cacbonat của kim loại hóa trị II trong dung dịch HCl. Sau phản ứng thu được 4,48 lít khí (đktc). Đem cô cạn dung dịch thu được thì khối lượng muối khan là:
A. 13 g
B. 15 g
C. 26 g
D. 30 g
Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
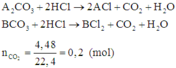
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)
Hòa tan hoàn toàn hỗn hợp 2 muối cacbonat của 2 kim loại hóa trị II trong dung dịch HCl dư thu được 10,08 lít khí không màu ở điều kiện tiêu chuẩn. Cô cạn dung dịch sau phản ứng thì khối lượng muối khan thu được so với trước phản ứng là
A. tăng 4,95 gam.
B. giảm 4,95 gam.
C. tăng 5,85 gam.
D. giảm 5,85 gam.
Hòa tan hoàn toàn hỗn hợp 2 muối cacbonat của 2 kim loại hóa trị II trong dung dịch HCl dư thu được 10,08 lít khí không màu ở điều kiện tiêu chuẩn. Cô cạn dung dịch sau phản ứng thì khối lượng muối khan thu được so với trước phản ứng là:
A. tăng 4,95 gam
B. giảm 4,95 gam
C. tăng 5,85 gam
D. giảm 5,85 gam
Đáp án A
Đặt công thức của hai muối là RCO3
Ta có: nCO2= 10,08/22,4= 0,45 mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
Theo PT ta có: nRCO3= nRCl2= nCO2= 0,45 mol
→mRCl2- mRCO3= 0,45. (R+71)- 0,45. (R+60)= 4,95 gam
→Muối sau phản ứng tăng so với trước phản ứng là 4,95 gam
Khi hoà tan hoàn toàn 3 gam hỗn hợp hai kim loại nhóm IA trong dung dịch HCl dư thu được 0,672 lít khí H 2 (đktc). Cô cạn dung dịch sau phản ứng thu được a gam muối khan, giá trị của a là
A. 4,90 gam
B. 5,71 gam
C. 5,15 gam
D. 5,13 gam
Cho hỗn hợp X gồm 2 kim loại thuộc nhóm IIA, ở hai chu kì liên tiếp nhau. Cho 8,4 gam X tan hòan toàn trong dung dịch HCl dư thu được 5,6 lít khí H2( đktc). Cô cạn dung dịch sau phản ứng thu được khối lượng muối khan là:
A. 26,15 gam
B. 17,275 gam
C. 8,9 gam
D. 43,9 gam
Đáp án: A
Ta có: nHCl= 2nH2 = 0,5 mol
m muối = m kim loại + mCl-
= 8,4 + 0,5. 35,5 = 26,15 gam
Hòa tan hoàn toàn 14,15 gam hỗn hợp X gồm Al và Cu trong dung dịch HCl dư thu được dung dịch Y, chất rắn Z và thoát ra V lít khí H2 (đktc). Cô cạn dung dịch Y thu được 6,675 gam muối khan.
a. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính V c. Nếu đốt cháy hoàn toàn lượng X trên trong khí O2 thì thể tích O2 đem đốt cháy là bao nhiêu.
a) \(n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,05<-----------0,05---->0,075
=> \(\%Al=\dfrac{0,05.27}{14,15}.100\%=9,54\%\)
=> \(\%Cu=\dfrac{14,15-0,05.27}{14,15}.100\%=90,46\%\)
b) \(V_{H_2}=0,075.22,4=1,68\left(l\right)\)
c) \(n_{Cu}=\dfrac{14,15-0,05.27}{64}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
2Cu + O2 --to--> 2CuO
0,2-->0,1
=> \(V_{O_2}=\left(0,1+0,0375\right).22,4=3,08\left(l\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ m_{AlCl_3}=6,675\left(mol\right)\\ n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\\ \Rightarrow n_{Al}=n_{AlCl_3}=0,05\left(mol\right)\\ \Rightarrow m_A=0,05.27=1,35\left(g\right);m_{Cu}=14,15-1,35=12,8\left(g\right)\\ \%m_{Cu}=\dfrac{12,8}{14,15}.100\approx90,459\%\\ \Rightarrow\%m_{Al}\approx9,541\%\\ b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,075.22,4=1,68\left(l\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{O_2}=\dfrac{3}{4}.n_{Al}+\dfrac{1}{2}.n_{Cu}=\dfrac{3}{4}.0,05+\dfrac{1}{2}.0,2=0,0875\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,0875.22,4=1,96\left(l\right)\)