A gồm: 0,01 mol Na+, 0,02 mol Ca2+; 0,02 mol và a mol ion X. Ion X và a là:
B. C l - và 0,01 mol
C. C O 3 2 - và 0,03 mol
D. O H - và 0,03 mol
Một dung dịch gồm: Na+ (0,01 mol); Ca2+ (0,02 mol); HCO3- (0,02 mol) và ion X (a mol). Ion X và giá trị của a là:
A. CO32- và 0,03.
B. Cl- và 0,01.
C. NO3- và 0,03.
D. OH- và 0,03.
Một dung dịch X gồm 0,01 mol Na+; 0,02 mol Ca2+; 0,02 mol HCO3– và a mol Y (bỏ qua sự điện li của nước). Ion Y và giá trị của a là
A. OH– và 0,03.
B. Cl– và 0,01.
C. CO32– và 0,03.
D. NO3– và 0,03
Đáp án D
Bảo toàn điện tích: ax = 0,01 + 0,02 x 2 - 0,02 = 0,03
Chỉ có D thõa mãn; vì OH- không tồn tại chung dung dịch với HCO3-
Một dung dịch gồm: 0,01 mol Na+; 0,02 mol Ca2+; 0,02 mol HCO3- và a mol ion X (bỏ qua sự điện li của nước). Ion X và giá trị của a là
A. NO3- và 0,03
B. Cl- và 0,01
C. CO32- và 0,03
D. OH- và 0,03
Đáp án A
TH1: Ion X có điện tích= -1 ⇒ nX = 0,01 + 0,02×2 – 0,02 = 0,03
⇒ chọn A hoặc D
Loại D vì OH- và HCO3- không cùng tồn tại trong cùng 1 dung dịch
Đáp án A.
TH2: Ion X có điện tích = -2 ⇒ nX = (0,01 + 0,02×2 – 0,02): 2 = 0,015 ( Không thỏa mãn đáp án)
Một dung dịch X gồm 0,01 mol Na+; 0,02 mol Ca2+; 0,02 mol HCO3– và a mol Y (bỏ qua sự điện li của nước). Ion Y và giá trị của a là
A. OH– và 0,03
B. Cl– và 0,01
C. CO32– và 0,03
D. NO3– và 0,03
Một dung dịch X gồm 0,02 mol Na+; 0,01 mol Ca2+; 0,02 mol HCO3-và a mol ion X (bỏ qua sự điện li của nước). Ion X và giá trị của a là
A. OH- và 0,02
B. Cl- và 0,02
C. NO3- và 0,01
D. CO3- và 0,01
Tổng ion dương là 0,04 mol và tổng ion âm là 0,02 + a => a = 0,02
=> Đáp án B
Một dung dịch X gồm 0,01 mol Na+; 0,02 mol Ca2+; 0,02 mol HCO3- và a mol ion Y (bỏ qua sự điện li của nước). Ion Y và giá trị của a là:
A. NO3- và 0,03
B. Cl- và 0,01
C. CO32- và 0,03
D. OH- và 0,03
Đáp án A
Để dung dịch X tồn tại thì Y là NO3- hoặc Cl-
Ta thấy có đáp án A thỏa mãn định luật bảo toàn điện tích:
0,01.1 + 0,02.2 = 0,02.1 + 0,03.1
Trong một cốc nước có chứa 0,01 mol Na+ , 0,02 mol Ca2+, 0,01 mol Mg2+, 0,05 mol HCO3-, 0,02 mol Cl-, nước trong cốc là:
A. Nước mềm.
B. Nước cứng toàn phần.
C. Nước cứng vĩnh cửu.
D. Nước cứng tạm thời.
Giải thích:
Ta thấy cốc nước có chứa các ion Ca2+, Mg2+, HCO3-, Cl- => đây thuộc nước cứng toàn phần
Đáp án B
Trong 1 cốc nước chứa 0,01 mol Na+ ; 0,02 mol Ca2+ ; 0,01 mol Mg2+ ; 0,05 mol HCO3- ; 0,02 mol Cl-. Các chất có thể dùng làm mềm nước trong cốc là
A. HCl, Na2CO3, Na2SO4
B. Na2CO3, Na3PO4
C. Ca(OH)2, HCl, Na2SO4
D. Ca(OH)2, Na2CO3
Đáp án B
![]() có thể làm mềm nước cứng do tạo tủa trực tiếp
có thể làm mềm nước cứng do tạo tủa trực tiếp
Với ![]()
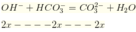
Để làm mềm nước thì kết tủa hoàn toàn ![]()
![]()
![]()
![]()
nên không thể làm mềm nước bằng C a ( O H ) 2
Trong một cốc nước chứa 0,01 mol Na+ ; 0,02 mol Ca2+ ; 0,01 mol Mg2+ ; 0,05 mol HCO3- ; 0,02 mol Cl-. Đun sôi nước trong cốc một thời gian lâu thu được nước thuộc loại nào:
A. Nước cứng vĩnh cửu
B. Nước cứng tạm thời
C. Nước mềm
D. Nước cứng toàn phần
Đáp án A
- Khi đun sôi: 2HCO3 → CO32- + CO2 + H2O
Mol 0,05 → 0,025
- Ta thấy tổng số mol (Ca2+, Mg2+) > số mol CO32-
=> Trong dung dịch sau khi đun có Ca2+, Mg2+ và Cl-
=> Đây là loại nước cứng vĩnh cửu