Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 300ml dung dịch gồm có NaOH 1M và Ba(OH)2 0,5M thu được 27,58 gam kết tủa. Giá trị của V là
A. 3,136.
B. 10,304 hoặc 1,568.
C. 10,304
D. 3,136 hoặc 10,304.
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 200ml dung dịch gồm có NaOH 1M và Ba(OH)2 0,5M thu được 15,76 gam kết tủa. Giá trị của V là
A. 0,896.
B. 1,792 hoặc 7,168.
C. 1,792.
D. 0,896 hoặc 3,584.
Dung dịch X gồm NaOH xM và Ca(OH)2 yM. Dung dịch Y gồm NaOH yM và Ca(OH)2 xM.
– Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch X thu được 4 gam kết tủa
– Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch Y thu được 7 gam kết tủa
Giá trị x : y gần nhất với
A. 1,0
B. 2,0
C. 2,5
D. 1,5
Đáp án D
Ta có:
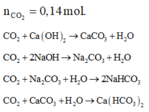
Nếu n C O 2 < 0,2x + 0,2y thì lượng kết tủa mỗi trường hợp tạo ra đúng bằng số mol Ca(OH)2.
thì lượng kết tủa mỗi trường hợp tạo ra đúng bằng số mol Ca(OH)2.
Do đó: 0,2x = 0,07; 0,2y = 0,04 => 0,2x + 0,2y = 0,11 < 0,14 (vô lý)
Do vậy cả 2 trường hợp đều có sự hòa tan kết tủa. Ta có:
TN1: Lượng kết tủa tạo ra là 0,2y - (0,14 - 0,2x - 0,2y) = 0,04
TN2: Lượng kết tủa tạo ra là 0,2x - (0,14 - 0,2x - 0,2y) = 0,07
Giải hệ: x = 0,4; y = 0,25 => x:y = 1,6
Dung dịch X gồm NaOH xM và Ca(OH)2 yM. Dung dịch Y gồm NaOH yM và Ca(OH)2 xM.
➢ Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch X thu được 4 gam kết tủa
➢ Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch Y thu được 7 gam kết tủa
Giá trị x : y gần nhất với
A. 1,5
B. 1,0
C. 2,0
D. 2,5
Dung dịch X gồm NaOH xM và Ca(OH)2 yM. Dung dịch Y gồm NaOH yM và Ca(OH)2 xM.
– Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch X thu được 4 gam kết tủa
– Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch Y thu được 7 gam kết tủa
Giá trị x : y gần nhất với
A. 1,0
B. 2,0
C. 2,5
D. 1,5
Đáp án D
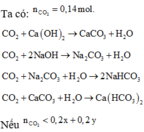
thì lượng kết tủa mỗi trường hợp tạo ra đúng bằng số mol Ca(OH)2.
Do đó: 0,2x = 0,07; 0,2y = 0,04 → 0,2x +0,2y = 0,11 < 0,14 (Vô lý).
Do vậy cả 2 trường hợp đều có sự hòa tan kết tủa. Ta có:
TN1: Lượng kết tủa tạo ra là 0,2y - (0,14 - 0,2x - 0,2y) = 0,04.
TN2: Lượng kết tủa tạo ra là 0,2x - (0,14 - 0,2x - 0,2y) = 0,07.
Giải hệ: x = 0,4; y = 0,25 → x:y = 1:6
Cho V lít khí CO2 (ở đktc) hấp thụ hoàn toàn vào 200 ml dung dịch hỗn hợp KOH 1M và Ba(OH)2 0,75M thu được 27,58 gam kết tủa. Giá trị lớn nhất của V là
A. 6,272 lít.
B. 8,064 lít.
C. 8,512 lít.
D. 2,688 lít.
Cho V lít khí CO2 (ở đktc) hấp thụ hoàn toàn vào 200 ml dung dịch hỗn hợp KOH 1M và Ba(OH)2 0,75M thu được 27,58 gam kết tủa. Giá trị lớn nhất của V là
A. 6,272 lít.
B. 8,064 lít.
C. 8,512 lít.
D. 2,688 lít.
Hỗn hợp X gồm Ba, BaO, Na, Na2O và K. Cho m gam hỗn hợp X vào nước dư thu được 3,136 lít H2 (đktc), dung dịch Y chứa 7,2 gam NaOH; 0,93m gam Ba(OH)2 và 0,044m gam KOH. Hấp thụ hoàn toàn 7,7952 lít CO2 (đktc) vào dung dịch Y thu được a gam kết tủa. Giá trị gần nhất của a là:
A. 25,5
B. 27,5
C. 24,5
D. 26,5
Đáp án A
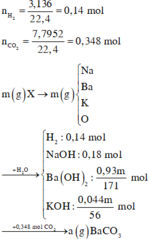
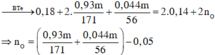
m = 23 . 0 , 18 + 137 . 0 , 93 m 171 + 39 . 0 , 44 m 56 + 16 n o
=> m - 23 . 0 , 18 + 137 . 0 , 93 m 171 + 39 . 0 , 044 56 + 16 0 , 93 m 171 + 0 , 044 56 - 0 , 05
=> m = 25,5 g

Giá trị a gần nhất với giá trị 25,5
Hỗn hợp X gồm Ba, BaO, Na, Na2O và K. Cho m gam hỗn hợp X vào nước dư thu được 3,136 lít H2 (đktc), dung dịch Y chứa 7,2 gam NaOH, 0,93m gam Ba(OH)2 và 0,044m gam KOH. Hấp thụ hoàn toàn 7,7952 lít CO2 (đktc) vào dung dịch Y thu được a gam kết tủa. Giá trị của a gần nhất với
A. 27,5
B. 24,5
C. 25,5
D. 26,5.
Đáp án : C
Nếu ta đốt cháy X tạo hỗn hợp T toàn oxit thì lượng mol nguyên tố kim loiaj không đổi
=> nH2 = nO pứ = 0,14 mol => moxit = mX + mO pứ = m + 2,24 (g)
Y : nNaOH = 0,18 => nNa2O = 0,09 mol
,nBa(OH)2 = nBaO = 31m/5700 ; nK2O = ½ nKOH = 5,5m/14000
=> mT = mBaO + mNa2O + mK2O
=> m = 25,5g
=> nOH = 0,4774 mol
,nCO2 = 0,348 mol
=> nCO3 = nOH – nCO2 = 0,1294 mol < nBa = 0,1387 mol
=> nBaCO3 = 0,1294
=>a = 25,49g
Hấp thụ hoàn toàn V lít CO2 (đktc) vào dung dịch chứa a mol Ba(OH)2 thì thu được 19,7 gam kết tủa. Hấp thụ hoàn toàn V lít CO2 (đktc) vào dung dịch chứa a mol Ba(OH)2 và a mol NaOH thì thu được 39,4 gam kết tủa. Giá trị của V và a tương ứng là
A. 5,60 và 0,2
B. 6,72 và 0,1
C. 8,96 và 0,3
D. 6,72 và 0,2
Chọn D
nCO2 dùng ở 2 thí nghiệm là như nhau nhưng TN2 cho nhiều BaCO3 hơn TN1
Þ Trong dung dịch sau phản ứng của TN1 còn Ba2+ cùng với CO32− hoặc HCO3-
Þ Dung dịch sau phản ứng của TN1 chỉ có Ba(HCO3)2.
Vậy ở TN1 bản chất là giống thí nghiệm 1 tạo ra 0,1 mol BaCO3 và dung dịch có a – 0,1 mol Ba(HCO3)2
Lượng NaOH thêm vào là a > nBa(HCO3)2 Þ Toàn bộ Ba2+ đã kết tủa
Þ a – 0,1 = 0,1 Þ a = 0,2; BTNT.C Þ nCO2 = 0,1 + 0,1.2 = 0,3 Þ V = 6,72.