Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). M là
A. Mg
B. Ca
C. Fe
D. Al
Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Mg
B. Ca
C. Fe
D. Al
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít khí H2 đktc. Kim loại M là kim loại nào sau đây?
A. Fe.
B. Al.
C. Ca.
D. Mg.
Đáp án B.
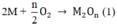
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
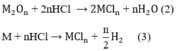
Số mol H2: 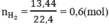
Theo phương trình (1)
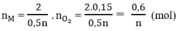
Theo phương trình (3)
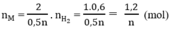
Tổng số mol M là 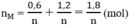
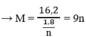
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al
Cho 16,2 gam kim loại M có hoá trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hoà tan vào dung dịch HCI dư thấy thoát ra 13,44 lít H2 ở đktc. Kim loại M là
A. Fe. B. AI. c. Ca. D. Mg.
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
Số mol H2:
Theo phương trình (1)
Theo phương trình (3)
Tổng số mol M là
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al
Cho 16,2 gam kim loại M có hoá trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hoà tan vào dung dịch HCI dư thấy thoát ra 13,44 lít H2 ở đktc. Kim loại M là
A. Fe. B. Al c. Ca. D. Mg.
1. Cho 8,64 gam kim loại R (có hoá trị n không đổi) tác dụng với O2, sau khi phản ứng hoàn toàn thu được 13,44 gam chất rắn. Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 1,344 lít H2 (đktc). Xác định kim loại R.2. Cho m gam Al tác dụng với 0.05 mol O2 thu được chất rắn X. Hòa tan hết X trong dung dịch HCl dư thu được 0.03 mol H2. Tính giá trị của m.
\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
.0,12/n...............0,12/n......0,06......
\(R_2O_n+2nHCl\rightarrow2RCl_n+nH_2O\)
.0,3/n......................................0,3....
\(n_{H_2O}=2n_{O_2}=0,3\left(mol\right)\)
Có : \(m=13,44=m_R+m_{R_2O_n}=\dfrac{0,12R}{n}+\dfrac{\left(2R+16n\right)0,3}{n}\)
\(\Rightarrow R=12n\)
=> R là Mg
\(n_{Al\left(I\right)}=\dfrac{3}{2}n_{H_2}=0,045\left(mol\right)\)
\(n_{Al\left(II\right)}=2n_{Al_2O_3}=\dfrac{2}{3}n_{H_2O}=\dfrac{2}{3}.2n_{O_2}=\dfrac{4}{3}n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
\(\Rightarrow m_{Al}=m=3,015\left(g\right)\)
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Fe
B. Al
C. Ca
D. Mg
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Fe
B. Al
C. Ca
D. Mg
Câu 9: Cho 16,2 gam kim loại M, hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCl dư thấy bay ra 13,44 lít H2 ở đktc. Kim loại M là?
\(n_{H_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
\(n_{M\left(pu\right)}=a\left(mol\right)\)
Bảo toàn e :
\(na=0.15\cdot4+0.6\cdot2=1.8\)
\(a=\dfrac{1.8}{n}\)
\(M=\dfrac{16.2}{\dfrac{1.8}{n}}=9n\)
\(n=3\Rightarrow M=27.M:Al\)
Bảo toàn e toàn bộ quá trình ta có: $n_{M}=\frac{1,8}{n}(mol)$
$\Rightarrow M_{M}=9n$
Lập bảng biện luận suy ra M là Al
Cho 16,2 gam kim loại M (hóa trị không đổi) tác dụng với 0,15 mol oxi. Chất rắn sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCL dư, thu được 13,44 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Kim loại M là
A. Ca
B. Zn
C. Al
D. Mg
Đáp án C
Các phương trình phản ứng :
M tác dụng với O2: 4 M + 2 n O 2 → t 0 2 M n O n
Chất rắn sau phản ứng tác dụng với dung dịch HCl thu được khí H2, chứng tỏ chất rắn sau có M dư nên O2 hết - chất rắn sau gồm M dư và M2On :
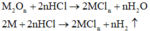
Tính toán:
Số mol H2 thu được là: n H 2 = 13 , 44 22 , 4 = 0 , 6 m o l
Sơ đồ phản ứng:
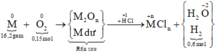
Các quá trình nhường, nhận electron cho cả quá trình:
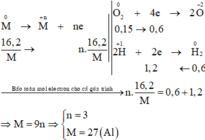
Cho 16,2 gam kim loại M có hoá trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hoà tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 ở đktc. Kimloại M là
A. Fe. B. Al. C. Ca. D. Mg.
Chọn B
4M + nO2 → 2M2On
0,15 (mol)
M2On + 2nHCl → 2MCln + nH2O
M + nHCl → MCln + H2
= 0,6 (mol)
Ta có: nM =
(mol)
=> M = 16,2 : = 9n; Biện luận:
n = 1 => M = 9 (loại).
n = 2 => M = 18 (loại).
n = 3 => M = 27 (Al)
A là hỗn hợp gồm: Ba, Al, Mg. Lấy m gam A cho tác dụng với nước tới khi hết phản ứng thấy thoát ra 3,36 lit H 2 (đktc). Lấy m gam A cho vào dung dịch xút dư tới khi hết phản ứng thấy thoát ra 6,72 lít H 2 (đktc). Lấy m gam A hoà tan bằng một lượng vừa đủ dung dịch axit HCl thì thu được một dung dịch và 8,96 lit H 2 (đktc). Hãy tính m gam.
A. 12,56 g
B. 12,26 g
C. 25,46 g
D. 25,64 g
Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
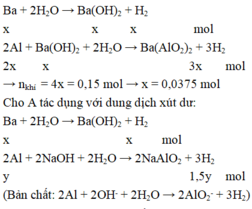

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B