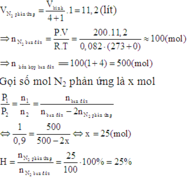Một bình kín chứa 3,584 lít một ankan (ở 0oC và 1,25atm). Đun nóng để xảy ra phản ứng cracking, rồi đưa nhiệt độ bình về 136,5oC thì áp suất đo được là 3atm. Hiệu suất của phản ứng crackinh là :
A. 20%.
B. 60%.
C. 40%.
D. 80%.
Trong một bình kín chứa 10 lít nitơ và 10 lít hiđro ở nhiệt độ 0oC và 10 atm. Sau phản ứng tổng hợp N H 3 , lại đưa bình về 0oC. Biết rằng có 60% hiđro tham gia phản ứng, áp suất trong bình sau phản ứng là
A. 10 atm.
B. 8 atm.
C. 9 atm.
D. 8,5 atm.
Cho vào một bình kín dung tích không đổi a mol Cl2 và 1 mol H2 thì áp suất của bình là 2,5 atm. Nung nóng bình cho phản ứng xảy ra với hiệu suất đạt 80%. Đưa bình về nhiệt độ ban đầu thì áp suất của bình là
A. 1,35 atm
B. 1,75 atm
C. 2 atm
D. 2,5 atm
Cho vào một bình kín dung tích không đổi a mol Cl2 và 1 mol H2 thì áp suất của bình là 2,5 atm. Nung nóng bình cho phản ứng xảy ra với hiệu suất đạt 80%. Đưa bình về nhiệt độ ban đầu thì áp suất của bình là:
A. 1,35 atm.
B. 1,75 atm.
C. 2 atm.
D. 2,5 atm.
Chọn đáp án D.
+ Áp suất tỷ lệ với số mol p 1 p 2 = n 1 n 2
+ Ta dễ thấy dù phản ứng xảy ra với hiệu suất bao nhiêu thì số mol khí cũng không đổi → p = c o n s t = 2 , 5 a t m
Một bình kín dung tích không đổi chứa hỗn hợp cùng thể tích khí N2 và H2 ở 0oC, 100atm. Sau khi tiến hành tổng hợp NH3, đưa nhiệt độ bình về 0oC, áp suất mới của bình là 90atm. Hiệu suất phản ứng tổng hợp NH3 là:
A. 10%
B. 25%
C. 20%
D. 30%
Đáp án D
Đặt nH2= nN2= a mol (ban đầu)
→ Tổng số mol khí ban đầu n1= a+a=2a (mol)
Do  nên hiệu suất tính theo H2
nên hiệu suất tính theo H2
Đặt nH2 pứ= x mol
N2 + 3H2 ⇌ 2NH3
Ban đầu a a mol
Phản ứng x/3 x 2x/3 mol
Sau pứ (a-x/3) (a-x) 2x/3 mol
Tổng số mol khí sau phản ứng n2= (a-x/3) + (a-x) + 2x/3= 2a- 2x/3 (mol)
Trong cùng điều kiện về nhiệt độ, tỉ lệ số mol bằng tỉ lệ áp suất

Cho 5 lít N2 và 15 lít H2 vào một bình kín dung tích không đổi . Ở 00C, áp suất trong bình là P1 atm. Đun nóng bình một thời gian thấy có 20% N2 tham gia phản ứng, đưa bình về nhiệt độ ban đầu thấy áp suất trong bình lúc này là P2 atm. Tỉ lệ P1 và P2 là:
A. 6 : 10
B. 10 : 6
C. 10 : 9
D. 9 : 10
Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì có  nên hiệu suất phản ứng tính theo N2 hoặc H2
nên hiệu suất phản ứng tính theo N2 hoặc H2
Giả sử ban đầu có 1 mol N2 và 3 mol H2, nkhí ban đầu= 4 mol
→nN2 pứ= 1.20%= 0,2 mol
N2+ 3H2 ⇌ 2NH3
Ban đầu 1 3 mol
Phản ứng 0,2 0,6 0,4 mol
Sau pứ 0,8 2,4 0,4 mol
nkhí sau pứ= 0,8 + 2,4 + 0,4= 3,6 mol
Trong cùng điều kiện nhiệt độ và thể tích thì tỉ lệ về số mol chính là tỉ lệ về áp suất

Một bình kín chứa hỗn hợp H 2 , C l 2 với áp suất ban đầu là P. Đưa bình ra ánh sáng để phản ứng xảy ra, sau đó đưa về nhiệt độ ban đầu thì áp suất bình lúc đó là P 1 . Mối quan hệ giữa P 1 và P là
A. P 1 = 2 P
B. P 1 > P
C. P = P 1
D. P 1 < P
Trong một bình kín dung tích không đổi ở đktc chứa etilen và H2, có bột Ni xúc tác. Đun nóng bình một thời gian sau đó đưa bình về nhiệt độ ban đầu (0oC), áp suất bình là p (atm). Cho biết tỉ khối hơi của hỗn hợp đầu và hỗn hợp sau phản ứng so với hiđro lần lượt là 7,5 và 9. Tính % thể tích của C2H6 có trong hỗn hợp sau phản ứng ?
A. 20%
B. 40%
C. 60%
D. 80%
Đáp án A
Đặt nC2H4 ban đầu = x mol; nH2 = y mol.
Ta có MY = 18 → H2 dư; hhY gồm C2H6 và H2 dư.
Theo BTKL: mX = mY = 28x + 2y gam.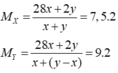
→ y = 5x → hhY gồm x mol C2H6 và 4x mol H2.
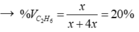
TD 5: cho 4 lít N2 và 14 lít H2 vào bình kín rồi nung nóng với xúc tác thích hợp để phản ứng xảy ra , sau phản ứng thu được 16,4 lít hỗn hợp khí ( các khí đo ở cùng đều kiện về nhiệt độ và áp suất)
a. Tính thể tích khí amoniac thu được
b. Xác định hiệu suất của phản ứng.
a) PTHH: N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Đặt thể tích N2 phản ứng là x (lít)
=> VH2 pứ= 3x (lít) , VNH3 sinh ra=2x (lít)
VN2 dư= 4-x (lít), VH2 dư= 14-3x (lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được sau phản ứng là:
V khí= VH2 dư+ VN2 dư+ VNH3= 14-3x + 4-x+ 2x= 16,4
=> x=0,8 lít
=>VNH3 sinh ra= 2x = 2.0,8 =1,6 (lít)
b)Do \(\dfrac{4}{1}< \dfrac{14}{3}\) =>Hiệu suất tính theo N2
=>H=\(\dfrac{V_{N_2\left(pứ\right)}}{V_{N_2\left(bđ\right)}}\)⋅100=\(\dfrac{0,8}{4}.100\)=20%
Trong một bình kín dung tích 56 lít (không đổi) chứa N2 và H2 theo tỷ lệ thể tích là 1:4. Ở 00C, áp suất 200 atm (xt Fe3O4). Nung nóng bình một thời gian sau đó đưa bình về nhiệt độ 00C thấy áp suất trong bình giảm 10% so với áp suất ban đầu.
Tính hiệu suất của phản ứng điều chế NH3?
A. 25%
B. 20%
C. 75%
D. 45%
Đáp án A
N2 và H2 theo tỷ lệ thể tích là 1 : 4 tính hiệu suất theo N2