Hòa tan hết 2,24 g Fe trong 120ml dung dịch HCl 1M bị loăng được dung dịch X. Cho AgNO3 dư vào X tạo m g kết tủa. Giá trị của m là
A. 19,40
B. 17,22
C. 21,54
D. 18,30
Đốt cháy m gam hỗn hợp Mg , Fe trong oxi một thời gian thu được (m + 4,16)g hỗn hợp X chứa các oxit. Hòa tan hoàn toàn hỗn hợp X bằng dung dịch HCl vừa đủ thu được dung dịch Y chứa (3m + 1,82)g muối. Cho AgNO3 dư vào dung dịch Y thấy tạo (9m + 4,06)g kết tủa. Mặt khác hòa tan hết 3,75m g hỗn hợp X bằng dung dịch HNO3 loãng dư thu được dung dịch Z chứa m’ gam muối. Giá trị của m là :
A. 107,6
B. 161,4
C. 158,92
D. 173,4
Chọn A
Bảo toàn khối lượng : mKL + mO = moxit => nO = 0,26 mol
Khi oxit phản ứng với HCl thì cũng tương tự như 1 mol O bị thay thế bởi 2 mol Cl-
=> nCl = 2nO = 0,52 mol
=> mKL + mCl = mmuối => m + 0,52.35,5 = 3m + 1,82
=> m = 8,32g
, mkết tủa = 9m + 4,06 = 78,94g
,nAgCl = nCl = 0,52 mol => Giả sử có Ag => nAg = 0,04 mol
Fe2+ + Ag+ -> Fe3+ + Ag
=> nFe2+ = nAg = 0,04 mol => nFeO(X) = 0,04
Vậy trong 3,75m (g) hỗn hợp X ( 31,2g) sẽ có nFeO = 0,04.31,2/(8,32 + 4,16) = 0,1
Khi phản ứng với HNO3 thì FeO -> Fe(NO3)3 ( Fe2+ -1e -> Fe3+)
Xét 3,75m gam X : Ta thấy nCl(muối) = ne trao đổi (1) = 1,3 mol
Khi phản ứng với HNO3 thì ne trao đổi (2) = ne trao đổi (1) + nFeO = nNO3 muối = 1,4 mol
=> m’ = mKL + mNO3 = 8,32.2,5 + 1,4.62 = 107,6g
( Nếu xét trường hợp không tạo NH4NO3)
Hòa tan hết 5,6 gam Fe trong 400 ml dung dịch HCl 1M thu được dung dịch X. Cho dung dịch X tác dụng với dung dịch AgNO3 dư, sau khi kết thúc phản ứng thu được khí NO duy nhất, đung dịch Y và m gam kết tủa. Giá trị của m là
A. 73,6 gam
B. 59,25 gam
C. 57,4 gam
D. 65,5 gam
Đáp án C
nFe = 5,6: 56 = 0,1 mol ; nHCl = 0,4.1 = 0,4 mol
Fe + 2HCl → FeCl2 + H2
Mol 0,1 → 0,2 → 0,1
=> nHCl dư = 0,4 – 0,2 = 0,2 mol
- Khi cho AgNO3 dư vào thì có phản ứng:
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
Mol:0,1 → 0,4/3 (< 0,2)
=> H+ dư, không còn Fe2+.
Ag+ + Cl- → AgCl
Bảo toàn nguyên tố Clo: nCl = nHCl ban đầu = 0,4 mol
=> nAgCl = 0,4 mol => m = 0,4.143,5 = 57,4g
Hòa tan hết 2,24 gam bột Fe vào 120 ml dung dịch HCl 1M, thu được dung dịch X. Cho X tác dụng với lượng dư dung dịch AgNO3, sau khi kết thúc các phản ứng thu được V lít khí NO ( sản phẩm khử duy nhất ở đktc) và m gam chất rắn. Giá trị của m và V lần lượt là
A. 18,30 và 0,672
B. 17,72 và 0,448
C. 18,30 và 0,224
D. 17,22 và 0,22
Hòa tan hết 2,24 gam bột Fe vào 120 ml dung dịch HCl 1M, thu được dung dịch X. Cho X tác dụng với lượng dư dung dịch AgNO3, sau khi kết thúc các phản ứng thu được V lít khí NO ( sản phẩm khử duy nhất ở đktc) và m gam chất rắn. Giá trị của m và V lần lượt là
A. 18,30 và 0,672
B. 17,72 và 0,448
C. 18,30 và 0,224
D. 17,22 và 0,22
Hòa tan hết 2,24 gam bột Fe vào 120 ml dung dịch HCl 1M, thu được dung dịch X. Cho X tác dụng với lượng dư dung dịch AgNO3, sau khi kết thúc các phản ứng thu được V lít khí NO (sản phẩm khử duy nhất, đktc) và m gam chất rắn. Giá trị của m và V lần lượt là
A. 17,22 và 0,224
B. 1,08 và 0,224
C. 18,3 và 0,448
D. 18,3 và 0,224
Hòa tan 2,24 gam Fe bằng 300 ml dung dịch HCl 0,4 M , thu được dung dịch X và khí H 2 . Cho dung dịch A g N O 3 dư vào X, thu được khí NO (sản phẩm khử duy nhất của N + 5 ) và m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 18,3.
B. 8,61.
C. 7,36.
D. 9,15.
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y được m gam hỗn hợp muối khan. Giá trị m là
A. 6,36 g.
B. 63,6 g.
C. 9,12g.
D. 91,2g.
Áp dụng phương pháp tăng giảm khối lượng:
Cứ 1 mol MCl2 → 1 mol M(NO3)2 và 2 mol AgCl thì m tăng 2.62 - 2.35,5 = 53 gam
Phản ứng tạo 0,12 mol AgCl có khối lượng muối tăng 3,18 gam
mmuối nitrat = mmuối clorua + mtăng = 5,94 + 3,18 = 9,12 (gam)
Đáp án C
Hòa tan hoàn toàn m gam Na vào V ml dung dịch HCl 1M thu được 3,36 lít khí H2 và dung dịch X. Cho dung dịch AgNO3 dư vào dung dịch X thu được 40,3 gam kết tủa. Giá trị của V là:
A. 0,2
B. 200
C. 0,3
D. 300
n H 2 = 0,15
Như đã biết, khi cho kim loại Na hòa tan vào dung dịch HCl, sau khi axit hết mà kim loại còn dư thì kim loại sẽ tiếp tục tác dụng với nước:
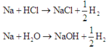
Quan sát hai phản ứng, ta có nNaCl + nNaOH = 0,3
Phản ứng tạo NaOH có thể xảy ra hoặc không nên ta gọi nNaCl = a; nNaOH = b (nếu không tạo ra NaOH thì b = 0).
Khi cho AgNO3 vào dung dịch X thì có các phản ứng tạo kết tủa:
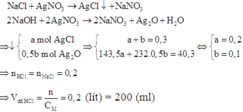
Đáp án B.
Cho a gam kim loại R tan hoàn toàn trong 200 ml dung dịch HCl 0,5M, thu được dung dịch X và 2,24 lít H2 (đktc). Cho dung dịch AgNO3 dư vào X, thu được m gam kết tủa. Giá trị của m là
A. 25,95.
B. 14,35.
C. 32,84.
D. 28,70.
Giải thích:
nHCl = 0,2.0,5 = 0,1 (mol); nH2 = 2,24 :22,4 = 0,1 (mol)
=> nHCl < 2nH2
=> R là kim loại kiềm hoặc kiềm thổ, phản ứng hết với HCl sau đó phản ứng được với H2O
2R + 2nHCl → RCln + nH2↑
0,1 → 0,05
2R + 2nH2O → 2R(OH)n + nH2↑
0,1/n ←0,05
RCln + nAgNO3 → nAgCl↓ + R(NO3)n
2R(OH)n + 2nAgNO3 → nAg2O↓ + R(NO3)n + nH2O
0,1/n → 0,05
=> m↓ = mAgCl + mAg2O = 0,1.143,5 + 0,05. 232 = 25,95(g)
Chú ý:
Tránh sai lầm khi chỉ tính khối lượng kết tủa là AgCl khi đó sẽ ra 14,35 g => chọn ngay đáp án B sẽ dẫn đến sai lầm
Đáp án A