Cho viên kẽm tác dụng với H N O 3 , sau phản ứng không thấy có khí sinh ra. Tổng hệ số cân bằng của phản ứng là
A. 26
B. 22
C. 24
D. 23
Cho viên Mg tác dụng với H N O 3 , sau phản ứng không thấy có khí sinh ra. Hệ số cân bằng của trong phản ứng là
A. 8
B. 9
C. 10
D. 12
Khi cho kim loại Mg tác dụng với HNO3, sau phản ứng không thấy xuất hiện khí. Tổng số hệ số của các chất (là các số nguyên tối giản) có trong phương trình khi cân bằng là:
A. 24
B. 22
C. 20
D. 29
Đáp án B
Khi cho kim loại Mg tác dụng với HNO3, sau phản ứng không thấy xuất hiện khí.
→ Sản phẩm khử là NH4NO3
PTHH:
4Mg+10 HNO3→ 4Mg(NO3)2+ NH4NO3+ 3H2O
→Tổng hệ số các chất là 22
Thực hiện phản ứng tổng hợp nitrobenzen theo sơ đồ:
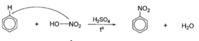
Cho các phát biểu sau:
(a) Vai trò của axit H2SO4 là hút nước sinh ra trong phản ứng, do đó ngăn cản được quá trình nitrobenzen tác dụng với nước.
(b) Nếu thay axit H2SO4 bằng axit HClO4 thì phản ứng nitro hóa vẫn xảy ra.
(c) Nitrobenzen sinh ra trong phản ứng là chất rắn, không màu.
(d) Nếu không có axit H2SO4, chỉ có axit HNO3 đậm đặc thì phản ứng nitro hóa không xảy ra.
Số phát biểu đúng là
A. 1
B. 1
C. 3
D. 4
Cho 26 gam kẽm tác dụng hết với dung dịch có chứa 29,2 gam axit clohiđric (HCl). Sau phản ứng thu được 54,4 gam kẽm clorua (ZnCl2) và khí hiđro. a) Lập phương trình hóa học của phản ứng? b) Cho biết các chất phản ứng và sản phẩm, tỉ lệ số nguyên tử, số phân tử giữa các chất và của hai cặp chất (tùy chọn) trong phản ứng này. c) Viết công thức về khối lượng của phản ứng. d) Tính khối lượng khí hiđro sinh ra? e) Biết nguyên tử cacbon có khối lượng tính bằng gam là 1,9926.10-23 gam. Tính khối lượng bằng gam của nguyên tử hiđro và kẽm? f) Cho lượng khí hiđro vừa thu được vào bình chứa 0,44g khí cacbonic (CO2). Tính số mol và thể tích hỗn hợp khí này ở điều kiện tiêu chuẩn.
a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) Chất phản ứng : $Zn,HCl$
Sản phẩm : $ZnCl_2,H_2$
Tỉ lệ số nguyên tử Zn : Số phân tử $HCl$ là 2 : 1
Tỉ lệ số phân tử $ZnCl_2$ : số phân tử $H_2$ là 1 : 1
c) $m_{Zn} + m_{HCl} = m_{ZnCl_2} + m_{H_2}$
d) $m_{H_2} = 26 + 29,2 - 54,4 = 0,8(gam)$
e) 1 đvC = $\dfrac{1,9926.10^{-23}}{12} = 1,6605.10^{-24}(gam)$
$m_H = 1.1,6605.10^{-24} = 1,6605.10^{-24}(gam)$
$m_{Zn} = 65.1,6605.10^{-24} = 107,9325.10^{-24}(gam)$
f)$n_{H_2} = 0,4(mol) ; n_{CO_2} = \dfrac{0,44}{44} = 0,01(mol)$
$\Rightarrow n_{hh} = 0,4 + 0,01 = 0,41(mol)$
$V_{hh} = 0,41.22,4 = 9,184(lít)$
Xét phản ứng: A + B → C + D. Khi cho 1 mol A tác dụng với 1 mol B thì hiệu suất cực đại của phản ứng đạt 66,67%. Hệ số cân bằng của phản ứng là:
A. 2.
B. 4.
C. 3.
D. 8.
Chọn B.
Với 1 mol A và 1 mol B, lúc cân bằng hiệu suất phản ứng đạt 66,67% nên: nA = nB = 0,3333 mol; nC = nD = 0,6667 mol.
Do đó: Kc = Kp = Kx = 4.
Cho kim loại kẽm(Zn) tác dụng với 200g axit clohidric sau phản ứng thấy thoát ra 4.48(l) khí H2 (dktc) a)tính khối lượng Zn phả ứng b) Tính nồng độ dung dịch HCl phản ứng c) Khử 24g CuO cho bằng lượng khí H2 nói trên. Chất nào dư. Khối lượng chất dư là bao nhiêu
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2.......0.4.......................0.2\)
\(m_{Zn}=0.2\cdot65=13\left(g\right)\)
\(C\%_{HCl}=\dfrac{0.4\cdot36.5}{200}\cdot100\%=7.3\%\)
\(n_{CuO}=\dfrac{24}{80}=0.3\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{t^0}}Cu+H_2O\)
\(1..........1\)
\(0.3.........0.2\)
\(LTL:\dfrac{0.3}{1}>\dfrac{0.2}{1}\Rightarrow CuOdư\)
\(m_{CuO\left(dư\right)}=\left(0.3-0.2\right)\cdot64=6.4\left(g\right)\)
Biểu diễn các phản ứng sau bằng phương trình chữ:
a) Đốt đây magie cháy trong oxi của không khí tạo thành magie oxit.
b) Cho viên kẽm vào ống nghiệm đựng dung dịch axit clohidric thấy sủi bọt khí hidro và sinh ra muối kẽm clorua.
c) Nhỏ dung dịch bari clorua vào axit sunfuric thấy có kết tủa trắng là muối bari sunfat và axit mới tạo thành là axit clohidric.
d) Đốt cháy xăng (chứa octan) tạo thành khí cacbonic và hơi nước.
e) Hidro cháy trong oxi tạo thành hơi nước.
f) Khi nấu cơm chứa tinh bột quá lửa tạo thành than (cacbon) và hơi nước.
g) Nhà máy nhiệt điện sử dụng nhiệt để làm quay tua bin sinh ra dòng điện.
Nguồn nhiệt này có được khi đốt cháy than đá chứa cacbon sinh ra khí cacbonic.
h) Tầng ozon ở phía cực nam bị thủng do phản ứng quang hóa. Phản ứng này xảy ra khi ozon bị phân hủy thành oxi.
i) Sắt bị gỉ là do để sắt ngoài không khí bị khí oxi phản ứng tạo thành gỉ chứa oxit sắt từ.
a) có chất mới được tào thành : magie ôxit
Magie + Khí oxi −→to→to Magie oxit
2Mg+O2−→to2MgO2Mg+O2→to2MgO
b) có 2 chất mới được tạo thành : kẽm clorua và khí hidro
Zn+2HCl→ZnCl2+H2↑Zn+2HCl→ZnCl2+H2↑
Kẽm + axit clohidric →→ Kẽm clorua + Khí hidro
d) chất mới được tạo thành là khí cabonic và hơi nước
PTHH: ..............................................
f) ôxit sắt từ được tạo thành
3Fe+2O2−→toFe3O43Fe+2O2→toFe3O4
Sắt + khí oxi −→to→to Sắt (II,III) oxit (hoặc ôxit sắt từ)
cho 1,3g kẽm tác dụng với HCl 7,3%. Phản ứng xong lấy lá kẽm ra khỏi dung dịch, rửa sạch làm khô thấy khối lượng lá kẽm giảm 0,65g so với trước phản ứng a) Tính thể tích khí H2 sinh ra ở điều kiện bình thường b) Tính khối lượng axit HCl đã tham gia phản ứng c) Tính nồng độ phần trăm của dung dịch sau phản ứng
\(n_{Zn\left(pứ\right)}=1,3-0,65=0,65g\)
\(n_{Zn}=\dfrac{0,65}{65}=0,01mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,01 0,02 0,01 0,01 ( mol )
\(V_{H_2}=0,01.24=0,24l\)
\(m_{HCl}=\dfrac{0,02.36,5}{7,3\%}=10g\)
\(m_{ZnCl_2}=0,01.136=1,36g\)
\(m_{ddspứ}=1,3+10-0,01.2=11,28g\)
\(C\%_{ZnCl_2}=\dfrac{1,36}{11,28}.100=12,05\%\)
Cho 16,25 gam Kẽm tác dụng với H2SO4, sau phản ứng thu được muối ZnSO4, khí hidro (đktc). a) Viết phương trình phản ứng hóa học b) Tính thể tích (đktc) khí hidro sinh ra. c) Tính khối lượng muối ZnSO4 tạo thành.
\(n_{Zn}=\dfrac{m}{M}=\dfrac{16,25}{65}=0,25\left(mol\right)\\ PTHH:Zn+H_2SO_4->ZnSO_4+H_2\)
tỉ lệ 1 : 1 : 1 : 1
n(mol) 0,25-->0,25------->0,25------>0,25
\(V_{H_2\left(dktc\right)}=n\cdot22,4=0,25\cdot22,4=5,6\left(l\right)\\ m_{ZnSO_4}=n\cdot M=0,25\cdot\left(65+32+16\cdot4\right)=40,25\left(g\right)\)