Điện phân một lượng dư dung dịch KCl với điện cực trơ, màng ngăn xốp thời gian 16,1 phút dòng điện I = 5A thu được 500 ml dung dịch X. pH của dung dịch X có giá trị là
A. 12,7
B. 1
C. 13
D. 1,3
Cho 24,94 gam hỗn hợp gồm CuSO4 và KCl vào nước dư, thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện I = 5A trong thời gian t giậy, thấy khối lượng dung dịch giảm 9,7 gam. Nếu thời gian điện phân là 1,5t giây, khối lượng catot tăng 6,4 gam; đồng thời thu được dung dịch Y. Dung dịch Y hòa tan tối đa m gam Al2O3. Giá trị của m và t lần lượt là
A. 1,36 gam và 4632 giây
B. 2,04 gam và 3088 giây
C. 1,36 gam và 3088 giây
D. 2,04 gam và 4632 giây
Điện phân 500 ml dung dịch hỗn hợp CuSO4 a mol/l và NaCl 1 mol/l với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi 5A trong thời gian 96,5 phút (hiệu suất quá trình điện phân là 100%, nước bay hơi không đáng kể) thu được dung dịch có khối lượng giảm so với ban đầu là 17,15 gam. Giá trị của a là
A. 0,3.
B. 0,4.
C. 0,2.
D. 0,5.
Điện phân 500 ml dung dịch hỗn hợp CuSO4 a mol/l và NaCl 1 mol/l với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi 5A trong thời gian 96,5 phút (hiệu suất quá trình điện phân là 100%, nước bay hơi không đáng kể) thu được dung dịch có khối lượng giảm so với ban đầu là 17,15 gam. Giá trị của a là
A. 0,3.
B. 0,4.
C. 0,2.
D. 0,5.
Điện phân 500 ml dung dịch hỗn hợp CuSO4 a mol/l và NaCl 1 mol/l với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi 5A trong thời gian 96,5 phút (hiệu suất quá trình điện phân là 100%, nước bay hơi không đáng kể) thu được dung dịch có khối lượng giảm so với ban đầu là 17,15 gam. Giá trị của a là
A. 0,2
B. 0,5
C. 0,3
D. 0,4
Dd có 0,5a mol CuSO4 và 0,5 mol NaCl.
Trong quá trình điện phân giả sử xảy ra :
+ Catot: Cu2+ → + 2e Cu
2H2O + 2e → 2OH- + H2
+ Anot: 2Cl- → Cl2 + 2e
ne trao đổi = 0,3 mol
=> nCl2= 0,15 mol ; nCu= 0,5a mol ; nH2= (0,3-a) mol
m giảm = m Cl2 + mCu + mH2
=> 17,15 = 71.0,15 + 64.0,5a + 2(0,3-a) => a=0,2 M
=>A
Cho 24,94 gam hỗn hợp gồm CuSO4 và KCl vào nước dư, thu được dung dịch X. Điện phân X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện I = 5A trong thời gian t giậy, thấy khối lượng dung dịch giảm 9,7 gam. Nếu thời gian điện phân là 1,5t giây, khối lượng catot tăng 6,4 gam; đồng thời thu được dung dịch Y. Y hòa tan tối đa m gam Al2O3. Giá trị của m và t lần lượt là
A. 2,04 gam và 4632 giây
B. 1,36 gam và 3088 giây
C. 2,04 gam và 3088 giây
D. 1,36 gam và 4632 giây
Điện phân 500 ml dung dịch hỗn hợp CuSO4 a mol/l và NaCl 1,0 mol/l với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi 5A trong thời gian 96,5 phút (hiệu suất quá trình điện phân là 100%, nước bay hơi không đáng kể) thu được dung dịch có khối lượng giảm so với ban đầu là 17,15 gam. Giá trị của a là
A. 0,5.
B. 0,2.
C. 0,3.
D. 0,4.
Đáp án B
ne = It/F = 5.(96,5.60)/96500 = 0,3 mol
nCl- (0,5) > ne (0,3) => Cl- chưa bị điện phân ở anot.
Giả sử Cu2+ chưa bị điện phân hết => nCu = 0,3/2 = 0,15 mol
nCl2 = 0,3/2 = 0,15 mol
m dung dịch giảm = mCu+mCl2 = 0,15.64 + 0,15.71 = 20,15 gam => Loại
=> Cu2+ bị điện phân hết, H2O đã bị điện phân ở catot.
Catot:
Cu2+ + 2e → Cu
x → 2x →x
H2O + 1e → OH- + 0,5H2
0,3-2x → 0,15-x
Anot:
Cl- - 1e → 0,5Cl2
0,3→ 0,15
m dung dịch giảm = mCu + mH2 + mCl2 => 17,15 = 64x + 2(0,15-x) + 0,15.71 => x = 0,1mol
=> a = 0,1/0,5 = 0,2 mol/lít
Điện phân dung dịch A chứa x mol CuSO4 và 0,24 mol KCl (điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi) trong thời gian t giây, thu được 3,136 lít khí ở anot (đktc). Nếu thời gian điện phân là 2t giây thì tổng thể tích khí thu được ở cả hai điện cực là 8,288 lít (đktc) và dung dịch sau điện phân là dung dịch X (thể tích 1 lít) có pH là y. Biết hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch. Giá trị của x và y là
A. 0,15 và 0,57
B. 0,17 và 0,57
C. 0,15 và 1,0
D. 0,17 và 1,0
Chọn đáp án D
nKhí ở anot = 0,14 > 0,24/2 Þ Có tạo O2 với nO2 = 0,14 – 0,24/2 = 0,02
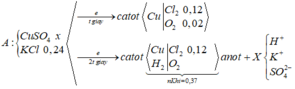
Tại t giây có ne = 0,12 x 2 + 0,02 x 4 = 0,32 Þ Tại 2t giây có ne = 0,32 x 2 = 0,64
Þ nO2 tại 2t giây = (0,64 - 0,12 x 2)/4 = 0,1 Þ nH2 = 0,37 - 0,12 - 0,1 = 0,15
Þ nCu tại 2t giây = 0,64/2 - 0,15 = 0,17 Þ x = 0,17 Þ nSO42- trong X = 0,17
BTNT.K Þ nK+ = 0,24; BTĐT trong X Þ nH+ = 0,17 x 2 - 0,24 = 0,1 Þ [H+] = 0,1M Þ pH = y = 1
Điện phân 200 ml dung dịch Y gồm KCl 0,1M và C u N O 3 2 0,2M với cường độ dòng điện 5A trong thời gian 1158 giây, điện cực trơ, màng ngăn xốp. Giả sử nước bay hơi không đáng kể. Độ giảm khối lượng của dung dịch sau khi điện phân là
A. 3,59 gam
B. 2,31 gam
C. 1,67 gam
D. 2,95 gam
Điện phân dung dịch A chứa x mol C u S O 4 và 0,24 mol KCl (điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi) trong thời gian t giây, thu được 3,136 lít khí ở anot (đktc). Nếu thời gian điện phân là 2t giây thì tổng thể tích khí thu được ở cả hai điện cực là 8,288 lít (đktc) và dung dịch sau điện phân là dung dịch X (thể tích 1lít) có pH là y. Biết hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch. Giá trị của x, y là
A. 0,15; 0,57
B. 0,17; 0,57
C. 0,15; 1
D. 0,17; 1
Đáp án D
Thời gian điện phân t:
n k h í = 3 , 136 22 , 4 = 0,14 mol
Anot:
Cl- → Cl2 +2e
0,24 0,12 0,24 mol
H2O → H+ + O2 + 4e
0,02 0,08 mol
ne trao đổi = 0,32 mol
ne trao đổi = I t F
=> thời gian 2t, ne trao đổi = 0,64 mol
thời gian điện phân 2t nkhí = 0,37 mol
khi đó anot :
Cl- → Cl2 + 2e
0,24 0,12 0,24 mol
H2O → H+ + O2 + 4e
0,1 0,4 mol
=> n H 2 = 0,37- 0,12 – 0,1 = 0,15 mol
catot:
Cu2+ +2e → Cu
x 2x x mol
H2O + 2e → 2OH- + H2
0,15 0,3 0,3 0,15 mol
2x+0,3 = 0,64
=> x = 0,17 mol
mặt khác
nH+ =0,1 mol ⇒ [H+] = 0,1
⇒ pH = 1