Điện phân (điện cực trơ) dung dịch muối sunfat của một kim loại hoá trị II với cường độ dòng điện 3A, sau 1930 giây thấy khối lượng catot tăng 1,68 gam. Tên kim loại là
A. Fe
B. Cu
C. Al
D. Ni
Điện phân (điện cực trơ) dung dịch muối sunfua của một kim loại hóa trị II với dòng điện cường độ 3A. Sau khi 1930 giây điện phân thấy khối lượng catot tăng 1,92 gam. Xác định tên kim loại.
Theo định luật Faraday ta có khối lượng chất thoát ra ở điện cực là :
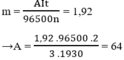
Trong đó A là nguyên tử khối
A = 64 ⇒ A là Cu
Điện phân (với điện cực trơ) dung dịch muối sunfat của một kim loại hóa trị II với I = 3A. Sau 1930 giây điện phân thấy khối lượng catot tăng 1,92g. Kim loại đó là
A. Zn.
B. Ba.
C. Ca.
D. Cu.
Điện phân (với điện cực trơ) dung dịch muối sunfat của một kim loại hóa trị II với I = 3A. Sau 1930 giây điện phân thấy khối lượng catot tăng 1,92g. Kim loại đó là:
A. Cu
B. Ba
C. Ca
D. Zn
Đáp án A
Quá trình điện phân: M2+ + 2e → M
Có: ne = I.t/F = 3.1930/96500 = 0,06 mol
=> nM = ½ ne = 0,03 mol
=> MM = 1,92: 0,03 = 64 (g/mol) => Cu
Điện phân bằng điện cực trơ dung dịch muối sunfat của kim loại hoá trị II với dòng điện có cường độ 6A. Sau 29 phút điện phân thấy khối lượng catot tăng 3,45 g. Kim loại đó là
A. Zn
B. Cu
C. Ni
D. Sn
Điện phân (điện cực trơ) dung dịch muối sunfua của một kim loại hóa trị II với dòng điện cường độ 3A. Sau khi 1930 giây điện phân thấy khối lượng catot tăng 1,92 gam.
Viết phương trình hóa học của phản ứng xảy ra tại mỗi điện cực và phương trình hóa học chung của sự điện phân.
Điện phân (điện cực trơ) dung dịch muối sunfua của một kim loại hóa trị II với dòng điện cường độ 3A. Sau khi 1930 giây điện phân thấy khối lượng catot tăng 1,92 gam.
a. Viết phương trình hóa học của phản ứng xảy ra tại mỗi điện cực và phương trình hóa học chung của sự điện phân.
b. Xác định tên kim loại.
\(a.Catot:M^{2+}+2e\rightarrow M\\ Anot:2H_2O\rightarrow4H^++O_2+4e\\ PTHH:2MSO_4+2H_2O-^{đp}\rightarrow2M+O_2+2H_2SO_4\\ b.m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,92\\ \Rightarrow A=64\left(Cu\right)\)
điện phân dung dịch muối clorua của kim loại hoá trị 2 với dòng điện cường độ 5A sau 1800 giây, thấy khối lượng catot tăng 3,03 gam . a) xác định kim loại đó b) viết sơ đồ điện phân dung dịch muối trên
a) Gọi CTHH của muối đó là XCl2
X+2 + 2e --> X
Có \(m=\dfrac{AIt}{nF}=\dfrac{M_X.5.1800}{2.96500}\)
=> \(M_X=65\left(Zn\right)\)
b)
Ở catot: Zn2+ + 2e --> Zn
Ở anot: 2Cl- --> Cl2 + 2e
\(ZnCl_2\underrightarrow{đpdd}Zn+Cl_2\)
Điện phân với điện cực trơ, cường độ dòng điện không đổi dung dịch muối nitrat của một kim loại M (có hóa trị không đổi). Sau thời gian t giây thấy khối lượng dung dịch giảm 6,96 gam và tại catot chỉ thu được a gam kim loại M. Sau thời gian 2t giây khối lượng dung dịch giảm 11,78 gam và tại catot thoát ra 0,224 lít khí (đktc). Giá trị của a là:
A. 8,64
B. 6,40
C. 6,48
D. 5,60
27/ Điện phân ( điện cực trơ) dd muối sunfat của một KL hóa trị II với cđdđ 3A, sau 1930 giây thấy khối lượng catot tăng 1,95g. Tên KL là ??
\(m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,95=>A=65\left(Zn\right)\)