Người ta dùng khí cacbon oxit để khử đồng (II) oxit. Nếu khử a gam đồng (II) oxit thì thu được bao nhiêu gam đồng?

Những câu hỏi liên quan
Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit clohidric hãy cho biết nếu dùng thể tích khí hidro ở trên để khử 20g đồng (II) oxit thì thu được bao nhiêu gam đồng
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=n_{Mg}=0,2\left(mol\right)\\ n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\\ CuO+H_2\underrightarrow{^{to}}Cu+H_2O\\ Vì:\dfrac{0,25}{1}>\dfrac{0,2}{1}\\ \Rightarrow CuOdư\\ \Rightarrow n_{Cu}=n_{H_2}=0,2\left(mol\right)\\ m_{Cu}=0,2.64=12,8\left(g\right)\)
Đúng 2
Bình luận (0)
\(n_{Mg}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,2
\(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
Pt : \(H_2+CuO\rightarrow\left(t_o\right)Cu+H_2O|\)
1 1 1 1
0,2 0,25 0,2
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\)
⇒ H2 phản ứng hết , CuO dư
⇒ Tính toán dựa vào số mol của H2
\(n_{Cu}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{Cu}=0,2.64=12,8\left(g\right)\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Người ta dùng khí cacbon oxit để khử đồng (II) oxit. Cho a = 150g, hãy tính kết quả bằng số.
a = 150g
⇒ m C u = 0,8a = 0,8.150 = 120(g)
Đúng 0
Bình luận (0)
Khử 32 gam hỗn hợp sắt (III) oxit và đồng (II) oxit bằng khí H2 thì thu được 9 gam H2O. Khối lượng kim loại thu được là bao nhiêu?
Xem chi tiết
\(Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ \text{Theo PTHH : } n_{H_2} = n_{H_2O} = \dfrac{9}{18} = 0,5(mol)\\ \text{Bảo toàn khối lượng : } m_{Oxit} + m_{H_2} = m_{kim\ loại} + m_{H_2O}\\ \Rightarrow m_{kim\ loại} = 32 + 0,5.2 - 9 = 24(gam)\)
Đúng 2
Bình luận (0)
\(n_{H_2O}=n_{H_2}=\dfrac{9}{18}=0.5\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{t^0}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)
\(BTKL:\)
\(m_{oxit}+m_{H_2}=m_{kl}+m_{H_2O}\)
\(\Rightarrow m_{kl}=32+0.5\cdot2-0.5\cdot18=24\left(g\right)\)
Đúng 0
Bình luận (0)
9, Người ta dùng hidro để khử m gam đồng ( II ) oxit, hãy tính khối lượng đồng thu được và tính cụ thể với m = 20 gam
Ta có: \(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
\(PTHH:CuO+H_2\overset{t^o}{--->}Cu+H_2O\)
Theo PT: \(n_{Cu}=n_{CuO}=0,25\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,25.64=16\left(g\right)\)
Đúng 2
Bình luận (0)
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?. b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao? c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
Đọc tiếp
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?.
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 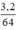 = 0,05 mol
= 0,05 mol
nFe = 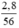 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 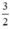 . nFe =
. nFe = 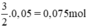 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 12,8 gam đồng trong lọ chứa khí oxi
a) Viết PTHH xảy ra.
b) Tính khối lượng đồng(II)oxit thu được.
c) Tính thể tích khí Hidro (đktc) cần dùng để khử hoàn toàn lượng đồng (II)oxit trên ở nhiệt độ cao.
a. Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit, và sắt (III) oxit ở nhiệt đô thích hợp?
b.Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c. Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,80 gam sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxi và sắt (III) oxit là bao nhiêu?
Đọc tiếp
a. Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit, và sắt (III) oxit ở nhiệt đô thích hợp?
b.Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c. Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,80 gam sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxi và sắt (III) oxit là bao nhiêu?
a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
Đúng 0
Bình luận (0)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)
Đúng 0
Bình luận (1)
a) Phương trình hoá học của các phản ứng:
H2 + CuO —> Cu + H2O (1)
3H2 + Fe2O3 —> Fe + 3H2O (2)
b) Trong phản ứng (1), (2): Chất khử là H2 vì chiếm oxi của chất khác, chất oxi hoá là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được: 6g - 2,8g = 3,2g
VH2 cần dùng (theo phương trình phản ứng (1)) :

VH2 cần dùng (theo phương trình phản ứng (2)) :

Đúng 0
Bình luận (0)
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
nCuO = 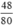 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.
Đúng 0
Bình luận (0)
Trộn 0,9 gam cacbon với 12,46 gam hỗn hợp gồm đồng(II) oxit và chì (II) oxit rồi nung nóng trong một môi trường không có không khí để oxit kim loại bị khử hết. Toàn bộ lượng khí sinh ra được dẫn vào dung dịch Ca(OH)_2dư, phản ứng xong thu được 6 gam kết tủa.a, Viết các phương trình hoá học xảy ra.b, Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp ban đầu.
Đọc tiếp
Trộn 0,9 gam cacbon với 12,46 gam hỗn hợp gồm đồng(II) oxit và chì (II) oxit rồi nung nóng trong một môi trường không có không khí để oxit kim loại bị khử hết. Toàn bộ lượng khí sinh ra được dẫn vào dung dịch Ca(OH)\(_2\)dư, phản ứng xong thu được 6 gam kết tủa.
a, Viết các phương trình hoá học xảy ra.
b, Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp ban đầu.
a) \(2CuO+C-^{t^o}\rightarrow2Cu+CO_2\)
\(2PbO+C-^{t^o}\rightarrow2Pb+CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
b) \(n_C=0,075\left(mol\right);n_{CO_2}=0,06\left(mol\right)\)
Vì nCO2 < nC => Sau phản ứng C dư
Gọi x,y là số mol của CuO, PbO
Ta có : \(\left\{{}\begin{matrix}\dfrac{1}{2}x+\dfrac{1}{2}y=0,06\\80x+223y=12,46\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,02\end{matrix}\right.\)
=> \(\%m_{CuO}=\dfrac{0,1.8}{12,46}.100=64,21\%\)
%m PbO =35,79%
Đúng 0
Bình luận (0)























